Aktivne sestavine: Fingolimod
GILENYA 0,5 mg trde kapsule
Indikacije Zakaj se zdravilo Gilenya uporablja? Za kaj je to?
Kaj je Gilenya
Zdravilna učinkovina v zdravilu Gilenya je fingolimod.
Čemu služi Gilenya
Zdravilo Gilenya se uporablja pri odraslih za zdravljenje recidivno remitentne multiple skleroze (MS), zlasti pri:
Bolniki, ki se na terapijo z MS niso odzvali.
ali
Bolniki s hitro razvijajočo se hudo MS.
Zdravilo Gilenya ne zdravi MS, vendar pomaga zmanjšati število recidivov in upočasniti napredovanje telesne okvare, ki jo povzroča MS.
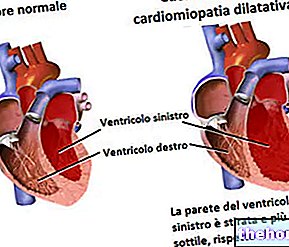
Kaj je multipla skleroza
MS je kronična bolezen, ki prizadene centralni živčni sistem (CNS), ki vključuje možgane in hrbtenjačo. Pri MS vnetje uniči zaščitno ovojnico (imenovano mielin), ki povezuje živce v osrednjem živčevju in preprečuje delovanje živcev, kot bi morali. Ta proces se imenuje demielinizacija.
Za ponavljajoče se remitentno MS je značilno ponavljajoče se napade (recidivi) nevroloških simptomov, ki odražajo vnetno stanje centralnega živčnega sistema. Simptomi se razlikujejo od bolnika do bolnika, običajno pa vključujejo težave pri hoji, odrevenelost, motnje vida ali ravnotežja.
Kako deluje Gilenya
Zdravilo Gilenya pomaga zaščititi živčni sistem pred napadi imunskega sistema, saj zmanjšuje sposobnost nekaterih belih krvnih celic (limfocitov), da prosto krožijo po telesu in jim preprečuje, da bi prišli do možganov in hrbtenjače. To omejuje poškodbe živcev, ki jih povzroča MS.
Kontraindikacije Kadar zdravila Gilenya ne smete uporabljati
Ne jemljite zdravila Gilenya
- če imate zmanjšan imunski odziv (zaradi sindroma imunske pomanjkljivosti, bolezni ali zdravil, ki zavirajo imunski sistem).
- če imate hudo okužbo ali kronično okužbo, na primer hepatitis ali tuberkulozo.
- če imate aktivnega raka (razen če gre za vrsto kožnega raka, imenovanega bazalnocelični kožni rak).
- če imate hude težave z jetri.
- če ste alergični na fingolimod ali katero koli sestavino tega zdravila.
Če kaj od naštetega velja za vas, povejte svojemu zdravniku, preden vzamete zdravilo Gilenya.
Previdnostni ukrepi pri uporabi Kaj morate vedeti, preden boste vzeli zdravilo Gilenya
Preden vzamete zdravilo Gilenya, se posvetujte s svojim zdravnikom:
- če imate nepravilen, nenormalen srčni utrip.
- če imate simptome nizkega srčnega utripa (npr. omotico, slabost ali palpitacije).
- če imate težave s srcem, zamašitev krvnih žil v srcu, ste v preteklosti imeli srčni napad ali srčni zastoj ali ste imeli angino pektoris.
- če ste v preteklosti imeli možgansko kap.
- če imate srčno popuščanje.
- če imate med spanjem hude težave z dihanjem (huda apneja med spanjem).
- če so vam povedali, da imate nenormalen EKG.
- če jemljete ali ste pred kratkim jemali zdravila za nepravilen srčni utrip, na primer kinidin, disopiramid, amiodaron ali sotalol.
- če jemljete ali ste pred kratkim jemali zdravila, ki upočasnjujejo bitje srca (na primer zaviralci adrenergičnih receptorjev beta, verapamil, diltiazem ali ivabradin, digoksin, antiholinesterazna zdravila ali pilokarpin).
- če ste kdaj imeli epizode nenadne izgube zavesti ali omedlevice (sinkopa).
- če se nameravate cepiti.
- če še niste imeli noric.
- če imate ali ste imeli motnje vida ali druge znake otekanja v predelu osrednjega vida (makula) na zadnji strani očesa (stanje, znano kot makularni edem, glejte spodaj), če imate ali ste imeli "vnetje ali" okužbo očesa (uveitis) ali če imate sladkorno bolezen (ki lahko povzroči težave z očmi).
- če imate težave z jetri
- če imate visok krvni tlak, ki ga zdravila ne morejo nadzorovati.
- če imate hude težave s pljuči ali če imate kašelj zaradi kajenja.
Če kaj od naštetega velja za vas, povejte svojemu zdravniku, preden vzamete zdravilo Gilenya.
Počasen srčni utrip (bradikardija) in nepravilen srčni utrip: Na začetku zdravljenja zdravilo Gilenya povzroči upočasnitev srčnega utripa. Posledično se lahko pojavijo omotica ali utrujenost, zavedanje srčnega utripa ali padec krvnega tlaka. Izrazito se obrnite na zdravnik, saj boste morda potrebovali takojšnje zdravljenje. Zdravilo Gilenya lahko povzroči tudi nepravilen srčni utrip, še posebej po prvem odmerku. Nepravilen srčni utrip se ponavadi normalizira v manj kot enem dnevu. Počasen srčni utrip se ponavadi vrne v normalno stanje v enem mesecu.
Zdravnik vas bo prosil, da po dajanju prvega odmerka zdravila Gilenya ostanete v kliniki ali bolnišnici vsaj 6 ur, med katerim vam bodo kadar koli izmerili pulz in krvni tlak: na ta način lahko sprejmete ustrezne ukrepe, če stranskih učinkov, ki se pojavijo na začetku zdravljenja. Pred prvim odmerkom zdravila Gilenya in po 6 urah spremljanja morate imeti na voljo elektrokardiogram. Zdravnik vam bo v tem obdobju morda neprekinjeno preverjal elektrokardiogram. Če po 6. ure, vaš srčni utrip je zelo nizek ali se zmanjša, ali če vaš EKG pokaže nenormalnosti, boste morda morali biti opazovani dlje časa (vsaj še 2 uri in morda do naslednjega jutra), dokler se te težave ne rešijo. enako se lahko zgodi, če ponovno vzame G ilenya po prekinitvi zdravljenja, odvisno od tega, kako dolgo je bila prekinitev in kako dolgo ste jemali zdravilo Gilenya pred prekinitvijo.
Če imate ali obstaja nevarnost nepravilnega ali nenormalnega srčnega utripa, če je vaš EKG nenormalen ali če imate srčno bolezen ali srčno popuščanje, zdravilo Gilenya morda ni primerno za vas.
Če ste kdaj imeli epizode nenadne izgube zavesti ali zmanjšanega srčnega utripa, zdravilo Gilenya morda ni primerno za vas. Obiskal vas bo kardiolog (specialist za srce), ki vam bo svetoval, kako začeti zdravljenje z zdravilom Gilenya, vključno s spremljanjem do naslednjega jutra.
Če jemljete zdravila, ki lahko povzročijo zmanjšanje srčnega utripa, zdravilo Gilenya morda ni primerno za vas. Obiskal vas bo kardiolog, ki bo ocenil, ali lahko kot alternativo jemljete zdravila, ki ne znižujejo srčnega utripa in vam omogočajo začetek zdravljenja z zdravilom Gilenya. Če ta sprememba terapije ni mogoča, vam bo kardiolog svetoval, kako začeti zdravljenje z zdravilom Gilenya, vključno s spremljanjem do naslednjega jutra.
Če še niste imeli noric: Če še niste imeli noric, bo zdravnik preveril vašo imunost proti virusu, ki ga povzroča (virus noric). Če niste zaščiteni pred virusom, boste pred začetkom zdravljenja z zdravilom Gilenya morda potrebovali cepljenje. Če se to zgodi, bo zdravnik odložil začetek zdravljenja z zdravilom Gilenya za največ en mesec po zaključku celotnega tečaja cepljenja.
Okužbe: Gilenya zmanjšuje število belih krvnih celic (zlasti limfocitov). Bele krvne celice se borijo proti okužbam. Med jemanjem zdravila Gilenya (in do 2 meseca po prekinitvi zdravljenja) lahko lažje pridete do okužbe. Vsaka obstoječa okužba se lahko poslabša. Okužbe so lahko resne in smrtno nevarne. Če menite, da imate okužbo, če imate povišano telesno temperaturo, če imate simptome gripe ali če imate glavobol, ki ga spremlja otrdel vrat, občutljivost na svetlobo, slabost in / ali zmedenost (to so lahko simptomi meningitisa), se obrnite na zdravnik takoj ..
Makularni edem: Pred začetkom zdravljenja z zdravilom Gilenya, če imate ali ste imeli motnje vida ali druge znake otekanja v predelu osrednjega vida (makula) na zadnji strani očesa, če imate ali ste imeli vnetje ali okužbo očesa (uveitis) ali če imate sladkorno bolezen, vas bo zdravnik morda prosil za pregled oči.
Zdravnik vas bo morda prosil za očesni pregled 3-4 mesece po začetku zdravljenja z zdravilom Gilenya.
Makula je majhno območje mrežnice, ki se nahaja v zadnjem delu očesa in vam omogoča, da jasno, ostro vidite oblike, barve in podrobnosti. Gilenya lahko povzroči otekanje makule, stanje, znano kot makularni edem. ponavadi v prvih 4 mesecih zdravljenja z zdravilom Gilenya.
Makularni edem se pogosteje pojavi, če imate sladkorno bolezen ali ste imeli "vnetje očesa", imenovano uveitis. V teh primerih vas bo zdravnik želel redno pregledovati glede prvih znakov makularnega edema.
Če ste imeli makularni edem, se pred ponovnim začetkom zdravljenja z zdravilom Gilenya posvetujte s svojim zdravnikom.
Makularni edem lahko povzroči nekatere vidne simptome (optični nevritis), ki se pojavijo tudi med napadi MS. V začetni fazi morda ne bo simptomov. Obvestite svojega zdravnika o vseh spremembah vida. Zdravnik vas bo morda prosil, da se obrnete nanje opravite očesni pregled, še posebej, če:
- osrednje območje gledanja ni izostreno ali ima sence;
- v osrednjem vidnem območju se razvije slepa pega;
- imate težave pri razlikovanju barv ali drobnih podrobnosti.
Preiskave delovanja jeter: Če imate hude težave z jetri, ne smete jemati zdravila Gilenya. Zdravljenje z zdravilom Gilenya lahko vpliva na delovanje jeter. Verjetno ne boste opazili nobenih simptomov, če pa opazite porumenelost kože ali belih oči, nenormalen temen urin ali nepojasnjeno slabost in bruhanje, takoj obvestite svojega zdravnika.
Če po začetku zdravljenja z zdravilom Gilenya opazite katerega od teh simptomov, takoj obvestite svojega zdravnika.
V prvih dvanajstih mesecih zdravljenja vas bo zdravnik zaprosil za krvne preiskave za preverjanje delovanja jeter. Če rezultati kažejo, da je prišlo do težav z jetri, bo zdravljenje z zdravilom Gilenya morda treba prekiniti.
Visok pritisk
Ker zdravilo Gilenya povzroči rahlo zvišanje krvnega tlaka, vam bo zdravnik morda redno pregledoval krvni tlak. Težave s pljuči Gilenya slabo vpliva na delovanje pljuč. Pri bolnikih s hudimi težavami s pljuči ali kašljem zaradi kajenja se lahko lažje pojavijo neželeni učinki.
Krvne slike Zaželeni učinek zdravljenja z zdravilom Gilenya je zmanjšanje količine belih krvnih celic v krvi, ki se običajno normalizirajo v 2 mesecih po prekinitvi zdravljenja. Če morate opraviti krvne preiskave, povejte svojemu zdravniku, da jemljete zdravilo Gilenya .
Pred začetkom zdravljenja z zdravilom Gilenya vam bo zdravnik potrdil, ali je število belih krvnih celic zadostno, in vas morda prosil, da ga redno ponavljate. Če nimate dovolj belih krvnih celic, boste morda morali prenehati jemati zdravilo Gilenya.
Sindrom zadnje reverzibilne encefalopatije (PRES)
Pri bolnikih z multiplo sklerozo, zdravljenih z zdravilom Gilenya, so redko poročali o sindromu, imenovanem posteriorna reverzibilna encefalopatija (PRES). Simptomi lahko vključujejo nenaden pojav hudega glavobola, zmedenost, epileptične napade in spremembe vida. Povejte svojemu zdravniku, če se med zdravljenjem z zdravilom Gilenya pojavi kateri od teh simptomov.
Uporaba pri starejših
Izkušnje z zdravilom Gilenya pri starejših bolnikih, starejših od 65 let, so omejene. Če imate dodatna vprašanja, se posvetujte z zdravnikom.
Otroci in mladostniki
Zdravilo Gilenya ni namenjeno uporabi pri otrocih in mladostnikih, mlajših od 18 let, saj pri bolnikih z MS, mlajšim od 18 let, ni bilo raziskano.
Interakcije Katera zdravila ali živila lahko spremenijo učinek zdravila Gilenya
Povejte svojemu zdravniku ali farmacevtu, če jemljete, ste pred kratkim jemali ali pa boste morda začeli jemati katero koli drugo zdravilo. Povejte svojemu zdravniku, če jemljete katero od naslednjih zdravil:
- Zdravila, ki zavirajo ali spreminjajo imunski sistem, vključno z drugimi zdravili za zdravljenje MS, kot so interferon beta, glatiramer acetat, natalizumab, mitoksantron, teriflunomid, dimetil fumarat ali alemtuzumab. Zdravila Gilenya ne smete uporabljati s temi zdravili, ker lahko okrepijo učinek na imunski sistem (glejte tudi "Ne jemljite zdravila Gilenya").
- Kortikosteroidi, zaradi možnega aditivnega učinka na imunski sistem.
- Cepiva. Če se morate cepiti, se najprej posvetujte z zdravnikom. Med zdravljenjem z zdravilom Gilenya in do 2 meseca po njem ne smete prejemati nekaterih vrst cepiv (živih oslabljenih cepiv), saj lahko sprožijo okužbo, ki naj bi jo preprečili. ...
- Zdravila, ki upočasnijo srčni utrip (na primer zaviralci adrenergičnih receptorjev beta, na primer atenolol). Sočasna uporaba zdravila Gilenya s temi zdravili bi lahko okrepila učinek na srčni utrip v prvih dneh zdravljenja z zdravilom Gilenya.
- Zdravila za nepravilen srčni utrip, kot so kinidin, disopiramid, amiodaron ali sotalol. Zdravnik se lahko odloči, da zdravila Gilenya ne bo predpisal, če jemljete tovrstna zdravila, saj lahko okrepijo učinek na nepravilen srčni utrip.
- Druga zdravila:
- zaviralci proteaz, protiinfekcijska sredstva, kot so ketokonazol, azolne protiglivične snovi, klaritromicin ali telitromicin.
- karbamazepin, rifampicin, fenobarbital, fenitoin, efavirenz ali šentjanževka (potencialno tveganje za zmanjšano učinkovitost).
Opozorila Pomembno je vedeti, da:
Nosečnost in dojenje
Pred začetkom zdravljenja z zdravilom Gilenya vas bo zdravnik morda pozval, da opravite test nosečnosti, da se prepričate, da niste noseči. Med jemanjem zdravila Gilenya ali dva meseca po prekinitvi zdravljenja se izogibajte zanositvi, saj obstaja nevarnost škode za otroka. Posvetujte se s svojim zdravnikom o zanesljivih metodah kontracepcije, ki jih lahko uporabljate med zdravljenjem z zdravilom Gilenya in še 2 meseca po prekinitvi zdravljenja. .
Če med jemanjem zdravila Gilenya zanosite, prekinite zdravljenje in takoj obvestite svojega zdravnika. Zdravnik se bo z vami odločil, kaj je najboljše za vas in vašega otroka.
Med jemanjem zdravila Gilenya ne dojite. Zdravilo Gilenya se izloča v materino mleko s tveganjem za resne neželene učinke pri novorojenčku.
Preden vzamete katerokoli zdravilo, se posvetujte z zdravnikom ali farmacevtom.
Vpliv na sposobnost upravljanja vozil in strojev
Zdravnik vam bo povedal, ali vam bolezen omogoča varno vožnjo in upravljanje strojev. Pričakuje se, da zdravilo Gilenya ne vpliva na sposobnost vožnje in upravljanja s stroji.
Na začetku zdravljenja pa boste morali po prvem odmerku zdravila Gilenya ostati v bolnišnici ali bolnišnici 6 ur. V tem času se lahko zmanjša sposobnost vožnje in upravljanja s stroji, lahko pa tudi dlje.
Odmerjanje in način uporabe Kako uporabljati zdravilo Gilenya: Odmerjanje
Zdravljenje z zdravilom Gilenya bo nadzoroval zdravnik z izkušnjami pri zdravljenju multiple skleroze.
Pri jemanju tega zdravila natančno upoštevajte zdravnikova navodila.
Če ste v dvomih, se posvetujte z zdravnikom. Odmerek je ena kapsula enkrat na dan. Zdravilo Gilenya vzemite enkrat na dan s kozarcem vode.Gilenyo lahko vzamete s hrano ali brez nje.
Jemanje zdravila Gilenya vsak dan ob istem času vam bo pomagalo, da se spomnite, kdaj jemati zdravilo.
Ne prekoračite priporočenega odmerka.
Zdravnik vas lahko neposredno preklopi z zdravljenja z interferonom beta, glatiramer acetatom ali dimetil fumaratom na zdravilo Gilenya, če ni znakov nenormalnosti, ki jih povzroča prejšnje zdravljenje. Zdravnik vam bo morda dal krvno preiskavo za izključitev teh nepravilnosti. Po prenehanju uporabe natalizumaba bo morda treba počakati 2-3 mesece, preden se začne zdravljenje z zdravilom Gilenya. Za prehod s teriflunomida vam bo zdravnik morda svetoval, da počakate nekaj časa ali nadaljujete s pospešenim postopkom izločanja. Če ste bili zdravljeni z alemtuzumabom, morate skrbno oceniti in se pogovoriti z zdravnikom, da ugotovite, ali je zdravilo Gilenya primerno za vas.
Če niste prepričani, kako dolgo boste jemali zdravilo Gilenya, se posvetujte z zdravnikom ali farmacevtom.
Preveliko odmerjanje Kaj storiti, če ste vzeli preveč zdravila Gilenya
Če ste vzeli večji odmerek zdravila Gilenya, kot bi smeli
Če ste vzeli preveč kapsul zdravila Gilenya, takoj obvestite svojega zdravnika.
Če ste pozabili vzeti zdravilo Gilenya
Če jemljete zdravilo Gilenya manj kot 1 mesec in pozabite vzeti 1 odmerek za cel dan, se pred naslednjim odmerkom posvetujte s svojim zdravnikom. Zdravnik se bo morda odločil, da vas bo opazoval pri naslednjem odmerku.
Če jemljete zdravilo Gilenya vsaj 1 mesec in ste pozabili vzeti zdravilo več kot 2 tedna, se pred naslednjim odmerkom posvetujte z zdravnikom. Zdravnik se bo morda odločil, da vas bo opazoval pri naslednjem odmerku. Če pa ste pozabili vzeti zdravilo 2 tedna ali manj, lahko naslednji odmerek vzamete po načrtu.
Nikoli ne vzemite dvojnega odmerka, da bi nadomestili pozabljeni odmerek.
Če ste prenehali jemati zdravilo Gilenya
Ne prenehajte jemati zdravila Gilenya ali spremenite odmerka, ne da bi se prej pogovorili s svojim zdravnikom.
Zdravilo Gilenya bo po prenehanju zdravljenja ostalo v telesu do 2 meseca. Število belih krvnih celic (limfocitov) lahko v tem času ostane nizko, neželeni učinki, opisani v tem navodilu, pa se lahko še vedno pojavijo. Po prekinitvi zdravljenja z zdravilom Gilenya bo morda treba počakati 6-8 tednov pred začetkom novega zdravljenja multiple skleroze.
Če morate po več kot 2 tednih po prekinitvi zdravljenja znova zagnati zdravilo Gilenya, se lahko znova pojavi učinek na srčni utrip, ki se običajno pojavi na začetku zdravljenja.bolnišnica pod nadzorom zdravnik.
Če imate dodatna vprašanja o uporabi tega zdravila, se posvetujte z zdravnikom ali farmacevtom
Neželeni učinki Kakšni so neželeni učinki zdravila Gilenya
Kot vsa zdravila ima lahko tudi to zdravilo neželene učinke, ki pa se ne pojavijo pri vseh bolnikih.
Nekateri neželeni učinki so lahko resni ali pa postanejo resni
Pogosti (pojavijo se lahko pri največ 1 od 10 oseb):
- Kašelj s sluznico, nelagodje v prsih, zvišana telesna temperatura (znaki pljučnih motenj)
- Okužba z virusom herpesa (ogenj sv. Antona ali herpes zoster) s simptomi, kot so mehurji, pekoč občutek, srbenje ali bolečina v koži, običajno v zgornjem delu telesa ali na obrazu. Drugi simptomi so lahko zvišana telesna temperatura in šibkost v zgodnjih fazah okužba, ki ji sledi odrevenelost, srbenje ali rdeče lise s hudo bolečino
- Počasen srčni utrip (bradikardija), nepravilen srčni ritem
Občasni (pojavijo se lahko pri največ 1 od 100 bolnikov):
- Pljučnica s simptomi, kot so zvišana telesna temperatura, kašelj, težko dihanje
- Makularni edem (otekanje v osrednjem vidnem predelu mrežnice na zadnji strani očesa) s simptomi, kot so sence ali slepe pege v središču vida, zamegljen vid, težave pri razlikovanju barv ali podrobnosti
Redki (pojavijo se lahko pri največ 1 od 1.000 bolnikov):
- Sindrom, imenovan posteriorna reverzibilna encefalopatija. Simptomi lahko vključujejo nenaden pojav hudega glavobola, zmedenost, epileptične napade in / ali motnje vida
Posamezni primeri:
- Kriptokokne okužbe (vrsta glivične okužbe), vključno s kriptokoknim meningitisom s simptomi, kot so glavobol, ki ga spremlja otrdelost vratu, občutljivost na svetlobo, slabost in / ali zmedenost.
Če opazite katerega od teh neželenih učinkov, takoj obvestite svojega zdravnika.
Drugi stranski učinki
Zelo pogosti (pojavijo se lahko pri več kot 1 od 10 bolnikov):
- Okužba z virusom gripe s simptomi, kot so utrujenost, mrzlica, vneto grlo, bolečine v sklepih ali mišicah, zvišana telesna temperatura
- Občutek pritiska ali bolečine v licih in čelu (sinusitis)
- Glavobol
- Driska
- Bolečine v hrbtu
- Krvni testi kažejo višje ravni jetrnih encimov
- Kašelj
Pogosti (pojavijo se lahko pri največ 1 od 10 oseb):
- Lišaj, "glivična okužba kože (pityriasis versicolor)
- Vrtoglavica
- Močan glavobol, ki ga pogosto spremljajo slabost, bruhanje in občutljivost na svetlobo (migrena)
- Nizke ravni belih krvnih celic (limfociti, levkociti)
- Slabost
- Kožni izpuščaj s srbenjem, rdečico in pekočino (ekcem)
- Srbenje
- Zvišane ravni maščob (trigliceridov) v krvi
- Izguba las
- Piskanje
- Depresija
- Zamegljen vid (glejte tudi poglavje o "makularnem edemu" Nekateri neželeni učinki so lahko ali postanejo resni))
- Hipertenzija (Gilenya lahko povzroči rahlo zvišanje krvnega tlaka)
Občasni (pojavijo se lahko pri največ 1 od 100 bolnikov):
- Nizke ravni nekaterih belih krvnih celic (nevtrofilcev)
- Depresivno razpoloženje
Redki (pojavijo se lahko pri največ 1 od 1.000 bolnikov):
- Bolezni krvnih žil
- Motnje živčnega sistema
- Rak limfnega sistema (limfom)
Neznana (pogostnosti iz razpoložljivih podatkov ni mogoče oceniti):
- Alergijska reakcija in kožni izpuščaj
Če se kateri od teh neželenih učinkov resno pojavi, obvestite svojega zdravnika.
Poročanje o stranskih učinkih
Če opazite kateri koli neželeni učinek, se posvetujte z zdravnikom ali farmacevtom, kar vključuje morebitne neželene učinke, ki niso navedeni v tem navodilu. O neželenih učinkih lahko poročate tudi neposredno prek nacionalnega sistema poročanja, navedenega v Dodatku V. S poročanjem o neželenih učinkih lahko pomagate zagotoviti več informacij o varnosti tega zdravila.
Potek in hramba
Zdravilo shranjujte nedosegljivo otrokom!
Tega zdravila ne smete uporabljati po datumu izteka roka uporabnosti, ki je naveden na škatli in pretisnem omotu poleg oznake "EXP" / "EXP". Rok uporabnosti se nanaša na zadnji dan navedenega meseca.
Shranjujte pri temperaturi do 25 ° C.
Shranjujte v originalni ovojnini za zaščito zdravila pred vlago.
Ne uporabljajte paketov, ki so poškodovani ali kažejo znake nedovoljenega dostopa.
Ne mečite nobenih zdravil v odpadne vode ali med gospodinjske odpadke. Vprašajte svojega farmacevta, kako zavreči zdravila, ki jih ne uporabljate več. Tako boste zaščitili okolje.
Kaj vsebuje zdravilo Gilenya
- Zdravilna učinkovina je fingolimod. Ena kapsula vsebuje 0,5 mg fingolimoda (v obliki hidroklorida).
- Pomožne snovi so: Vsebina kapsule: magnezijev stearat, manitol Ovojnica kapsule: rumeni železov oksid (E172), titanov dioksid (E171), želatinsko črnilo: lak (E904), dehidriran alkohol, izopropil alkohol, butil alkohol, propilenglikol, prečiščena voda , koncentrirana raztopina amoniaka, kalijev hidroksid, črni železov oksid (E172), rumeni železov oksid (E172), titanov dioksid (E171), dimetikon
Izgled zdravila Gilenya in vsebina pakiranja
Gilenya 0,5 mg trde kapsule imajo neprozorno belo neprozorno telo in globoko rumeno neprozorno kapico. Na glavi je vgraviran črni napis "FTY0,5mg", na telesu pa dve rumeni pasovi.
Zdravilo Gilenya je na voljo v pakiranjih s 7, 28 ali 98 kapsulami ali v več pakiranjih s 84 kapsulami (3 pakiranja po 28 kapsul). Na trgu ni vseh navedenih pakiranj.
Navodilo za uporabo vira: AIFA (Italijanska agencija za zdravila). Vsebina, objavljena januarja 2016. Prisotne informacije morda niso posodobljene.
Za dostop do najnovejše različice je priporočljivo dostopati do spletnega mesta AIFA (Italijanska agencija za zdravila). Zavrnitev odgovornosti in koristne informacije.
01.0 IME ZDRAVILA
GILENYA 0,5 MG Trdne kapsule
▼ Zdravilo je predmet dodatnega spremljanja. To bo omogočilo hitro identifikacijo novih varnostnih informacij. Zdravstvene delavce prosimo, da poročajo o vseh domnevnih neželenih učinkih. Za informacije o poročanju o neželenih učinkih glejte poglavje 4.8.
02.0 KAKOVOSTNA IN KOLIČINSKA SESTAVA
Ena trda kapsula vsebuje 0,5 mg fingolimoda (v obliki hidroklorida).
Za celoten seznam pomožnih snovi glejte poglavje 6.1.
03.0 FARMACEVTSKA OBLIKA
Trda kapsula.
16 -milimetrska kapsula z intenzivno rumeno neprozorno kapico in belim neprozornim telesom; črna gravura "FTY0,5 mg" na glavi in dva okrogla rumena traka, vgravirana na telesu.
04.0 KLINIČNE INFORMACIJE
04.1 Terapevtske indikacije
Zdravilo Gilenya je samostojno indicirano kot zdravilo za spreminjanje bolezni pri zelo aktivni recidivno remitentni multipli sklerozi v naslednjih skupinah odraslih bolnikov:
- Bolniki z visoko aktivnostjo bolezni kljub zdravljenju z vsaj eno terapijo spreminjanje bolezni (glejte poglavji 4.4 in 5.1 za izjeme in informacije o izperi).
Te bolnike lahko opredelimo kot tiste, ki se niso odzvali na celoten in ustrezen potek terapije (običajno vsaj eno leto zdravljenja) z vsaj eno terapijo spreminjanje bolezni. Bolniki so morali imeti v preteklem letu med zdravljenjem vsaj 1 ponovitev bolezni in imeti vsaj 9 hiperintenzivnih lezij T2 na MRI možganov ali vsaj 1 lezijo, ki povečuje gadolinij. En bolnik neodzivni opredelimo ga lahko tudi kot bolnika, ki ima nespremenjeno ali povečano stopnjo recidiva v primerjavi s prejšnjim letom ali ima hude relapse.
ali
-Bolniki s hitro razvijajočo se hudo recidivno-remitentno multiplo sklerozo, opredeljeno z dvema ali več onesposobljenimi relapsi v enem letu, in z 1 ali več lezijami, ki povečujejo gadolinij na MRI možganov, ali z znatnim povečanjem obremenitve lezije T2 v primerjavi s prejšnjo MRI v zadnjem času izvede.
04.2 Odmerjanje in način uporabe
Zdravljenje mora začeti in nadzorovati zdravnik z izkušnjami z multiplo sklerozo.
Odmerjanje
Priporočeni odmerek zdravila Gilenya je ena 0,5 mg kapsula, ki se jemlje peroralno enkrat na dan. Zdravilo Gilenya lahko jemljete med obroki in proč od njih.
Priporoča se enako spremljanje kot na začetku zdravljenja po prvem odmerku, če se zdravljenje prekine zaradi:
• 1 ali več dni v prvih dveh tednih zdravljenja
• več kot 7 dni v tretjem in četrtem tednu zdravljenja
• več kot 2 tedna po enem mesecu zdravljenja.
Če je prekinitev zdravljenja krajša od zgoraj opisane, je treba zdravljenje nadaljevati z dajanjem naslednjega odmerka, kot je bilo načrtovano (glejte poglavje 4.4).
Posebne populacije
Upokojenci
Zdravilo Gilenya je treba uporabljati previdno pri bolnikih, starih 65 let ali več, ker ni na voljo dovolj podatkov o varnosti in učinkovitosti (glejte poglavje 5.2).
Moteno delovanje ledvic
V glavnih ključnih študijah, izvedenih pri multipli sklerozi, zdravila Gilenya pri bolnikih z okvarjenim delovanjem ledvic niso preučevali. Na podlagi kliničnih farmakoloških študij pri bolnikih z blago do hudo ledvično okvaro prilagoditev odmerka ni potrebna.
Moteno delovanje jeter
Zdravila Gilenya se ne sme uporabljati pri bolnikih s hudo okvaro jeter (razred C po Child-Pughu) (glejte poglavje 4.3). Čeprav pri bolnikih z blago ali zmerno okvaro jeter prilagajanje odmerka ni potrebno, je pri uvedbi zdravljenja pri teh bolnikih priporočljiva previdnost (glejte poglavji 4.4 in 5.2).
Bolniki s sladkorno boleznijo
Zdravila Gilenya niso preučevali pri bolnikih z multiplo sklerozo in sladkorno boleznijo. Pri teh bolnikih je treba zdravilo Gilenya uporabljati previdno zaradi možnega povečanega tveganja za edem makule (glejte poglavji 4.4 in 4.8). Ti bolniki morajo redno opraviti oftalmološke preglede glede znakov makularnega edema.
Pediatrična populacija
Varnost in učinkovitost zdravila Gilenya pri otrocih, starih od 0 do 18 let, še nista bili ugotovljeni, trenutno razpoložljivi podatki so opisani v poglavju 5.2, vendar ni mogoče dati priporočil o odmerjanju.
04.3 Kontraindikacije
- Diagnosticiran sindrom imunske pomanjkljivosti.
- Bolniki, pri katerih obstaja večje tveganje za oportunistične okužbe, vključno z bolniki z oslabljenim imunskim sistemom (vključno s tistimi, ki se zdravijo s sočasno imunosupresivno terapijo, ali tistimi, ki so imunsko oslabljeni s prejšnjimi terapijami).
- Hude aktivne okužbe, kronične aktivne okužbe (hepatitis, tuberkuloza).
- Diagnosticirani aktivni maligni tumorji, razen pri bolnikih z bazalnoceličnim kožnim rakom.
- Huda okvara jeter (razred C po Child-Pughu).
- Preobčutljivost za zdravilno učinkovino ali katero koli pomožno snov, navedeno v poglavju 6.1.
04.4 Posebna opozorila in ustrezni previdnostni ukrepi za uporabo
Bradiaritmija
Začetek zdravljenja z zdravilom Gilenya povzroči prehodno znižanje srčnega utripa in je lahko povezan tudi z zamudo pri atrioventrikularni prevodnosti, vključno z izoliranimi epizodami popolne, prehodne in spontano izzvenele atrioventrikularne blokade (glejte poglavji 4.8 in 5.1).
Po dajanju prvega odmerka se zmanjšanje srčnega utripa začne v eni uri in je največ v prvih 6 urah. V naslednjih dneh ta učinek po odmerku traja, čeprav je na splošno manj intenziven, in se običajno v naslednjih tednih zmanjša ... Pri nadaljevanju dajanja se povprečni srčni utrip v enem mesecu vrne na izhodiščno vrednost, vendar se pri nekaterih bolnikih srčni utrip morda ne bo vrnil na izhodiščno vrednost do konca prvega meseca. zdravljenje in izzvenelo v prvih 24 urah po začetku zdravljenja. Zmanjšanje srčnega utripa, ki ga povzroči fingolimod, je po potrebi mogoče odpraviti s parenteralno uporabo odmerkov atropina ali izoprenalina.
Vsi bolniki morajo imeti elektrokardiogram in izmeriti krvni tlak pred prvim odmerkom zdravila Gilenya in po 6 urah. Vse bolnike je treba 6 ur spremljati glede znakov in simptomov bradikardije z urnim merjenjem srčnega utripa in krvnega tlaka.V teh 6 urah je priporočljivo stalno spremljanje EKG v realnem času.
Če se po dajanju pojavijo simptomi bradiaritmije, je treba začeti ustrezne postopke vodenja kliničnih bolnikov in spremljati, dokler simptomi ne izginejo. Če bolnik med spremljanjem po prvem odmerku potrebuje farmakološki poseg, ga je treba spremljati do naslednjega jutra v bolnišnici in ga je treba ponoviti po drugem odmerku zdravila Gilenya.
Če je po 6 urah vrednost srčnega utripa najnižja po prvem odmerku (kar kaže na to, da največji farmakodinamični učinek na srce morda še ni očiten), je treba spremljanje nadaljevati vsaj 2 uri in do srca hitrost se spet poveča.Potrebno je tudi dodatno spremljanje (vsaj do naslednjega jutra in v vsakem primeru do odprave simptomov), če po 6 urah po dajanju prvega odmerka srčni utrip utripa na minuto ali če elektrokardiogram pokaže nov začetek atrioventrikularne blokade druge stopnje ali višjo ali če je interval QTc ≥500 msek. Začetek atrioventrikularne blokade tretje stopnje kadar koli mora povzročiti tudi podaljšanje spremljanja (vsaj do naslednjega jutra).
Zaradi nevarnosti hudih motenj ritma se zdravila Gilenya ne sme uporabljati pri bolnikih z atrioventrikularno blokado druge stopnje Mobitza tipa II ali višjo, pri bolnikih s sindromom bolnega sinusa ali sinoatrijskim blokom, anamnezo simptomatske bradikardije ali ponavljajoče se sinkope ali pri bolnikih z znatnim podaljšanjem QT (QTc> 470 msec (ženske) ali> 450 msec (moški)). Ker se lahko pomembna bradikardija slabo prenaša pri bolnikih z znano ishemično boleznijo srca (vključno z angino pektoris), cerebrovaskularno boleznijo, anamnezo miokardnega infarkta, kongestivnim srčnim popuščanjem, anamnezo srčnega zastoja, nenadzorovano hipertenzijo ali hudo apnejo v spanju, se zdravila Gilenya ne sme uporabljati pri ti bolniki. Pri teh bolnikih je treba razmisliti o zdravljenju z zdravilom Gilenya le, če pričakovane koristi odtehtajo možna tveganja; če se odločimo za začetek zdravljenja z zdravilom Gilenya, se moramo pred začetkom zdravljenja posvetovati s kardiologom, ki bo določil najprimernejše spremljanje. Za začetek zdravljenja je priporočljivo spremljanje vsaj do naslednjega jutra (glejte tudi poglavje 4.5).
Zdravila Gilenya niso preučevali pri bolnikih z aritmijami, ki potrebujejo zdravljenje z antiaritmiki razreda Ia (npr. Kinidin, disopiramid) ali razreda III (npr. Amiodaron, sotalol). Antiaritmiki razreda Ia in razreda III so bili povezani s primeri torsades de pointes pri bolnikih z bradikardijo. Ker začetek zdravljenja z zdravilom Gilenya povzroči zmanjšanje srčnega utripa, se zdravila Gilenya ne sme uporabljati sočasno s temi zdravili.
Izkušnje z zdravilom Gilenya pri bolnikih, ki se sočasno zdravijo z zaviralci adrenergičnih receptorjev beta, zaviralci kalcijevih kanalčkov, ki povzročajo zmanjšanje srčnega utripa (na primer verapamil, diltiazem ali ivabradin), ali z drugimi zdravili, ki lahko zmanjšajo srčni utrip (npr. Digoksin, antiholinesterazna zdravila ali pilokarpin ) je omejeno.Ker je začetek zdravljenja z zdravilom Gilenya povezan tudi z zmanjšanim srčnim utripom (glejte tudi poglavje 4.8 Bradiaritmija), je lahko sočasna uporaba teh zdravil na začetku zdravljenja z zdravilom Gilenya povezana s hudo bradikardijo in srčnim blokom. pri bolnikih, ki prejemajo ta zdravila, se ne sme uvesti zdravljenja z zdravilom Gilenya (glejte tudi poglavje 4.5). Pri teh bolnikih je treba razmisliti o zdravljenju z zdravilom Gilenya le, če pričakovane koristi odtehtajo tveganje. Če upoštevate zdravljenje z zdravilom Gilenya, je priporočljivo, da se se je pred začetkom zdravljenja posvetoval o prehodu na druga zdravila, ki ne povzročajo znižanja srčnega utripa. zdravljenja. Priporočljivo je spremljanje vsaj do naslednjega jutra (glejte tudi poglavje 4.5).
Odvisno od trajanja prekinitve in trajanja zdravljenja (čas med začetkom zdravljenja in njegovo prekinitvijo) se lahko učinki na srčni utrip in atrioventrikularno prevodnost vrnejo ob ponovnem začetku zdravljenja z zdravilom Gilenya. Priporoča se enako spremljanje kot na začetku zdravljenja po prvem odmerku, če se zdravljenje prekine zaradi:
• 1 ali več dni v prvih dveh tednih zdravljenja
• več kot 7 dni v tretjem in četrtem tednu zdravljenja
• več kot 2 tedna po enem mesecu zdravljenja.
Če je prekinitev zdravljenja krajša od zgoraj opisane, je treba zdravljenje nadaljevati z dajanjem naslednjega odmerka, kot je bilo načrtovano.
Interval QT
V temeljiti študiji intervala QT, izvedeni z odmerki fingolimoda 1,25 mg ali 2,5 mg, v stanju dinamičnega ravnovesja (ko je bil še vedno prisoten negativen kronotropni učinek fingolimoda) je zdravljenje s fingolimodom povzročilo podaljšanje odmerka. Popravljen interval QT (QTc) s zgornja meja 90% intervala zaupanja ≤ 13,0 ms. Med fingolimodom in podaljšanjem intervala QTc niso opazili korelacije med odmerkom ali izpostavljenostjo in odzivom, niti kot absolutno vrednost niti kot spremembo od izhodišča.
Klinični pomen teh ugotovitev ni znan. V študijah pri bolnikih z multiplo sklerozo niso opazili klinično pomembnega podaljšanja intervala QT, vendar bolniki s tveganjem za podaljšanje intervala QT niso bili vključeni v klinična preskušanja.
Pri bolnikih s pomembnimi dejavniki tveganja, kot je hipokaliemija ali prirojeno podaljšanje intervala QT, se je treba izogibati zdravilom, ki lahko podaljšajo interval QTc.
Okužbe
Pomemben farmakodinamični učinek zdravila Gilenya je od odmerka odvisno zmanjšanje števila perifernih limfocitov na 20-30% izhodiščnih vrednosti. To je posledica reverzibilne sekvestracije limfocitov v limfoidnih tkivih (glejte poglavje 5.1).
Pred začetkom zdravljenja z zdravilom Gilenya bi morala biti na voljo nedavna popolna krvna slika (tj. Odvzeta v 6 mesecih pred ali po prekinitvi predhodnega zdravljenja). Med zdravljenjem je priporočljivo tudi redno ocenjevati krvno sliko po 3 mesecih in nato vsaj enkrat letno ter v primeru pojava znakov okužbe. Absolutno število limfocitov pod 0,2x109 / l, če je potrjeno, bi moralo prekiniti zdravljenje do se vrnejo v normalno stanje, saj so v kliničnih preskušanjih pri bolnikih z absolutnim številom limfocitov pod 0,2x109 / l prenehali uporabljati fingolimod.
Začetek zdravljenja z zdravilom Gilenya je treba pri bolnikih s hudimi okužbami, ki so v teku, odložiti do okrevanja.
Pred začetkom zdravljenja z zdravilom Gilenya je treba bolnike oceniti glede imunskega stanja pri noricah. Ker ni zgodovine noric, ki bi jo potrdil zdravnik, ali dokazov o celovitem cepljenju proti noricam, je priporočljivo, da bolnike pred začetkom zdravljenja z zdravilom Gilenya testiramo na protitelesa proti virusu noric (ZZV). Pri bolnikih z negativnim titrom protiteles se pred začetkom zdravljenja z zdravilom Gilenya priporoča celovito cepljenje proti noricam (glejte poglavje 4.8). Začetek zdravljenja z zdravilom Gilenya je treba odložiti za en mesec, da bo cepljenje popolnoma učinkovito.
Učinki zdravila Gilenya na imunski sistem lahko povečajo tveganje za okužbe (glejte poglavje 4.8). Pri bolnikih, zdravljenih z zdravilom Gilenya, ki imajo simptome okužbe, je treba uvesti učinkovite diagnostične in terapevtske strategije. Bolnike je treba poučiti, naj med zdravljenjem z zdravilom Gilenya poročajo o simptomih okužbe svojemu zdravniku.
Če se pri bolniku razvije huda okužba, je treba razmisliti o prekinitvi zdravljenja z zdravilom Gilenya in oceniti razmerje med koristmi in tveganji pred nadaljevanjem zdravljenja.
Izločanje fingolimoda po prekinitvi zdravljenja lahko traja do dva meseca, zato je treba v tem obdobju vztrajati pri nadzoru okužbe. Bolnikom je treba naročiti, naj v dveh mesecih po prenehanju zdravljenja z fingolimodom poročajo o simptomih okužbe.
Makularni edem
O makularnem edemu z motnjami vida ali brez njega so poročali pri 0,5% bolnikov, zdravljenih z 0,5 mg fingolimoda, predvsem v prvih 3-4 mesecih zdravljenja (glejte poglavje 4.8). Zato je priporočljivo oftalmološko oceno 3-4 mesece po začetku zdravljenja.Če bolniki kadar koli med zdravljenjem poročajo o motnjah vida, je treba opraviti pregled fundusa, vključno z makulo.
Bolniki z uveitisom v anamnezi in bolniki s sladkorno boleznijo imajo povečano tveganje za nastanek edema makule (glejte poglavje 4.8). Zdravila Gilenya niso preučevali pri bolnikih z multiplo sklerozo in sočasno sladkorno boleznijo. Bolnikom z multiplo sklerozo in sočasno sladkorno boleznijo ali uveitisom v anamnezi je priporočljivo, da pred začetkom zdravljenja opravijo oftalmološko preiskavo in kontrolne preglede med zdravljenjem.
Nadaljevanje zdravljenja z zdravilom Gilenya pri bolnikih z makularnim edemom ni bilo raziskano. Če se pri bolniku pojavi makularni edem, je priporočljivo prekiniti zdravljenje z zdravilom Gilenya. Pri odločanju, ali je treba zdravljenje z zdravilom Gilenya nadaljevati po okrevanju, je treba upoštevati možne koristi in tveganja za posameznega bolnika.
Funkcija jeter
Pri bolnikih z multiplo sklerozo, zdravljenih z zdravilom Gilenya, so poročali o zvišanju jetrnih encimov, zlasti alanin aminotransferaze (ALT), pa tudi gama glutamiltranspeptidaze (GGT) in aspartat transaminaze (AST). V kliničnih preskušanjih se je zvišanje ALT ≥ 3 -kratnik zgornje meje normalnega območja (ZMN) pojavilo pri 8,0% bolnikov, zdravljenih s 0,5 mg fingolimoda v primerjavi z 1,9% bolnikov, zdravljenih s placebom. se je pojavilo pri 1,8% bolnikov, zdravljenih s fingolimodom, in pri 0,9% bolnikov, zdravljenih s placebom.V kliničnih preskušanjih so zdravljenje s fingolimodom prekinili, če je bilo povečanje> 5 -kratnik zgornje meje normalnega območja. Pri nekaterih bolnikih, ki so bili po prekinitvi zdravljenja ponovno zdravljeni, se je ponovno pojavilo zvišanje vrednosti jetrnih transaminaz, kar je potrdilo povezavo med tem povečanjem in zdravilom. V kliničnih študijah so se povišane vrednosti jetrnih transaminaz pojavile kadar koli med zdravljenjem, čeprav se je večina pojavila v prvih 12 mesecih. Koncentracija transaminaz v krvi se je normalizirala približno 2 meseca po prekinitvi zdravljenja s fingolimodom.
Zdravila Gilenya niso preučevali pri bolnikih s predhodno hudo okvaro jeter (razred C po Child-Pughu), zato jih pri teh bolnikih ne smejo uporabljati (glejte poglavje 4.3).
Zaradi imunosupresivnih lastnosti fingolimoda je treba pri bolnikih z aktivnim virusnim hepatitisom odložiti začetek zdravljenja do prekinitve aktivne faze.
Pred začetkom zdravljenja z zdravilom Gilenya bi morale biti na voljo nedavne analize (tj. V preteklih 6 mesecih) ravni transaminaz in bilirubina. Če koncentracija jetrnih transaminaz doseže vrednosti, ki so več kot 5 -kratnik normalne meje (ZMN), je treba opraviti pogostejše preglede, vključno s preverjanjem serumskega bilirubina in alkalne fosfataze (ALP).Če po večkratnih pregledih vrednosti jetrnih transaminaz ostanejo več kot 5 -kratnik meje normale (ZMN), je treba zdravljenje z zdravilom Gilenya prekiniti in znova začeti šele, ko se vrednosti jetrnih transaminaz normalizirajo.
Pri bolnikih s simptomi jetrne disfunkcije, kot so nepojasnjena slabost, bruhanje, bolečine v trebuhu, utrujenost, anoreksija, zlatenica in / ali temen urin, je treba oceniti raven jetrnih encimov; če se potrdi pomembna poškodba jeter (npr. ravni jetrnih transaminaz, ki za več kot 5 -krat presegajo zgornjo mejo normalnega območja in / ali se zviša raven bilirubina v serumu), je treba zdravljenje z zdravilom Gilenya prekiniti. Nadaljevanje zdravljenja bo odvisno od tega, ali je ugotovljen drug vzrok za poškodbo jeter ali od tega, ali ima bolnik korist pri ponovnem začetku zdravljenja v primerjavi s tveganjem za ponovitev jetrne disfunkcije.
Čeprav ni podatkov, ki bi dokazovali, da imajo bolniki z že obstoječo boleznijo jeter povečano tveganje za povečanje testov delovanja jeter, je pri uporabi zdravila Gilenya pri bolnikih z anamnezo pomembne bolezni jeter potrebna previdnost.
Vpliv na serološke teste
Ker fingolimod zmanjšuje število limfocitov v krvi s prerazporeditvijo v sekundarne limfoidne organe, ga ni mogoče uporabiti za oceno stanja limfocitov pri bolniku, zdravljenem z zdravilom Gilenya. Laboratorijski testi, ki vključujejo uporabo mononuklearnih celic v obtoku, zahtevajo večji volumen krvi zaradi zmanjšanja števila limfocitov v obtoku.
Učinki na krvni tlak
Bolniki z nenadzorovano hipertenzijo so bili izključeni iz kliničnih preskušanj zdravila Gilenya pred trženjem; zato se posebna pozornost priporoča, če se bolniki z nenadzorovano hipertenzijo zdravijo z zdravilom Gilenya.
V kliničnih študijah pri bolnikih z multiplo sklerozo je bilo zdravljenje z 0,5 mg fingolimoda povezano s povprečnim povišanjem sistoličnega krvnega tlaka za približno 3 mmHg in diastoličnim krvnim tlakom za približno 1 mmHg: do teh povečanj je prišlo približno 1 mesec pozneje. V dvoletni s placebom kontrolirani študiji so o hipertenziji kot neželenem dogodku poročali pri 6,5% bolnikov, zdravljenih z 0,5 mg zdravila Gilenya, in pri 3,3% bolnikov, zdravljenih s placebom. Zato je treba med zdravljenjem z zdravilom Gilenya redno preverjati krvni tlak.
Učinki na dihalni sistem
Med zdravljenjem z zdravilom Gilenya so opazili rahlo od odmerka odvisno zmanjšanje volumna prisilnega izdiha (FEV1) in difuzne zmogljivosti ogljikovega monoksida (Dlco), zmanjšanja, ki so se pojavila v prvem mesecu in so med zdravljenjem ostala stabilna. Zdravilo Gilenya je treba uporabljati previdno pri bolnikih s hudimi dihalnimi motnjami, pljučno fibrozo in kronično obstruktivno pljučno boleznijo (glejte poglavje 4.8).
Sindrom zadnje reverzibilne encefalopatije
V redkih primerih sindroma posteriorne reverzibilne encefalopatije (PRES) so v kliničnih preskušanjih in po trženju poročali o odmerku 0,5 mg (glejte poglavje 4.8). Med poročanimi simptomi so bili nenaden pojav hudega glavobola, slabost, bruhanje, spremenjeno duševno stanje, vid motnje in epileptični napadi. Simptomi PRES so običajno reverzibilni, vendar lahko napredujejo v ishemično kap ali možgansko krvavitev. Zamuda pri diagnozi in zdravljenju lahko povzroči trajne nevrološke posledice. Če obstaja sum na prisotnost PRES, je treba zdravljenje z zdravilom Gilenya prekiniti.
Prejšnje zdravljenje z imunosupresivnimi ali imunomodulatornimi terapijami
Študije za oceno učinkovitosti in varnosti zdravila Gilenya pri prehodu s teriflunomida, dimetil fumarata ali alemtuzumaba na zdravilo Gilenya niso bile opravljene. Ko pacienti preidejo z drugega zdravljenja. spreminjanje bolezni v Gilenyi je treba upoštevati razpolovni čas in mehanizem delovanja druge terapije, da bi se izognili aditivnemu učinku na imunski sistem in hkrati zmanjšali tveganje ponovne aktivacije bolezni. popolno krvno sliko pred začetkom zdravljenja z zdravilom Gilenya, da zagotovite, da so učinki na imunski sistem, ki jih povzroča prejšnja terapija (npr. citopenija), izginili.
Na splošno se lahko zdravljenje z zdravilom Gilenya začne takoj po prekinitvi zdravljenja z interferonom ali glatiramer acetatom.
V primeru dimetil fumarata je obdobje izperi zadostovati mora za obnovitev ustrezne krvne slike pred začetkom zdravljenja z zdravilom Gilenya.
Zaradi dolge razpolovne dobe natalizumaba izločanje običajno traja do 2-3 mesece po prekinitvi zdravljenja. Teriflumonid se počasi izloča tudi iz plazme. Brez pospešenega postopka izločanja lahko izločanje teriflunomida iz plazme traja od nekaj mesecev do 2 let. Priporočljivo je izvesti pospešen postopek izločanja, kot je opisano v povzetku glavnih značilnosti zdravila za teriflunomid, ali pa obdobje izpiranja ne sme biti krajše od 3,5 mesecev. Pri prehodu z zdravljenja z natalizumabom ali teriflunomidom na zdravilo Gilenya je potrebna previdnost glede možnih sočasnih učinkov na imunski sistem.
Alemtuzumab ima močne in dolgotrajne imunosupresivne učinke. Ker resnično trajanje teh učinkov ni znano, je priporočljivo, da se z alemtuzumabom ne začne zdravljenje z zdravilom Gilenya, razen če koristi zdravljenja za posameznega bolnika očitno odtehtajo tveganje.
Odločitev o sočasni uporabi podaljšanega zdravljenja s kortikosteroidi je treba sprejeti po skrbnem premisleku.
Sočasna uporaba z močnimi induktorji CYP450
Fingolimod je treba uporabljati previdno v kombinaciji z močnimi induktorji CYP450. Priporočljivo je, da se šentjanževka ne daje sočasno (glejte poglavje 4.5).
Prekinitev terapije
Na podlagi razpolovne dobe zdravila je treba v primeru odločitve o prekinitvi zdravljenja z zdravilom Gilenya pustiti interval 6 tednov brez zdravljenja, da se fingolimod izloči iz krvi (glejte poglavje 5.2). se normalizira v 1-2 mesecih po prekinitvi zdravljenja (glejte poglavje 5.1). Začetek drugih terapij v tem časovnem intervalu povzroči sočasno izpostavljenost fingolimodu. Uporaba imunosupresivnih zdravil kmalu po prekinitvi zdravljenja z zdravilom Gilenya ima lahko dodaten učinek na imunski sistem, zato je priporočljiva previdnost.
04.5 Interakcije z drugimi zdravili in druge oblike interakcij
Antineoplastične, imunomodulatorne ali imunosupresivne terapije
Antineoplastičnih, imunomodulatornih ali imunosupresivnih terapij se ne sme uporabljati sočasno zaradi nevarnosti aditivnih učinkov na imunski sistem (glejte poglavji 4.3 in 4.4).
Prav tako je potrebna previdnost, ko bolniki po prekinitvi zdravljenja z dolgotrajnimi terapijami z učinki na imunski sistem, kot sta natalizumab ali mitoksantron (glejte poglavje 4.4), začnejo z zdravljenjem z zdravilom Gilenya (glejte poglavje 4.4). V kliničnih preskušanjih pri sklerozi. kortikosteroidov ni bila povezana s povečano stopnjo okužb.
Cepljenja
Cepljenja so lahko manj učinkovita med zdravljenjem in do dva meseca po prekinitvi zdravljenja z zdravilom Gilenya. Uporaba živih oslabljenih cepiv lahko predstavlja tveganje za okužbe, zato se jim je treba izogniti (glejte poglavji 4.4 in 4.8).
Snovi, ki povzročajo bradikardijo
Fingolimod so preučevali v kombinaciji z atenololom in diltiazemom. Pri dajanju fingolimoda in atenolola v študiji interakcij pri zdravih prostovoljcih je bilo ob začetku zdravljenja za 15% manj srčnega utripa; tega učinka pri diltiazemu niso opazili. Zaradi možnega aditivnega učinka. ne smejo začeti pri bolnikih, ki jemljejo zaviralce adrenergičnih receptorjev beta ali druga zdravila, ki lahko zmanjšajo srčni utrip, na primer antiaritmike razreda Ia in III, zaviralce kalcijevih kanalov (kot so ivabradin, verapamil ali diltiazem), digoksin, antiholinesteraze ali pilokarpin (glejte poglavji 4.4 in 4.8 Če pri teh bolnikih razmišljamo o zdravljenju z zdravilom Gilenya, se je treba posvetovati s kardiologom, ki bo razmislil o prehodu na druga zdravila, ki ne povzročajo zmanjšanja srčnega utripa, ali določil ustrezno spremljanje na začetku zdravljenja. Če zdravljenja z zdravili, ki znižujejo srčni utrip, ni mogoče prekiniti, je priporočljivo spremljanje vsaj do naslednjega jutra.
Spremembe farmakokinetike fingolimoda, ki jih povzročajo druge snovi
Fingolimod se presnavlja predvsem s CYP4F2. Pri njegovi presnovi so lahko vključeni tudi drugi encimi, kot je CYP3A4, zlasti v primeru močne indukcije CYP3A4. Pričakuje se, da močni zaviralci nosilnih beljakovin ne bodo vplivali na vedenje fingolimoda. Sočasna uporaba fingolimoda s ketokonazolom je povzročila 1,7-kratno povečanje izpostavljenosti (AUC) fingolimodu in fingolimod fosfatu z zaviranjem CYP4F2. Pri dajanju fingolimoda s snovmi, ki lahko zavirajo CYP3A4 (zaviralci proteaz, azolni protiglivičniki, nekateri makrolidi, kot sta klaritromicin ali telitromicin).
Sočasna uporaba 600 mg karbamazepina dvakrat na dan je dosegla stanje dinamičnega ravnovesja in enkratni odmerek 2 mg fingolimoda je zmanjšal AUC fingolimoda in njegovega presnovka za približno 40%. Drugi močni induktorji encima CYP3A4, kot so rifampicin, fenobarbital, fenitoin, efavirenz in šentjanževka, lahko povzročita zmanjšanje AUC fingolimoda in njegovega presnovka vsaj za to velikost. Ker bi to lahko ogrozilo njihovo učinkovitost, je pri kombinirani uporabi potrebna previdnost, vendar sočasna uporaba s šentjanževko ni priporočljiva (glejte poglavje 4.4).
Spremembe farmakologije drugih snovi, ki jih povzroča fingolimod
Ni verjetno, da bi fingolimod medsebojno deloval s snovmi, ki se presnavljajo predvsem z encimi CYP450 ali substrati glavnih nosilnih beljakovin.
Sočasna uporaba fingolimoda s ciklosporinom ni povzročila sprememb v izpostavljenosti ciklosporinu ali fingolimodu, zato se pričakuje, da fingolimod ne bo spremenil farmakokinetike zdravil, ki so substrati CYP3A4.
Sočasna uporaba fingolimoda s peroralnimi kontraceptivi (etinilestradiol in levonorgestrel) ni povzročila nobene spremembe v izpostavljenosti peroralnim kontraceptivom, izpostavljenosti tem zdravilom.
04.6 Nosečnost in dojenje
Ženske v rodni dobi / Kontracepcija pri ženskah
Pred začetkom zdravljenja z zdravilom Gilenya je treba ženske v rodni dobi obvestiti o možnih resnih tveganjih za plod in o potrebi po uporabi učinkovitih kontracepcijskih ukrepov med zdravljenjem z zdravilom Gilenya. Ker traja približno dva meseca po prekinitvi zdravljenja, da se fingolimod izloči iz telesa (glejte poglavje 4.4), obstaja potencialno tveganje za plod, zato je treba v tem času nadaljevati kontracepcijske ukrepe.
Nosečnost
Pred začetkom zdravljenja pri ženskah v rodni dobi mora biti na voljo negativen test nosečnosti. Ženske med zdravljenjem ne smejo zanositi, zato je priporočljiva učinkovita kontracepcija. Če ženska med jemanjem zdravila Gilenya zanosi, je priporočljivo prekiniti zdravljenje.
Študije na živalih so pokazale reproduktivno toksičnost, vključno z izgubo ploda in okvarami organov, zlasti obstojno okvaro arterijskega debla in prekata (glejte poglavje 5.3). Poleg tega je receptor, na katerega deluje fingolimod (sfingozin-1-fosfat), vključen v nastanek žil med embriogenezo. Podatkov o uporabi fingolimoda pri nosečnicah je zelo malo.
Ni podatkov o učinkih fingolimoda na porod in porod.
Čas hranjenja
Fingolimod se izloča v mleko doječih živali v koncentracijah, ki so 2-3 krat višje od koncentracij v plazmi matere (glejte poglavje 5.3). Zaradi možnosti resnih neželenih učinkov na fingolimod pri dojenčkih se ženske, ki se zdravijo z zdravilom Gilenya dojiti.
Plodnost
Podatki iz predkliničnih študij ne kažejo, da je fingolimod povezan s povečanim tveganjem za okvaro plodnosti (glejte poglavje 5.3).
04.7 Vpliv na sposobnost vožnje in upravljanja s stroji
Zdravilo Gilenya nima vpliva ali ima zanemarljiv vpliv na sposobnost vožnje in upravljanja s stroji.
Vendar se lahko ob začetku zdravljenja z zdravilom Gilenya včasih pojavi omotica ali zaspanost.
04.8 Neželeni učinki
Povzetek varnostnega profila
Varnostna populacija zdravila Gilenya izhaja iz dveh s placebom kontroliranih kliničnih preskušanj III. Faze in enega aktivno nadzorovanega kliničnega preskušanja III. Faze, izvedenega pri bolnikih z multiplo sklerozo, ki se ponavlja. Vključuje skupaj 2.431 bolnikov, zdravljenih z zdravilom Gilenya (0,5 ali 1,25 mg). V 2-letni s placebom kontrolirani klinični študiji D2301 (FREEDOMS) je bilo 854 bolnikov (placebo: 418 bolnikov) zdravljenih s fingolimodom. V 2-letni, s placebom kontrolirani študiji D2309 (FREEDOMS II) je bilo s fingolimodom zdravljenih 728 bolnikov z multiplo sklerozo (placebo: 355 bolnikov). Združeni rezultati teh dveh študij kažejo, da so bili najhujši neželeni učinki, ki so se pojavili pri uporabi zdravila Gilenya 0,5 mg, okužbe, makularni edem in prehodni atrioventrikularni blok na začetku zdravljenja. Najpogostejši neželeni učinki (incidenca ≥ 10%), ki so se pojavili pri uporabi zdravila Gilenya 0,5 mg so bile gripa, sinusitis, glavobol, driska, bolečine v hrbtu, povišani jetrni encimi in kašelj. Najpogostejši neželeni učinek pri uporabi zdravila Gilenya 0,5 mg, ki je povzročil "prekinitev zdravljenja", je bil zvišanje ravni ALT v krvi (2,2%). V enoletni študiji D2302 (TRANSFORMS), ki je vključevalo 849 bolnikov, zdravljenih s fingolimodom in ki so kot kontrolo uporabljali interferon beta-1α, so bili neželeni učinki na splošno podobni tistim v s placebom nadzorovanih študijah, ob upoštevanju različnega trajanja študije.
Spodaj so navedeni neželeni učinki, o katerih so poročali za 0,5 mg zdravila Gilenya v študijah D2301 (FREEDOMS) in D2309 (FREEDOMS II). Kategorije pogostnosti so opredeljene po naslednji konvenciji: zelo pogosto (≥ 1/10); pogosti (≥1 / 100,
Povzetek tabele neželenih učinkov
* Ne poroča v študijah FREEDOMS, FREEDOMS II in TRANSFORMS. Kategorizacija pogostnosti dogodkov je temeljila na ocenjeni "izpostavljenosti fingolimodu pri približno 10.000 bolnikih v vseh kliničnih preskušanjih".
Opis nekaterih posebnih neželenih učinkov
Okužbe
V kliničnih preskušanjih pri bolnikih z multiplo sklerozo je bila skupna stopnja okužb (65,1%), o katerih so poročali pri odmerku 0,5 mg, podobna tisti pri placebu. Vendar so bile pri bolnikih, zdravljenih z zdravilom Gilenya, pogostejše okužbe spodnjih dihal, predvsem bronhitis in v manjši meri herpetične okužbe in pljučnica.
Tudi pri odmerku 0,5 mg so poročali o nekaj primerih razširjene herpetične okužbe, vključno s smrtnimi primeri.
Makularni edem
V kliničnih študijah pri bolnikih z multiplo sklerozo se je makularni edem pojavil pri 0,5% bolnikov, zdravljenih s priporočenim odmerkom 0,5 mg, in pri 1,1% bolnikov, zdravljenih z višjim odmerkom (1,25 mg). Večina primerov se je pojavila v prvih 3-4 mesecih zdravljenja. Nekateri bolniki so poročali o zamegljenem vidu in zmanjšani ostrini vida; drugi so bili asimptomatski, diagnoza pa je bila postavljena med rutinskim oftalmološkim obiskom.Makularni edem se je na splošno izboljšal ali spontano izginil po prekinitvi zdravljenja z zdravilom Gilenya. Tveganja ponovitve po ponovni izpostavljenosti zdravljenju niso preučevali.
Incidenca makularnega edema je povečana pri bolnikih z multiplo sklerozo z anamnezo uveitisa (17% z anamnezo uveitisa v primerjavi z 0,6% brez anamneze uveitisa). Zdravila Gilenya niso preučevali pri bolnikih z multiplo sklerozo in sladkorno boleznijo. bolezni, povezane s povečanim tveganjem za nastanek makularnega edema (glejte poglavje 4.4) V kliničnih študijah pri bolnikih s presaditvijo ledvic, vključno s sladkorno boleznijo, je zdravljenje z 2,5 mg in 5 mg fingolimoda povzročilo dvakrat večjo incidenco makularnega edema.
Bradiaritmija
Začetek zdravljenja z zdravilom Gilenya povzroči prehodno znižanje srčnega utripa in je lahko povezan tudi z zamudo pri atrioventrikularni prevodnosti. V kliničnih preskušanjih pri bolnikih z multiplo sklerozo so največji upad srčnega utripa opazili v prvih 6 urah po operaciji. " uvedbo zdravljenja, pri čemer se je pogostost med zdravljenjem z zdravilom Gilenya 0,5 mg zmanjšala v povprečju za 12-13 utripov na minuto. Pri bolnikih, zdravljenih z 0,5 mg zdravila Gilenya, so redko opazili zmanjšanje srčnega utripa pod 40 utripov na minuto. Povprečni srčni utrip se je v enem mesecu po nadaljevanju zdravljenja vrnil na izhodiščno vrednost. Bradikardija je bila na splošno asimptomatska, vendar so nekateri bolniki imeli blage do zmerne simptome, vključno s hipotenzijo, omotico, utrujenostjo in / ali palpitacijami, ki so izzvenele v prvih 24 urah po začetku zdravljenja (glejte tudi poglavji 4.4 in 5.1.).
V kliničnih študijah pri bolnikih z multiplo sklerozo so atrioventrikularni blok prve stopnje (podaljšanje "PR-intervala na EKG") opazili pri 4,7% bolnikov, zdravljenih z 0,5 mg fingolimoda, pri 2,8% bolnikov, zdravljenih z intramuskularnim interferonom beta- 1α in pri 1,6% bolnikov, zdravljenih s placebom. O atrioventrikularnem bloku druge stopnje so poročali pri manj kot 0,2% bolnikov, zdravljenih z 0,5 mg zdravila Gilenya. V postmarketinških izkušnjah so v 6-urnem obdobju spremljanja po prvem odmerku zdravila Gilenya poročali o posameznih epizodah prehodnega, spontano razrešenega popolnega atrioventrikularnega bloka. ure pri začetku zdravljenja.Čeprav za večino bolnikov ni bil potreben zdravniški poseg, je en bolnik, zdravljen z zdravilom Gilenya 0, 5 mg, prejel izoprenalin po asimptomatskem atrioventrikularnem bloku druge stopnje Mobitz.
Po trženju so se v 24 urah po dajanju prvega odmerka pojavili osamljeni dogodki s poznim nastopom, vključno s prehodno asistolijo in nepojasnjeno smrtjo. Ocenjevanje teh primerov je zapleteno zaradi prisotnosti sočasnih zdravil in / ali že obstoječih stanj Korelacija teh dogodkov z Gilenyjo je negotova.
Krvni pritisk
V kliničnih študijah pri bolnikih z multiplo sklerozo je bilo zdravljenje z zdravilom Gilenya 0,5 mg povezano s povprečnim povišanjem sistoličnega krvnega tlaka za približno 3 mmHg in diastoličnim krvnim tlakom za približno 1 mmHg: do teh povečanj je prišlo približno 1 mesec pozneje. o hipertenziji so poročali pri 6,5% bolnikov, zdravljenih s 0,5 mg fingolimoda, in pri 3,3% bolnikov, zdravljenih s placebom. V prvem mesecu in na prvi dan zdravljenja (glejte tudi poglavje 4.4 Učinki na krvni tlak).
Funkcija jeter
Pri bolnikih z multiplo sklerozo, zdravljenih z zdravilom Gilenya, so poročali o zvišanju jetrnih encimov. V kliničnih študijah so pri 8,0% oziroma 1,8% bolnikov, zdravljenih z zdravilom Gilenya, opazili asimptomatsko povišanje ravni ALT v krvi ≥ 3-krat in ≥ 5-kratno zgornjo mejo normalnega območja (0,5 mg). zdravljenju po prekinitvi so se ponovno pojavile zvišanje vrednosti jetrnih transaminaz, kar je potrdilo povezavo med tem povečanjem in zdravilom. po prekinitvi zdravljenja z zdravilom Gilenya. Pri majhnem številu bolnikov (N = 10 pri odmerku 1,25 mg, N = 2 pri odmerku 0,5 mg), ki so doživeli povišanje ALT ≥ 5 -kratnik zgornje meje normalnega območja in so nadaljevali zdravljenje z zdravilom Gilenya, so bile vrednosti ALT se je normaliziralo v približno 5 mesecih (glejte tudi poglavje 4.4 Delovanje jeter).
Motnje živčnega sistema
V kliničnih študijah so bili redki dogodki, ki vključujejo živčni sistem, vključno z ishemično in hemoragično kapjo in atipičnimi nevrološkimi motnjami, kot so npr. Dogodki, podobni akutnemu diseminiranemu encefalomijelitisu (EAD).
Vaskularne patologije
Redki primeri periferne arterijske bolezni so se pojavili pri bolnikih, zdravljenih s fingolimodom v višjih odmerkih (1,25 mg).
Dihalni sistem
Med zdravljenjem z zdravilom Gilenya so opazili rahlo od odmerka odvisno zmanjšanje volumna prisilnega izdiha (FEV1) in difuzne zmogljivosti ogljikovega monoksida (Dlco), zmanjšanja, ki so se pojavila v prvem mesecu in so med zdravljenjem ostala stabilna. Pri 24. mesecu je bil odstotek znižanja predvidene FEV1 za predvideni FEV1 2,7% za 0,5 mg fingolimoda in 1,2% za placebo, razlika, ki je izginila po prekinitvi zdravljenja. za placebo.
Limfomi
Tako v kliničnih preskušanjih kot v obdobju trženja so poročali o primerih različnih vrst limfoma, vključno s smrtnim primerom pozitivnega B-celičnega limfoma virusa Epstein-Barr (EBV). Incidenca primerov limfoma (celice B in celice T) ) je bil v kliničnih študijah višji od pričakovanega v splošni populaciji.
Hemofagocitni sindrom
Poročali so o zelo redkih primerih hemofagocitnega sindroma (Hemofagocitni sindrom, HPS) s smrtnim izidom pri bolnikih, zdravljenih s fingolimodom v kontekstu "okužbe." HPS je redko stanje, ki je bilo opisano v povezavi z okužbami, imunosupresijo in različnimi avtoimunskimi boleznimi.
Poročanje o domnevnih neželenih učinkih
Poročanje o domnevnih neželenih učinkih, ki se pojavijo po odobritvi zdravila, je pomembno, saj omogoča stalno spremljanje razmerja med koristmi in tveganji zdravila. Zdravstvene delavce prosimo, da o vsakem sumu na neželene učinke poročajo prek nacionalnega sistema za poročanje. V "Prilogi V .
04.9 Preveliko odmerjanje
Pri zdravih prostovoljcih so enkratni odmerki do 80 -kratni priporočeni odmerek (0,5 mg) dobro prenašali. Pri odmerku 40 mg je 5 od 6 preiskovancev poročalo o šibki stiski v prsih ali omedlevici, klinično povezani z reaktivnostjo dihalnih poti.
Fingolimod lahko povzroči bradikardijo na začetku zdravljenja, zmanjšanje srčnega utripa pa se običajno pojavi v eni uri po prvem odmerku in je največ v prvih 6 urah. Negativni kronotropni učinek zdravila Gilenya traja več kot 6 ur in postopoma izzveni v naslednjih dneh zdravljenja (za več podrobnosti glejte poglavje 4.4). Poročali so o upočasnitvi atrioventrikularne prevodnosti, posamezna poročila o atrioventrikularni blokadi. Popolna, prehodna in spontana razrešitev (glejte poglavji 4.4 in 4.8).
Če preveliko odmerjanje sovpada s prvo izpostavljenostjo zdravilu Gilenya, je pomembno, da bolnika neprekinjeno (v realnem času) spremljamo z elektrokardiografijo z urnim merjenjem srčnega utripa in krvnega tlaka, vsaj v prvih 6 urah (glejte poglavje 4.4).
Potrebno je tudi dodatno spremljanje (vsaj do naslednjega jutra in v vsakem primeru do odprave simptomov), če je po 6 urah po prvem odmerku srčni utrip
Fingolimoda se ne odstrani niti z dializo niti s plazmaferezo.
05.0 FARMAKOLOŠKE LASTNOSTI
05.1 Farmakodinamične lastnosti
Farmakoterapevtska skupina: selektivni imunosupresivi.
Oznaka ATC: L04AA27.
Mehanizem delovanja
Fingolimod je modulator receptorja sfingozin-1-fosfata (S1P).S pomočjo sfingosin kinaze se fingolimod pretvori v aktivni presnovek fingolimod fosfat, ki se pri nizkih nanomolarnih koncentracijah veže na receptor S1P1, ki se nahaja na površini limfocitov, in zlahka prečka krvno-možgansko pregrado, da se veže na receptor v osrednjem živcu. sistem S1P1, nameščen na celicah centralnega živčnega sistema. Fingolimod fosfat, ki deluje kot funkcionalni antagonist receptorjev S1P, izraženih na limfocitih, zavira sposobnost limfocitov pobegniti iz bezgavk, kar povzroči prerazporeditev in ne uničenje limfocitov. Ta prerazporeditev zmanjša infiltracijo patogenih limfocitov v centralni živčni sistem, kjer sodelujejo pri vnetju živcev in poškodbah tkiva. Študije in poskusi na živalih in vitro kažejo, da lahko fingolimod deluje tudi z interakcijo z receptorji S1P, izraženimi na celicah centralnega živčnega sistema.
Farmakodinamični učinki
V 4-6 urah po prvi uporabi 0,5 mg fingolimoda se število limfocitov v periferni krvi zmanjša na približno 75% izhodiščne vrednosti. Z vsakodnevnim dajanjem se število limfocitov še naprej zmanjšuje dva tedna in doseže minimalno vrednost približno 500 celic / mikroliter ali približno 30% izhodiščne vrednosti. 18% bolnikov je vsaj enkrat doseglo minimalno vrednost pod 200 celic / mikroliter. S stalnim dnevnim zdravljenjem ostaja število limfocitov nizko. Večina limfocitov T in B se redno seli skozi limfoidne organe: fingolimod deluje predvsem na te celice. Približno 15-20% limfocitov T ima fenotip TEM (efektor spomina): te celice so pomembne za periferni imunski nadzor. Ker se ta vrsta limfocitov praviloma ne seli v limfoidne organe, fingolimod na te celice ne deluje. Povečanje števila perifernih limfocitov je očitno v dneh po prekinitvi zdravljenja s fingolimodom; število limfocitov se običajno normalizira v enem do dveh mesecih. Kronična uporaba fingolimoda povzroči rahlo zmanjšanje števila nevtrofilcev za približno 80% izhodiščne vrednosti.Fingolimod ne deluje na monocite.
Fingolimod povzroči prehodno zmanjšanje srčnega utripa in zmanjšano atrioventrikularno prevodnost ob začetku zdravljenja (glejte poglavji 4.4. In 4.8). Največje zmanjšanje srčnega utripa opazimo v 6 urah po dajanju s 70% negativnim kronotropnim učinkom. Z naslednjimi odmerki se srčni utrip v enem mesecu vrne na izhodiščno vrednost. Zmanjšanje srčnega utripa, ki ga povzroči fingolimod, je mogoče odpraviti s parenteralno uporabo atropina ali izoprenalina. Dokazano je tudi, da ima inhalacijski salmeterol skromen pozitiven kronotropni učinek. Na začetku zdravljenja s fingolimodom se povečuje število prezgodnjih atrijskih kontrakcij, vendar ni povečane stopnje atrijske fibrilacije / trepetanja ali ventrikularnih aritmij ali ektopije. Zdravljenje s fingolimodom ne povzroči zmanjšanja srčnega utripa in ne vpliva na simpatikomimetične odzive srca, vključno z dnevnimi spremembami srčnega utripa in odzivom na napor.
Zdravljenje s fingolimodom, enkratnimi ali ponavljajočimi se odmerki po 0,5 mg in 1,25 mg dva tedna, ne povzroči občutnega povečanja upora dihalnih poti, izmerjenega kot FEV1 in s prisilnim izdihavalnim tokom (FEF) 25-75. Vendar se pri enkratnih odmerkih fingolimoda ≥ 5 mg (10-kratnik priporočenega odmerka) pojavi od odmerka odvisno odpornost dihalnih poti. Zdravljenje s ponavljajočimi se odmerki fingolimoda 0,5 mg, 1,25 mg ali 5 mg ne vodi do motene oksigenacije ali desaturacije kisika pri vadbi ali povečanja odziva dihalnih poti na metaholin.
Klinična učinkovitost in varnost
Učinkovitost zdravila Gilenya je bila dokazana v dveh študijah, ki so ocenjevale dajanje fingolimoda 0,5 mg in 1,25 mg enkrat na dan pri bolnikih z recidivno remitentno multiplo sklerozo. ≥1 ponovitev v preteklem letu. Ocena razširjene lestvice invalidnosti (EDSS) je bila 0-5,5. Tretja študija, izvedena pri isti populaciji bolnikov, je bila zaključena po registraciji Gilenye.
V 2-letno, randomizirano dvojno slepo, s placebom nadzorovano študijo D2301 (FREEDOMS) je bilo vključenih 1272 bolnikov (n = 425, zdravljenih z 0,5 mg fingolimoda, 429 s 1,25 mg fingolimoda, 418 s placebom). Srednje vrednosti izhodiščnih značilnosti so bile: starost 37 let, trajanje bolezni 6,7 leta, ocena EDSS 2,0. Rezultati so predstavljeni v tabeli 1. Med vsemi odmerki 0,5 mg in 1,25 mg ni bilo pomembnih razlik.
Tabela 1: Študija D2301 (PROSTOSTI): Glavni rezultati
† Napredovanje invalidnosti, opredeljeno kot povečanje EDSS za eno točko, potrjeno po treh mesecih
** str
Z analizo so bile ocenjene vse klinične točke namen zdravljenja. Analize v zvezi s podatki MRI so uporabile ocenljive nabore podatkov.
Bolniki, ki so zaključili fazo jedro 24-mesečne študije FREEDOMS so lahko vstopili v fazo podaljšanja za slepo odmerjanje (D2301E1) in prejeli fingolimod. Skupaj je vstopilo 920 bolnikov (n = 331 je nadaljevalo z odmerkom 0,5 mg, 289 z odmerkom 1,25 mg, 155 je prešlo s placeba na 0,5 mg in 145 s placeba na 1,25 mg). Po 12 mesecih (36. mesec) je bilo še vedno vključenih 856 bolnikov (93%). Med 24. in 36. mesecem je letna stopnja recidivov (ARR) pri bolnikih, ki so prejemali 0,5 mg fingolimoda v fazi jedro študije, ki je nadaljevala z istim odmerkom (0,5 mg), je bila 0,17 (0,21 v fazi jedro študija). Letna stopnja recidivov pri bolnikih, ki so prešli s placeba na fingolimod 0,5 mg, je bila 0,22 (0,42 v fazi jedro študija).
Podobne rezultate smo dobili v 2-letni, randomizirani, dvojno slepi, s placebom kontrolirani študiji faze III (D2309; FREEDOMS 2), izvedeni pri 1 083 bolnikih z recidivno remitentno multiplo sklerozo (n = 358, zdravljenih s fingolimodom 0,5 mg , 370 s fingolimodom 1,25 mg, 355 s placebom). Srednje vrednosti izhodiščnih značilnosti so bile: starost 41 let, trajanje bolezni 8,9 leta, ocena EDSS 2,5.
Tabela 2: Študija D2309 (FREEDOMS 2): Glavni rezultati
† Napredovanje invalidnosti, opredeljeno kot povečanje EDSS za eno točko, potrjeno po treh mesecih
** str
Z analizo so bile ocenjene vse klinične točke namen zdravljenja. Analize v zvezi s podatki MRI so uporabile ocenljive nabore podatkov.
V študiji D2302 (TRANSFORMI), faza III, ki traja 1 leto, je bila randomizirana, dvojno slepa, kontrolirana in dvojna lutka v primerjavi z aktivnim zdravilom (interferon beta-1α) je bilo vključenih 1280 bolnikov (n = 429, zdravljenih z 0,5 mg fingolimoda, 4,25 s fingolimodom 1,25 mg, 431 z intramuskularno injekcijo interferona beta-1α v odmerku 30 mikrogramov enkrat na teden). Srednje vrednosti izhodiščnih značilnosti so bile: starost 36 let, trajanje bolezni 5,9 leta, ocena EDSS 2,0. Rezultati študije so predstavljeni v tabeli 3. Med odmerki 0,5 mg in 1,25 mg glede na končne točke študije ni bilo pomembne razlike.
Tabela 3: Študija D2302 (TRANSFORME): Glavni rezultati
† Napredovanje invalidnosti, opredeljeno kot povečanje EDSS za eno točko, potrjeno po treh mesecih
** str
Z analizo so bile ocenjene vse klinične točke namen zdravljenja. Analize v zvezi s podatki MRI so uporabile ocenljive nabore podatkov.
Bolniki, ki so zaključili fazo jedro 12-mesečne študije TRANSFORMS so lahko vstopili v fazo podaljšanja slepo za odmerjanje (D2302E1) in prejeli fingolimod. Vstopilo je skupaj 1030 bolnikov, vendar 3 od teh niso prejeli zdravljenja (n = 356 se je nadaljevalo pri odmerku 0,5 mg, 330 pri odmerku 1,25 mg, 167 je prešlo z interferona beta-1α na 0,5 mg in 174 z interferonom beta -1α pri 1,25 mg). Po 12 mesecih (24. mesec) je bilo še vedno vključenih 882 bolnikov (86%). Med 12. in 24. mesecem je letna stopnja recidivov (ARR) pri bolnikih, ki so prejemali 0,5 mg fingolimoda v fazi jedro študije, ki je nadaljevala z istim odmerkom (0,5 mg), je bila 0,20 (0,19 v fazi jedro študija). Letna stopnja recidivov pri bolnikih, ki so prešli z interferona beta-1α na fingolimod 0,5 mg, je bila 0,33 (0,48 v fazi jedro študija).
Zbrani rezultati študij D2301 in D2302 so pokazali dosledno in statistično pomembno zmanjšanje glede na nadzor letne stopnje recidivov v podskupinah, opredeljenih glede na spol, starost, predhodno zdravljenje MS, aktivnost bolezni ali invalidnost na začetku.
Nadaljnja analiza rezultatov kliničnih preskušanj kaže pomembne učinke zdravljenja na podskupine bolnikov z visoko aktivno multiplo sklerozo, ki se vrača.
Evropska agencija za zdravila je odložila obveznost predložitve rezultatov študij z zdravilom Gilenya pri eni ali več podskupinah pediatrične populacije z multiplo sklerozo (za informacije o pediatrični uporabi glejte poglavje 4.2).
05.2 "Farmakokinetične lastnosti
Farmakokinetični podatki so bili pridobljeni pri zdravih prostovoljcih, bolnikih s presaditvijo ledvic in bolnikih z multiplo sklerozo.
Farmakološko aktivni presnovek, odgovoren za učinkovitost, je fingolimod fosfat.
Absorpcija
Absorpcija fingolimoda poteka počasi (Tmax 12-16 ur) in je obsežna (≥85%). Navidezna absolutna biološka uporabnost po peroralni uporabi je 93%(interval zaupanja: 79-111%). stanje dinamičnega ravnovesja koncentracije se dosežejo v 1-2 mesecih po uporabi enkratnih dnevnih odmerkov fingolimoda in alo stanje dinamičnega ravnovesja so približno 10 -krat višji od tistih, ki so jih opazili pri začetnem odmerku.
Vnos hrane ne spremeni vrednosti najvišje koncentracije (Cmax) ali sistemske izpostavljenosti (AUC) fingolimoda. Cmax fingolimod fosfata se je rahlo povečal za 34%, medtem ko je bila AUC nespremenjena, zato lahko zdravilo Gilenya jemljete na poln ali prazen želodec (glejte poglavje 4.2).
Distribucija
Fingolimod se hitro porazdeli v rdečih krvnih celicah in je prisoten v 86% krvnih celic. Fingolimod fosfat ima 17% manjšo porazdelitev rdečih krvnih celic. Vezava fingolimoda in fingolimod fosfata na plazemske beljakovine je visoka (> 99%).
Fingolimod je obsežno porazdeljen v tkivih s porazdeljenim volumnom približno 1.200 ± 260 litrov.
Biotransformacija
Pri ljudeh se fingolimod presnavlja z reverzibilno stereoselektivno fosforilacijo s tvorbo farmakološko aktivnega (S) -enantiomera fingolimod fosfata. Fingolimod se izloči z oksidativno biotransformacijo, ki jo katalizirajo predvsem CYP4F2 in po možnosti drugi izoencimi, in poznejša razgradnja v neaktivne presnovke, podobne tistim pri maščobnih kislinah. Opazili so tudi tvorbo farmakološko neaktivnih nepolarnih ceramidnih analogov fingolimoda. Glavni encim, vključen v presnovo fingolimoda, je delno identificiran in je lahko CYP4F2 ali CYP3A4.
Po enkratnem peroralnem dajanju fingolimoda [14C] so glavne sestavine, povezane s fingolimodom, odkrite v krvi s prispevkom k AUC do 34 dni po dajanju celotnih radioaktivno označenih komponent, fingolimod sam (23%), fingolimod fosfat ( 10%) in nekateri neaktivni presnovki (presnovek karboksilne kisline M3 (8%), metabolit ceramida M29 (9%) in metabolit ceramida M30 (7%)).
Odprava
Krvni očistek fingolimoda je 6,3 ± 2,3 L / h, povprečni končni razpolovni čas izločanja (t1 / 2) pa je 6-9 dni. Ravni fingolimoda in fingolimod fosfata v krvi se v končni fazi vzporedno zmanjšujejo, kar ima za posledico podobno polovico -živi za obe molekuli.
Po peroralnem dajanju se približno 81 % odmerka počasi izloči z urinom v obliki neaktivnih presnovkov.Fingolimod in fingolimod fosfat se v urinu ne izločijo nespremenjeni, ampak sta prisotni kot glavni sestavini v blatu, pri čemer vsaka količina predstavlja manj kot 2,5 % odmerka Po 34 dneh je okrevanje uporabljenega odmerka 89%.
Linearnost
Koncentracije fingolimodnega in fingolimod fosfata se po večkratnem dajanju enkratnih dnevnih odmerkov 0,5 mg ali 1,25 mg navidezno sorazmerno povečajo.
Značilnosti pri določenih populacijah
Farmakokinetika fingolimodnega in fingolimod fosfata se ne razlikuje med moškimi in ženskami, pri bolnikih različnega etničnega izvora ali pri bolnikih z blago do hudo okvaro ledvic.
Pri osebah z blago, zmerno ali hudo okvaro jeter (razredi A, B in C po Child-Pughu) niso opazili spremembe Cmax fingolimoda, medtem ko se je AUC fingolimoda povečala za 12%, 44%in 103%. Pri bolnikih s hudo okvaro jeter ( Child-Pugh razred C), Cmax fingolimod fosfata se je zmanjšal za 22% in AUC se ni bistveno spremenila. Farmakokinetika fingolimod fosfata pri bolnikih z blago do zmerno okvaro jeter ni bila ocenjena. Navidezni razpolovni čas izločanja fingolimoda je bil pri osebah z blago okvaro jeter nespremenjen, pri bolnikih z zmerno ali hudo okvaro jeter pa se je povečal za približno 50%.
Fingolimoda se ne sme uporabljati pri bolnikih s hudo okvaro jeter (razred C po Child-Pughovem razredu) (glejte poglavje 4.3). Pri bolnikih z blago in zmerno okvaro jeter je treba zdravljenje s fingolimodom začeti previdno (glejte poglavje 4.2).
Klinične izkušnje in farmakokinetični podatki pri bolnikih, starejših od 65 let, so omejeni, pri bolnikih, starih 65 let in več, je treba zdravilo Gilenya uporabljati previdno (glejte poglavje 4.2).
Pediatrična populacija
Podatki iz študije o presaditvi ledvice, ki vključuje 7 otrok, starejših od 11 let, so omejeni (študija FTY720A0115). Primerjava teh podatkov s tistimi pri zdravih odraslih prostovoljcih je malo pomembna in o farmakokinetičnih lastnostih fingolimoda pri otrocih ni mogoče sklepati.
05.3 Predklinični podatki o varnosti
Predklinični varnostni profil fingolimoda so ovrednotili pri miših, podganah, psih in opicah. Glavni ciljni organi so bili limfoidni sistem (limfopenija in limfoidna atrofija), pljuča (povečanje telesne mase, hipertrofija gladkih mišic na bronhioloalveolarnem stičišču) in pri različnih vrstah srce (negativen kronotropni učinek, povišan krvni tlak, perivaskularne spremembe in miokardni degeneracija); v 2-letni študiji je bil fingolimod na krvnih žilah (vaskulopatija) aktiven le pri podganah v odmerkih 0,15 mg / kg in več, kar je približno 4-krat večja od sistemske izpostavljenosti pri človeku (AUC) pri dnevnem odmerku 0, 5 mg.
V 2-letni študiji pri podganah s peroralnimi odmerki fingolimoda do največjega dovoljenega odmerka 2,5 mg / kg niso opazili nobenih dokazov o rakotvornosti, kar je približno 50-kratna sistemska izpostavljenost pri človeku (AUC) pri odmerku 0,5 mg.V dvoletni študiji na miših pa so pri odmerkih 0,25 mg / kg in več opazili večjo incidenco malignega limfoma, kar je približno 6-krat večja od izpostavljenosti ljudi sistemski (AUC) pri dnevnem odmerku 0,5 mg.
V študijah na živalih ni bilo ugotovljeno, da bi bil fingolimod mutagen ali klastogen.
Fingolimod ni vplival na število / gibljivost semenčic ali plodnost samcev in samic podgan do največjega preizkušenega odmerka (10 mg / kg), kar predstavlja približno 150 -kratno mejo sistemske izpostavljenosti pri človeku (AUC) pri dnevnem odmerku 0,5 mg.
Pokazalo se je, da je fingolimod pri podganah teratogen, če ga jemljemo v odmerkih 0,1 mg / kg ali več. Najpogostejše plodne visceralne malformacije vključujejo trajno okvaro arterijskega debla in ventrikularnega septuma.Teratogenega potenciala pri kuncih ni mogoče v celoti oceniti, vendar so pri odmerkih 1,5 mg / kg in več opazili povečano smrtnost zarodkov in plodov, pri odmerkih 5 mg / kg pa zmanjšali sposobnost preživetja plodov in upočasnilo rast ploda.
Pri podganah se je preživetje mladičev F1 generacije v zgodnjem obdobju po porodu zmanjšalo v odmerkih, ki niso povzročali strupenosti za mater. Vendar pa zdravljenje s fingolimodom na generacijo F1 ni vplivalo na telesno težo, razvoj, vedenje in plodnost.
Fingolimod se je izločal v mleko zdravljenih doječih živali, pri brejih kuncih pa je prešel placentno pregrado.
Ocena okoljskega tveganja (Ocena okoljskega tveganja, WAS)
Pri uporabi zdravila Gilenya pri bolnikih z recidivno multiplo sklerozo ni pričakovati nobenega okoljskega tveganja.
06.0 FARMACEVTSKE INFORMACIJE
06.1 Pomožne snovi
Vsebina kapsule:
Magnezijev stearat
Manitol
Lupina kapsule:
Rumeni železov oksid (E172)
Titanov dioksid (E171)
Žele
Črnilo:
Lak (E904)
Dehidriran alkohol
Izopropilni alkohol
Butilni alkohol
Propilen glikol
Očiščena voda
Koncentrirana raztopina amoniaka
Kalijev hidroksid
Črni železov oksid (E172)
Rumeni železov oksid (E172)
Titanov dioksid (E171)
Dimetikon
06.2 Nezdružljivost
Ni pomembno.
06.3 Obdobje veljavnosti
2 leti.
06.4 Posebna navodila za shranjevanje
Shranjujte pri temperaturi do 25 ° C.
Shranjujte v originalni ovojnini za zaščito zdravila pred vlago.
06.5 Vrsta ovojnine in vsebina pakiranja
Pakiranja s 7, 28 ali 98 trdimi kapsulami ali več pakiranji, ki vsebujejo 84 (3 pakiranja po 28) v pretisnih omotih iz PVC / PVDC / aluminija.
Pakiranja, ki vsebujejo 7 x 1 trde kapsule v perforiranih pretisnih omotih za eno dozo iz PVC / PVDC / aluminija.
Na trgu ni vseh navedenih pakiranj.
06.6 Navodila za uporabo in rokovanje
Brez posebnih navodil.
07.0 IMETNIK DOVOLJENJA ZA PROMET
Novartis Europharm Limited
Wimblehurst Road
Horsham
Zahodni Sussex, RH12 5AB
UK
08.0 ŠTEVILKA DOVOLJENJA ZA PROMET
EU / 1/11/677 / 001-006
040949012
040949024
040949036
040949048
040949051
09.0 DATUM PRVEGA DOVOLJENJA ALI PODALJŠANJA DOVOLJENJA
17.03.2011
10.0 DATUM REVIZIJE BESEDILA
Junija 2014