Če bi govorili o dvajsetih aminokislinah, ki sestavljajo proteinske strukture in modificirane, bi bilo treba opisati vsaj dvanajst specializiranih presnovnih poti.
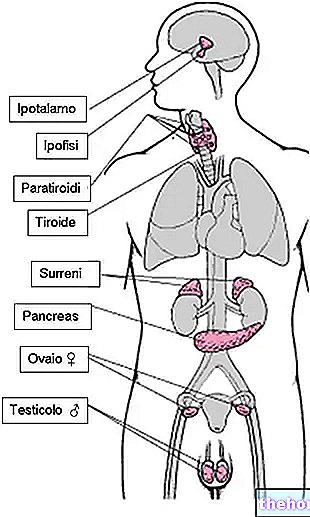
Toda zakaj celice uporabljajo toliko presnovnih poti, ki zahtevajo energijo (na primer za regeneracijo katalitičnih mest encimov), vsaka z encimsko dediščino, za katabolizacijo aminokislin? Skoraj iz vseh aminokislin je mogoče s pomočjo specializiranih poti pridobiti presnovke, ki se v manjši meri uporabljajo za proizvodnjo energije (na primer z glukoneogenezo in potjo ketonskih teles), predvsem pa vodijo v nastanek kompleksnih molekule z velikim številom ogljikovih atomov (na primer iz fenilalanina in tirozina se v nadledvičnih žlezah proizvajajo hormoni, ki so za to specializirani); če bi bilo po eni strani enostavno proizvajati energijo iz aminokislin, bi bilo po drugi strani zapleteno graditi kompleksne molekule, ki se začnejo iz majhnih molekul: katabolizem aminokislin jim omogoča, da izkoristijo svoje okostje, da pridobijo večje vrste.
Zdrava oseba dnevno razgradi dva ali tri hektograme aminokislin: 60-100 g jih izvira iz beljakovin, vnesenih s prehrano, več kot 2 hektograma pa iz normalnega prometa beljakovin, ki so sestavni del organizma ( aminokisline teh beljakovin, ki so poškodovane s redoks procesi, se nadomestijo z drugimi in katabolizirajo).
Aminokisline dajejo energijski prispevek v smislu ATP: po odstranitvi α-amino skupine lahko preostali ogljikov ogrodje aminokislin po ustreznih transformacijah vstopi v Krebsov cikel. Poleg tega, ko primanjkuje hranil in se količina glukoze zmanjša, se aktivira glukoneogeneza: glukoneogenetske aminokisline naj bi bile tiste, ki jih je po ustreznih spremembah mogoče vnesti v glukoneogenezo; glukoneogenetske aminokisline so tiste, ki jih je mogoče pretvoriti v piruvat ali v fumarat (fumarat se lahko pretvori v malat, ki zapusti mitohondrij in se v citoplazmi pretvori v oksaloacetat, iz katerega je mogoče pridobiti fosfoenol piruvat). kis-acetat.
Ta, ki je bil pravkar opisan, je zelo pomemben vidik, saj lahko aminokisline v primeru takojšnjega postenja odpravijo pomanjkanje sladkorja; če se post ohrani, se po dveh dneh vmeša presnova lipidov (ker beljakovinskih struktur ni mogoče preveč napadati), se v tej fazi, ker je glukoneogeneza zelo omejena, maščobne kisline pretvorijo v acetil koencim A in ketonska telesa. Od nadaljnjega posta se možgani prilagodijo tudi uporabi ketonskih teles.
Prenos α-amino skupine iz aminokislin poteka s transaminacijsko reakcijo; pravijo, da encimi, ki katalizirajo to reakcijo, transaminaze (ali amino transferaza). Ti encimi uporabljajo encimski kofaktor, imenovan piridoksal fosfat, ki posreduje s svojo aldehidno skupino. Piridoksal fosfat je produkt fosforilacije piridoksina, ki je vitamin (B6), ki ga najdemo predvsem v zelenjavi.
Transaminaze imajo naslednje lastnosti:
Visoka specifičnost za par ketoglutarat-glutamat α;
Ime sta dobila po drugem paru.
Encimi transaminaze vedno vključujejo par α-ketoglutarat-glutamat in se razlikujejo glede na drugi par.
Primeri:
L "aspartatne transaminaze tj. GOT (glutamat-osal acetatna transaminaza): encim prenese a-amino skupino iz aspartata v α-ketoglutarat, pri čemer pridobi oksaloacetat in glutamat.
L "alanin transaminaza tj. GTP (glutamat-piruvat transaminaza): encim prenese a-amino skupino iz "alanina v" α-ketoglutarat, pri čemer pridobi piruvat in glutamat.
Različne transaminaze uporabljajo α-ketoglurat kot akceptor aminokisline aminokislin in jo pretvorijo v glutamat; nastale aminokisline pa se uporabljajo na poti ketonskih teles.
Ta vrsta reakcije se lahko zgodi v obeh smereh, saj se prekinejo in tvorijo vezi z enako energijsko vsebnostjo.
Transaminaze so tako v citoplazmi kot v mitohondriji (večinoma so aktivne v citoplazmi) in se razlikujejo po svoji izoelektrični točki.
Transaminaze lahko tudi dekarboksilirajo aminokisline.
Moral bo obstajati način za pretvorbo glutamata nazaj v α-ketoglutarat: to se naredi z deaminacijo.
Tam glutamat dehidrogenaza je encim, ki lahko pretvori glutamat v α-ketoglutarat in zato pretvori aminokisline aminokislin v obliki glutamata v amoniak. Dogaja se redoks proces, ki poteka skozi vmesni α-amino glutarat: amoniak in α-ketoglutarat se sprostita in se vrneta v obtok.
Nato odlaganje aminokislin aminokislin poteka skozi transaminaze (ki se razlikujejo glede na substrat) in glutamat dehidrogenazo, ki določa nastanek amoniaka.
Obstajata dve vrsti glutamat dehidrogenaze: citoplazmatska in mitohondrijska; kofaktor, ki je tudi kosubstrat tega encima, je NAD (P) +: glutamat dehidrogenaza uporablja NAD + ali NADP + kot akceptor reducirajoče moči. Citoplazmatska oblika raje, čeprav ne izključno, NADP +, medtem ko mitohondrijska oblika raje NAD +. Namen mitohondrijske oblike je odstraniti amino skupine: vodi v nastanek amoniaka (ki je substrat za specializiran encim v mitohondriji) in NADH (ki se pošlje v dihalno verigo). Citoplazmatska oblika deluje v nasprotni smeri, to je, da uporablja amoniak in α-ketoglutarat za dajanje glutamata (ki ima biosintetsko destinacijo): ta reakcija je redukcijska biosinteza in uporabljeni kofaktor je NADPH.
Glutamat dehidrogenaza deluje, kadar je treba odstraniti aminokisline aminokislin, kot je amoniak (z urinom), ali ko so ogrodja aminokislin potrebna za proizvodnjo energije: ta encim bo imel zato kot negativne modulatorje sisteme, ki so indikacija dobre razpoložljivosti energije (ATP, GTP in NAD (P) H) in kot pozitivni modulatorji sistemi, ki kažejo na potrebo po energiji (AMP, ADP, GDP, NAD (P) +, aminokisline in ščitnični hormoni).
Aminokisline (predvsem levcin) so pozitivni modulatorji glutamat dehidrogenaze: če so aminokisline prisotne v citoplazmi, jih lahko uporabimo za sintezo beljakovin ali pa jih je treba odstraniti, ker jih ni mogoče kopičiti (to pojasnjuje, zakaj so aminokisline pozitivni modulatorji) ).
Odstranjevanje amoniaka: cikel sečnine
Ribe odstranijo amoniak z vnosom v vodo skozi škrge; ptice ga pretvorijo v sečno kislino (ki je kondenzacijski produkt) in jo izločijo z blatom. Poglejmo, kaj se dogaja pri ljudeh: rekli smo, da glutamat dehidrogenaza pretvori glutamat v α- ketoglutarat in amoniak, vendar nismo rekli, da se to pojavlja le v mitohondrijih jeter.
Temeljno vlogo odstranjevanja amoniaka skozi cikel sečnine igrajo mitohondrijske transaminaze.

Ogljikov dioksid v obliki bikarbonatnega iona (HCO3-) se aktivira s kofaktorjem biotina, ki tvori karboksi biotin, ki reagira z amoniakom, da nastane karbaminska kislina; naslednja reakcija uporablja ATP za prenos fosfata na karbaminsko kislino, ki tvori karbamil fosfat in ADP (pretvorba ATP v ADP je gonilna sila za pridobivanje karboksibiotina.) To fazo katalizira karbamil fosfat sintetaza in se pojavlja v mitohondriji. Karbamil fosfat in ornitin sta substrata za encim ornitin trans karbamilaza ki jih pretvori v citrulin; ta reakcija se pojavi v mitohondrijih (hepatocitih). Proizveden citrulin zapusti mitohondrij in v citoplazmi preide pod "delovanje"arginin sukcinat sintetaza: obstaja fuzija med ogljikovim ogrodjem citrulina in aspartatom z nukleofilnim napadom in posledično odstranitvijo vode. Encim arginin sukcinat sintetaza potrebuje molekulo ATP, zato pride do energetskega povezovanja: hidroliza ATP v AMP in pirofosfat (slednji se nato pretvori v dve molekuli ortofosfata) se pojavi z izgonom molekule d "vode iz substrata in ne z delovanjem vode medija.
"Naslednji encim je"arginin sukcinaza: ta encim lahko v citoplazmi razcepi arginin sukcinat na arginin in fumarat.
Encim zaključi cikel sečnine arginaza: dobimo sečnino in ornitin; sečnino odstranijo ledvice (urin), medtem ko se ornitin vrne v mitohondrije in nadaljuje cikel.
Cikel sečnine je podvržen posredni modulaciji z argininom: kopičenje arginina kaže, da je treba cikel sečnine pospešiti; modulacija arginina je posredna, ker arginin pozitivno modulira encim acetil glutamat sintetazo. Slednji je sposoben prenesti acetilno skupino na dušik glutamata: nastane N-acetil glutamat, ki je neposreden modulator encima karbamil-fosfosintetaze.
Arginin se kopiči kot presnovek cikla sečnine, če proizvodnja karbamil fosfata ne zadošča za odstranitev ornitina.
Urea se proizvaja samo v jetrih, vendar obstajajo tudi druga mesta, kjer potekajo prve reakcije.
Možgani in mišice uporabljajo posebne strategije za odpravo amino skupin. Možgani uporabljajo zelo učinkovito metodo, pri kateri se uporablja encim glutamin sintetaza in encim glutamaza: prvi je prisoten v nevronih, drugi pa v jetrih. Ta mehanizem je zelo učinkovit iz dveh razlogov:
Dve amino skupini se prevažata iz možganov v jetra v enem vozilu;
Glutamin je veliko manj strupen kot glutamat (tudi glutamat izvaja prenos nevronov in ne sme presegati fiziološke koncentracije).
Pri ribah podoben mehanizem prinaša aminokislino aminokislin v škrge.
Iz mišic (skeletnih in srčnih) amino skupine pridejo v jetra skozi cikel glukoza-alanin; encim, ki je vključen, je glutamin-piruvat transaminaza: omogoča transpozicijo amino skupin (ki so v obliki glutamata), pretvorbo piruvata v alanin in hkrati glutamat v α-ketoglutarat v mišici ter katalizacijo obratni proces v jetrih.
Transaminaze z različnimi nalogami ali položaji imajo tudi strukturne razlike in jih je mogoče določiti z elektroforezo (imajo različne izoelektrične točke).
Prisotnost transaminaz v krvi je lahko simptom poškodbe jeter ali srca (tj. Poškodbe tkiva jeter ali srčnih celic); transaminaze so v zelo visokih koncentracijah tako v jetrih kot v srcu: z elektroforezo je mogoče ugotoviti, ali je prišlo do poškodbe v jetrih ali srčnih celicah.