Splošnost
Zdravljenje kronične mieloične levkemije (CML) vključuje več terapevtskih možnosti, ki lahko bolezen obdržijo dalj časa. Rutinski testi krvi in kostnega mozga ter pogosto ocenjevanje s strani hematologa ali onkologa lahko spremljajo napredovanje raka.

Iz rezultatov medicinskih preiskav (krvna slika, citogenetski in molekularni testi) je mogoče razumeti:
- Stopnja učinkovitosti zdravljenja skozi čas in razvoj odziva na terapijo;
- Če se bolezen ne odziva več na zdravila (odpornost na terapijo).
Spremljanje in odziv na terapijo
Pravilno spremljanje poteka bolezni je bistveno za preverjanje učinkovitosti terapije in posledično za takojšnje posredovanje v primeru neuspešnega zdravljenja.
Citogenetske analize in raziskave molekularne biologije se uporabljajo tudi v diagnostične namene tudi za oceno stopnje odziva na terapevtski protokol in za poudarjanje obstojnosti bolezni po zdravljenju (študija minimalne preostale bolezni):
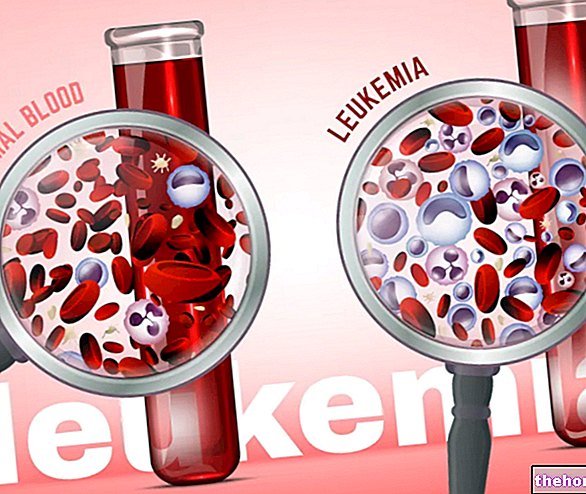
- Popoln hematološki odziv: Ko začne terapija učinkovati, se število celic levkemije zmanjša. Hematološki testi ne morejo več zaznati aberantnih klonov, vendar je to mogoče s citogenetsko analizo.
- Popoln citogenetski odziv: dobljen, ko prisotnost Philadelphia kromosoma (Ph) ni več poudarjena s konvencionalno citogenetsko analizo (standardni pristop za spremljanje odziva na zdravljenje) ali s fluorescenčno hibridizacijo in situ (FISH), tehniko, ki ocenjuje odstotek Ph + celice kostnega mozga. Citogenetska analiza, izvedena na vzorcu kostnega mozga s fino iglo, je tudi edina metoda za ugotavljanje prisotnosti kakršnih koli kromosomskih sprememb, razen kromasoma Philadelphia, s prognostično vlogo.
- Popoln molekularni odziv: doseže se, ko molekularna analiza ne more zaznati izražanja hibridnega gena BCR / ABL. Terapija se je izkazala za učinkovito in molekularni signali, ki spodbujajo proizvodnjo proteinov bcr-abl, so tako nizki, da jih ni mogoče zaznati niti z zelo občutljivimi testi, kot so molekularni. Zvišane ravni prepisov, ki jih spremljamo, lahko kažejo na izgubo odziva na zdravljenje.
Doseganje teh rezultatov predstavlja zelo pomemben rezultat: številne študije kažejo, da imajo bolniki s popolnim citogenetskim in molekularnim odzivom zelo veliko verjetnost, da bodo dolgo preživeli, ne da bi bolezen napredovala v pospešeno in / ali blastno fazo .
Na učinkovitost terapije lahko vplivajo številni dejavniki, zato je v začetnih fazah priporočljivo nadaljevati s testi po 3, 6, 12 in 18 mesecih.
Doslej pridobljeni podatki iz kliničnih študij, ki opredeljujejo optimalen odziv in neuspeh v različnih časih zdravljenja, so privedli do oblikovanja sheme spremljanja, ki jo je treba upoštevati za pravilno vodenje bolnika (indikacije predlaga Evropska mreža levkemije):
Hematolog (ali onkolog) bo lahko določil nekatere cilje in preveril učinkovitost terapije v konkretnem kliničnem primeru, saj se bolniki na terapijo odzovejo drugače in ne morejo vsi doseči optimalnih terapevtskih mejnikov v predvidenem časovnem obdobju. ...
Terapevtske možnosti
Glavni cilj zdravljenja CML je "doseči popolno molekularno remisijo: bolezen zdravimo z zdravljenjem (tudi če ne izgine popolnoma)", število proizvedenih patoloških klonov pa je dovolj omejeno, da ne povzroča nobenih simptomov. Večina ljudi ne more popolnoma znebite celic levkemije, zdravljenje lahko pomaga doseči dolgotrajno remisijo bolezni.
Terapevtski cilji lahko vključujejo:
- Omejite manifestacijo simptomov kronične mieloične levkemije;
- Obnovi normalne parametre, povezane s številom krvnih celic;
- Zmanjšajte število celic s Philadelphia kromosomsko levkemijo (Ph +) in molekularnih signalov (BCR / ABL prepisi);
- Cilj za izginotje Philadelphia + kromosomov (popoln citogenetski odziv).
Konvencionalna antiblastična zdravila
Nekatera antiblastična zdravila, npr busulfan (alkiliranje) in l "hidroksisečnino (specifični zaviralec sinteze DNA), so bili še posebej v preteklosti uporabljeni za doseganje citoredukcije in obvladovanje bolezni v kronični fazi. Konvencionalno zdravljenje je povzročilo izboljšanje kakovosti življenja, vendar ni moglo bistveno spremeniti naravne zgodovine bolezni ali preprečiti napredovanja v pospešeno / blastno fazo.
Rekombinantni interferon-alfa
Od zgodnjih osemdesetih let je bila uvedba interferonov dovoljeno opazovati, poleg zmanjšanja in normalizacije deleža granulocitov, doseganje negativizacije citogenetskih in molekularnih testov, ki povzročajo daljše trajanje kronične faze, s posledičnim zmanjšanjem razvoja v pospešeni in / ali blastni fazi. Interferon -alfa je zmanjšal vlogo običajne terapije s KML: to zdravilo lahko pri 20-30% bolnikov sproži popoln citogenetski odziv, zlasti moti prevajanje proliferativnih signalov v celicah Ph + in zavira celice množenja celic. Interferon-alfa deluje tudi s posrednim mehanizmom na preživetje celic levkemije, zmanjšuje njihovo adhezijo in povečuje aktivnost celic imunskega sistema.
Omejitev uporabe tega zdravila je zaradi njegove zanemarljive strupenosti.Neželeni učinki interferona vključujejo utrujenost, zvišano telesno temperaturo in izgubo telesne teže. Da bi izboljšali dosežene rezultate, so interferon kombinirali z drugimi citotoksičnimi učinkovinami. Samo povezanost interferona s citozin arabinozidom (ARA-C) je pokazala boljše rezultate kot interferon sam, brez očitne prednosti preživetja.
Alogenska presaditev kostnega mozga
Presaditev matičnih celic od zdravega darovalca, združljivega s prejemnikom (alogenska presaditev), že leta predstavlja najpogostejšo terapevtsko indikacijo in je še danes edino zdravljenje, ki lahko dokončno izkorenini neoplazmo.
Ta postopek, če se izvede v kronični fazi, lahko v približno 50% primerov povzroči petletno preživetje brez bolezni.
Alogenska presaditev kostnega mozga vključuje prvo fazo uničenja vseh (ali skoraj vseh) celic Ph + s kondicionirno terapijo (kemoterapija v kombinaciji s obsevanjem celotnega telesa), čemur sledi rekonstitucija hematopoetskega mozga z infuziranimi matičnimi celicami darovalci. Poleg tega limfociti donorskega kostnega mozga prispevajo k nadzoru in / ali odpravi vseh celic Ph + z imunsko posredovanim učinkom, imenovanim učinek "presadek proti levkemiji" (presadek proti levkemiji). Odziv na terapijo je mogoče spremljati z oceno, ali so molekularne spremembe, značilne za kronično mieloično levkemijo, izginile. Alogenska presaditev kostnega mozga predstavlja terapevtsko zdravljenje, ki lahko "ozdravi" KML, vendar na žalost vključuje stopnjo neuspešnosti zaradi usodne toksičnosti in / ali ponovitve. Ta postopek je pravzaprav zelo zahteven in nanj lahko vplivajo starost pacient in bolnik ter prezgodnja presaditev (meseci ali leta od diagnoze kronične faze): zaradi potencialne nevarnosti je izvedljivo le pri bolnikih, mlajših od 55 let, brez nadaljnjih spremljajočih patologij. Zato alogenska presaditev predstavlja resnično terapevtsko priložnost le za manjše število bolnikov s KML (upoštevajoč tudi težave pri iskanju združljivega darovalca matičnih celic).
V zadnjem času so pri osebah s kronično mieloično levkemijo, ki niso upravičene do alografta (starost, pomanjkanje darovalca, zavrnitev itd.), Predlagali avtotransplantacijo. Pacientov kostni mozeg, ponovno infuziran po "namerno ustrezni citocidni terapiji za celice Ph + (z antiblastičnim + interferonom), bi se obnovil s prevladujočo ponovno razširitvijo Ph-celic.
Imatinib mezilat (Glivec ®)
Zgodovina zdravljenja kronične mieloične levkemije je bila revolucionirana z uvedbo prvega zaviralca tirozin kinaze (imatinib mezilat), ki je močno prispeval k izboljšanju kakovosti življenja bolnikov.
Imatinib je specifičen zaviralec BCR / ABL, zasnovan po razumevanju molekularne biologije bolezni in uporabljen pri zdravljenju Ph + kronične mieloične levkemije.
Zdravilo lahko povzroči popolno molekularno citogenetsko remisijo pri 80-90% bolnikov, aktivno pa je tudi pri mieloidnih novotvorbah z eozinofilijo in vpletenostjo PDGRF (rastni faktor, pridobljen iz trombocitov, serumski mitogen, vključen v številna patološka stanja, kar spodbuja kemotaksijo in proliferacijo zmogljivost).
Imatinib selektivno blokira aktivnost tirozin kinaze BCR / ABL z zaviralnim mehanizmom ATP: zdravilo veže visoko energijsko molekulo (ATP), ki je na voljo v določeni domeni BCR / ABL kinaze, preprečuje fosforilacijo drugih substratov in blokira kaskado reakcij, ki bi bile odgovorne za proces nastajanja Ph + levkemičnih klonov. Odmerek te molekule (imatinib metizilat) se giblje od 400 mg / dan do 800 mg / dan glede na fazo bolezni in odziv. Trenutno je zaradi svoje izjemne učinkovitosti zdravilo izbire za zdravljenje KML. Neželeni učinki, ki so reverzibilni pri suspenziji in / ali zmanjšanju odmerka, so lahko različni (povečane transaminaze, slabost, kožni izpuščaji, zastajanje tekočine itd.).
Sčasoma so opazili primere, ki kažejo odpornost na zdravilo (na primer bolnike z napredovalo boleznijo), in opredelili so biološko-klinična merila za opredelitev vrste odziva na zdravljenje. Zdi se, da so mehanizmi, odgovorni za to odpornost, več (mutacije kinazne domene, amplifikacija / prekomerna ekspresija BCR / ABL, klonska evolucija ...). V teh primerih nadaljevanje zdravljenja z imatinibom ni več primerno.
Za bolnike s temi stanji so možne naslednje možnosti:
- Alogenska presaditev;
- Konvencionalna terapija (hidroksisečnina, busulfan itd.);
- L "interferon;
- Eksperimentalna terapija (z zaviralci tirozin kinaze druge generacije).
Zaviralci tirozin kinaze druge generacije
Neuspeh pri zdravljenju z imatinibom je povezan z napredovanjem pospešene in / ali blastne faze kronične mieloične levkemije in ima posebno slabo prognozo. V zadnjih letih so farmakološke raziskave v klinični praksi dovolile uporabo zaviralcev tirozin kinaze druge generacije, aktivnih pri bolnikih, pri katerih je prišlo do odpornosti na imatinib: Dasatinib (Sprycel ®) in Nilotinib (Tasigna ®) se uporabljajo pri bolnikih s kronično fazo in / ali napredovanje CML, odporno na Glivec ® in lahko ponovno inducira popolne in obstojne hematološke, citogenetske in molekularne odzive. Številne študije pa so pokazale, da lahko klon Ph + zaradi svoje genetske nestabilnosti razvije mutacije domeno kinaze BCR / ABL in se izkažejo za odporne na različna zaviralna zdravila. Druge molekule v poskusni fazi (zaviralci 3. generacije) so namenjene specifičnim tarčam kronične mieloične levkemije; zlasti so sposobne preobčutiti levkemične celice Ph + s specifičnimi mutacijami (primer: Mk-0457 za odporno CML in z mutacijo T315I, ki neposredno vpliva mesto vezave imatiniba).
Drugi članki o zdravljenju kronične mieloične levkemije
- Kronična mieloična levkemija: Kronična mieloična levkemija: diagnoza
- Kronična mieloična levkemija: opredelitev, vzroki, simptomi