Aktivne sestavine: Sunitinib
SUTENT 12,5 mg trde kapsule
SUTENT 25 mg trde kapsule
SUTENT 37,5 mg trde kapsule
SUTENT 50 mg trde kapsule
Indikacije Zakaj se zdravilo Sutent uporablja? Za kaj je to?
Sutent vsebuje zdravilno učinkovino sunitinib, ki je zaviralec proteinske kinaze. Uporablja se za zdravljenje raka s preprečevanjem delovanja posebne skupine beljakovin, za katere je znano, da sodelujejo pri rasti in širjenju rakavih celic.
Zdravilo Sutent vam bo predpisal le zdravnik, ki ima izkušnje z uporabo zdravil proti raku.
Sutent se uporablja za zdravljenje odraslih z naslednjimi vrstami raka:
- Stromalni rak prebavil (GIST), vrsta raka želodca in črevesja, v primerih, ko imatinib (drugo zdravilo proti raku) ne deluje več ali ga ni več mogoče jemati.
- Metastatski rak ledvic (MRCC), vrsta raka ledvic, ki se je razširil na druge dele telesa.
- Nevroendokrini tumorji trebušne slinavke (pNET) (tumorji celic trebušne slinavke, ki proizvajajo hormone), ki napredujejo ali se ne dajo odstraniti
. Če niste prepričani, kako zdravilo Sutent deluje ali zakaj je bilo to zdravilo predpisano vam, se posvetujte z zdravnikom.
Kontraindikacije Kadar zdravila Sutent ne smete uporabljati
Ne jemljite zdravila Sutent:
- Če ste alergični na sunitinib ali katero koli sestavino tega zdravila (navedeno v poglavju 6).
Previdnostni ukrepi pri uporabi Kaj morate vedeti, preden boste vzeli zdravilo Sutent
Preden vzamete zdravilo Sutent, povejte svojemu zdravniku:
- Če imate visok krvni tlak. Zdravilo Sutent lahko povzroči zvišanje krvnega tlaka. Zdravnik vam bo med jemanjem zdravila Sutent morda preveril krvni tlak in bo po potrebi jemal zdravila za znižanje krvnega tlaka.
- Če imate ali ste imeli motnje krvi, težave s krvavitvami ali modrice. Zdravljenje z zdravilom Sutent lahko povzroči povečano tveganje za krvavitev, spremembe v številu določenih krvnih celic, katerih pomanjkanje vodi v anemijo ali vpliva na sposobnost strjevanja krvi. Tveganje za krvavitev je lahko večje, če jemljete varfarin ali acenokumarol, zdravila, ki redčijo kri, da preprečijo nastanek krvnih strdkov. Povejte svojemu zdravniku, če med jemanjem zdravila Sutent pride do krvavitve.
- Če imate težave s srcem. Sutent lahko povzroči težave s srcem. Povejte svojemu zdravniku, če se počutite zelo utrujeni, težko dihate ali imate otekle noge in gležnje.
- Če opazite nenormalne spremembe srčnega ritma. Sutent lahko povzroči spremembe v srčnem ritmu. Med zdravljenjem z zdravilom Sutent vam bo zdravnik morda dal elektrokardiogram, da oceni obseg teh sprememb.
- Če ste pred kratkim imeli težave s krvnimi strdki v venah in / ali arterijah (vrste krvnih žil), vključno z možgansko kapjo, srčnim infarktom, embolijo ali trombozo. Takoj se obrnite na svojega zdravnika, če med zdravljenjem s Sutentom začutite tesnost ali bolečino v prsih, bolečine v rokah, hrbtu, vratu ali čeljusti, zasoplost, odrevenelost ali šibkost na eni strani telesa, tresenje pri hoji, bolečino ali omotico.
- Če imate težave s ščitnico. Sutent lahko povzroči težave s ščitnico. Povejte svojemu zdravniku, če se med jemanjem zdravila Sutent lažje utrudite, če ste na splošno hladnejši od drugih ljudi ali če se vaš glas zniža. Pred jemanjem zdravila Sutent in redno med jemanjem zdravila je treba preveriti delovanje ščitnice. Če ščitnica ne proizvaja dovolj ščitničnega hormona, bo morda treba vzeti nadomestni ščitnični hormon.
- Če imate ali ste imeli težave s trebušno slinavko ali žolčnikom. Povejte svojemu zdravniku, če opazite katerega od naslednjih znakov in simptomov: bolečine v trebuhu (zgornjem delu trebuha), slabost, bruhanje in zvišano telesno temperaturo, ki jih lahko povzroči vnetje trebušne slinavke ali žolčnika.
- Če imate ali ste kdaj imeli težave z jetri. Povejte svojemu zdravniku, če med zdravljenjem z zdravilom Sutent opazite katerega od naslednjih znakov in simptomov jetrnih težav: srbenje, porumenelost kože ali oči, temen urin ter bolečine ali nelagodje v zgornjem desnem predelu želodca. opraviti teste za preverjanje delovanja jeter pred in med zdravljenjem z zdravilom Sutent ter po potrebi klinično.
- Če imate ali ste imeli težave z ledvicami. Zdravnik bo spremljal delovanje ledvic.
- Če vas čaka operacija ali ste bili pred kratkim operirani. Sutent lahko vpliva na način celjenja ran. Na splošno, če boste imeli operacijo, morate prenehati uporabljati Sutent. Zdravnik se bo odločil, kdaj bo spet začel zdravljenje s Sutentom.
- Pred začetkom zdravljenja z zdravilom Sutent je priporočljivo opraviti zobozdravniški pregled.
- če imate ali ste imeli bolečine v ustih, zobeh in / ali čeljusti, otekanje ali rane v ustih, odrevenelost ali občutek teže v čeljusti ali popuščanje zob, takoj obvestite svojega zdravnika in zobozdravnika.
- če ste na invazivnem zobozdravstvenem posegu ali zobozdravstveni operaciji, povejte svojemu zdravniku, da se zdravite z zdravilom Sutent, zlasti če jemljete tudi intravenske bisfosfonate ali ste jih jemali že prej.Bisfosfonati so zdravila, ki se uporabljajo za preprečevanje kostnih zapletov, ki so bili morda predpisani za drugo zdravstveno težavo.
- Če imate ali ste kdaj imeli težave s kožo in podkožjem. Med zdravljenjem s tem zdravilom se lahko pojavi "gangrenozna pioderma" (boleča razjeda na koži) ali "nekrotizirajoči fasciitis" (hitro razširjena "okužba kože / mehkih tkiv, ki je lahko usodna). Prekinitev zdravljenja. Resne kožne reakcije (Stevens-Johnson sindrom, toksična epidermalna nekroliza, multiformni eritem) so poročali pri uporabi sunitiniba, ki se je sprva pojavljal na trupu kot rdečkaste tarčaste lise ali krožne lise, pogosto z mehurčki v sredini. Reakcija lahko napreduje do razširjenega mehurjenja ali luščenja kože in je lahko usodna. Če se pojavi izpuščaj ali kateri od teh kožnih simptomov, se nemudoma posvetujte z zdravnikom.
- Če imate ali ste imeli napade. Čim prej obvestite svojega zdravnika, če imate visok krvni tlak, glavobol, izgubo vida.
- Če imate sladkorno bolezen. Pri bolnikih s sladkorno boleznijo je treba redno preverjati raven sladkorja v krvi, da bi ugotovili, ali je treba spremeniti odmerek zdravil za sladkorno bolezen, da bi zmanjšali tveganje za nizek krvni sladkor.
Otroci in mladostniki
Sutent ni indiciran za bolnike, mlajše od 18 let. Zdravila Sutent pri otrocih in mladostnikih niso preučevali.
Interakcije Katera zdravila ali živila lahko spremenijo učinek zdravila Sutent
Povejte svojemu zdravniku ali farmacevtu, če jemljete, ste pred kratkim jemali ali pa boste morda začeli jemati katero koli drugo zdravilo, tudi če ste ga dobili brez recepta in zdravila brez recepta.
Nekatera zdravila lahko spremenijo raven Sutenta v telesu. Zdravniku morate povedati, če jemljete zdravila, ki vsebujejo naslednje učinkovine:
- ketokonazol, itrakonazol - uporablja se za zdravljenje glivičnih okužb
- eritromicin, klaritromicin, rifampicin - uporabljajo se za zdravljenje okužb
- ritonavir - uporablja se za zdravljenje aidsa
- deksametazon - kortikosteroid, ki se uporablja za več stanj
- fenitoin, karbamazepin, fenobarbital - uporabljajo se za zdravljenje epilepsije in drugih nevroloških stanj
- zeliščni pripravki, ki vsebujejo šentjanževko (Hypericum perforatum) - uporabljajo se za zdravljenje depresije in tesnobe
Zadostno s hrano in pijačo
Med zdravljenjem z zdravilom Sutent se je treba izogibati vnosu grenivkinega soka.
Opozorila Pomembno je vedeti, da:
Nosečnost in dojenje
Če ste noseči ali sumite, da ste noseči, obvestite svojega zdravnika.
Sutent se med nosečnostjo ne sme uporabljati, razen če je to nujno potrebno. Zdravnik se bo z vami pogovoril o možnih tveganjih Sutentnega zdravljenja med nosečnostjo.
Če je nosečnost možna, morate med zdravljenjem z zdravilom Sutent uporabljati zanesljivo metodo kontracepcije.
Če dojite, obvestite svojega zdravnika. Med zdravljenjem z zdravilom Sutent ne smete dojiti.
Vpliv na sposobnost upravljanja vozil in strojev
Če ste omotični ali nenavadno utrujeni, bodite še posebej previdni pri vožnji ali upravljanju strojev.
Odmerjanje, način in čas dajanja Kako uporabljati Sutent: Odmerjanje
Pri jemanju tega zdravila natančno upoštevajte zdravnikova navodila.
Če ste v dvomih, se posvetujte z zdravnikom. Zdravnik vam bo predpisal pravi odmerek glede na vrsto raka, ki ga morate zdraviti. Če se zdravite zaradi GIST ali MRCC, je običajni odmerek 50 mg enkrat na dan 28 dni (4 tedne), nato pa 14 dni (2 tedna) počitka (brez zdravil) v 6 -tedenskih ciklih. Če se zdravite zaradi pNET, je običajen odmerek 37,5 mg enkrat na dan brez počitka. Zdravnik vam bo določil odmerek, ki ga potrebujete, in kdaj prekiniti zdravljenje s Sutentom. Sutent se lahko jemlje s hrano ali brez nje.
Preveliko odmerjanje Kaj storiti, če ste vzeli preveč zdravila Sutent
Če ste vzeli večji odmerek zdravila Sutent, kot bi smeli
Če ste pomotoma vzeli preveč kapsul, se takoj posvetujte z zdravnikom. Morda bo potrebna zdravniška pomoč
Če ste pozabili vzeti zdravilo Sutent
Ne vzemite dvojnega odmerka, če ste pozabili vzeti prejšnji odmerek.
Neželeni učinki Kakšni so stranski učinki zdravila Sutent
Kot vsa zdravila ima lahko tudi to zdravilo neželene učinke, ki pa se ne pojavijo pri vseh bolnikih.
Takoj se posvetujte z zdravnikom, če opazite katerega od teh resnih neželenih učinkov (glejte tudi Kaj morate vedeti, preden boste vzeli zdravilo Sutent):
Težave s srcem. Povejte svojemu zdravniku, če se počutite zelo utrujeni, težko dihate ali imate otekle noge in gležnje. To so lahko simptomi srčnih težav, kot so srčno popuščanje in težave s srčno mišico (kardiomiopatija).
Težave s pljuči ali dihanjem. Povejte svojemu zdravniku, če imate kašelj, bolečine v prsih, nenaden pojav zasoplosti ali izkašljevanje krvi. To so lahko simptomi pljučne embolije, ki se pojavi, ko krvni strdki potujejo v pljuča.
Težave z ledvicami. Povejte svojemu zdravniku, če opazite "spremenjeno pogostost ali odsotnost uriniranja, kar bi lahko bili simptomi" odpovedi ledvic.
Krvavitev. Takoj obvestite svojega zdravnika, če med jemanjem zdravila Sutent opazite katerega od naslednjih simptomov ali resno krvavitev: otekel, boleč želodec (trebuh); bruhanje s krvjo; temno, lepljivo blato; glavobol ali spremembe duševnega stanja, izkašljevanje krvi ali izpljunka s krvjo iz pljuč ali dihalnih poti.
Uničenje tumorja, ki povzroči perforacijo črevesja. Povejte svojemu zdravniku, če imate hude bolečine v črevesju, zvišano telesno temperaturo, slabost, bruhanje, kri v blatu ali spremembe v črevesnih navadah.
Drugi neželeni učinki, ki se lahko pojavijo pri uporabi zdravila Sutent, so:
Zelo pogosti neželeni učinki (pojavijo se lahko pri več kot 1 od 10 bolnikov)
- Zmanjšanje števila trombocitov, rdečih krvnih celic in / ali belih krvnih celic (npr. Nevtrofilcev).
- Zasoplost
- Visok krvni pritisk.
- Prekomerna utrujenost, izguba moči.
- Oteklina zaradi tekočine pod kožo in okoli oči, globok alergijski izpuščaj.
- Bolečine / draženje v ustih, bolečina / vnetje / suha usta, motnje okusa, želodčne motnje, slabost, bruhanje, driska, zaprtje, bolečine v trebuhu / oteklina, izguba / zmanjšanje apetita.
- Zmanjšana aktivnost ščitnice (hipotiroidizem).
- Vrtoglavica
- Glavobol.
- Krvavitev iz nosu.
- Bolečine v hrbtu, bolečine v sklepih.
- Bolečine v rokah in nogah.
- Rumenenje kože / razbarvanje kože, prekomerna pigmentacija kože, razbarvanje las, izpuščaj na dlaneh in podplatih, izpuščaj, suha koža.
- Kašelj.
- Vročina.
- Težko zaspati.
Pogosti neželeni učinki (pojavijo se lahko pri 1 do 10 na 100 bolnikov)
- Nastanek strdkov v krvnih žilah.
- Nezadosten dotok krvi v srčno mišico zaradi obstrukcije ali zožitve koronarnih arterij.
- Bolečina v prsnem košu.
- Zmanjšana količina krvi, ki jo črpa srce.
- Zadrževanje tekočine tudi okoli pljuč.
- Okužbe.
- Znižana raven sladkorja v krvi. Če opazite znake in simptome nizkega krvnega sladkorja: Če občutite utrujenost, palpitacije, znojenje, lakoto in izgubo zavesti, čim prej obvestite svojega zdravnika.
- Izguba beljakovin v urinu, kar včasih povzroči otekanje.
- Sindrom gripe.
- Nenormalni krvni testi, vključno z jetrnimi in encimi trebušne slinavke.
- Visoke ravni sečne kisline v krvi.
- Hemoroidi, rektalna bolečina, krvavitev dlesni, težave pri požiranju ali nezmožnost požiranja.
- Pekoč ali boleč občutek v jeziku, vnetje sluznice prebavnega trakta, odvečni plin v želodcu ali črevesju.
- Izguba teže.
- Mišično -skeletne bolečine (bolečine v mišicah in kosteh), mišična oslabelost, mišična utrujenost, mišične bolečine, mišični krči.
- Suhost nosu, zamašen nos.
- Prekomerno solzenje.
- Spremembe občutljivosti kože, suha koža, srbenje, luščenje in vnetje kože, mehurji, akne, razbarvanje nohtov, izpadanje las.
- Nenormalni občutki v okončinah.
- Pretirano zmanjšanje / povečanje občutljivosti, zlasti na dotik.
- Pekoč občutek v želodcu.
- Dehidracija.
- Rdečica obraza.
- Sprememba barve urina.
- Depresija.
- Mrzlica.
Občasni neželeni učinki (pojavijo se lahko pri 1 do 10 na 1.000 bolnikov)
- Okužbe mehkih tkiv, tudi v anogenitalni regiji, so potencialno smrtno nevarne.Takoj se obrnite na svojega zdravnika, če se pojavijo simptomi okužbe okoli kožne rane, vključno z zvišano telesno temperaturo, bolečino, pordelostjo, oteklino ali odvajanjem gnoja ali krvi.
- Možganska kap.
- Srčni napad zaradi prekinitve ali zmanjšane oskrbe srca s krvjo.
- Spremembe električne aktivnosti srca ali spremenjen srčni ritem.
- Tekočina okoli srca (perikardni izliv).
- Jetrna insuficienca.
- Bolečine v želodcu (trebuhu), ki jih povzroča "vnetje trebušne slinavke.
- Uničenje tumorja, ki povzroči perforacijo črevesja.
- Vnetje (otekanje in pordelost) žolčnika z ali brez pripadajočih kamnov.
- Nenormalen komunikacijski kanal med dvema telesnima votlinama ali s kožo.
- Bolečine v ustih, zobeh in / ali čeljusti, otekanje ali draženje v ustih, odrevenelost ali občutek teže v čeljusti ali popuščanje zob. To so lahko znaki in simptomi poškodbe čeljustne kosti (osteonekroza). Če opazite katerega od teh znakov in simptomov, takoj obvestite svojega zdravnika in zobozdravnika.
- Prekomerna proizvodnja ščitničnih hormonov ima za posledico povečano presnovo. Težave pri celjenju ran po operaciji.
- Povečanje mišičnega encima v krvi (kreatin fosfokinaza).
- Neustrezna in pretirana reakcija na alergene.
Redki neželeni učinki (pojavijo se lahko pri 1 do 10 na 10.000 ljudi)
- Hude reakcije kože in / ali sluznice (Stevens-Johnsonov sindrom, toksična epidermalna nekroliza, multiformni eritem).
- Sindrom tumorske lize (TLS) - TLS obsega niz presnovnih zapletov, ki se lahko pojavijo med zdravljenjem raka. Povzročajo jih produkti razpada prizadetih rakavih celic in lahko vključujejo: slabost, težko dihanje, nepravilen srčni utrip, mišične krče, krče, moten urin in utrujenost, povezano z nenormalnimi laboratorijskimi testi (visoke ravni kalija, sečne kisline in fosforne kisline) in nizke ravni kalcija v krvi), kar lahko povzroči spremembe v delovanju ledvic in akutno odpoved ledvic.
- Nenormalna razčlenitev mišic, ki lahko povzroči težave z ledvicami (rabdomioliza).
- Motnje delovanja možganov, ki lahko povzročijo različne simptome, kot so glavobol, zmedenost, epileptični napadi in izguba vida (sindrom zadnje reverzibilne levkoencefalopatije).
- Boleče razjede na koži (gangrenozna pioderma).
- Vnetje jeter (hepatitis).
- Vnetje ščitnice.
Poročanje o stranskih učinkih
Če opazite kateri koli neželeni učinek, se posvetujte z zdravnikom, kar vključuje morebitne neželene učinke, ki niso navedeni v tem navodilu. O neželenih učinkih lahko poročate tudi neposredno prek nacionalnega sistema poročanja, navedenega v Dodatku V. S poročanjem o neželenih učinkih lahko pomagate zagotoviti več informacij o varnosti tega zdravila.
Potek in hramba
- Zdravilo shranjujte nedosegljivo otrokom!
- Tega zdravila ne smete uporabljati po datumu izteka roka uporabnosti, ki je naveden na škatli in na nalepki poleg oznake "EXP". Rok uporabnosti se nanaša na zadnji dan v mesecu.
- Za shranjevanje tega zdravila niso potrebni posebni pogoji.
- Tega zdravila ne uporabljajte, če opazite, da je ovojnina poškodovana ali kaže znake nedovoljenega poseganja.
Ne mečite nobenih zdravil v odpadne vode ali med gospodinjske odpadke. Vprašajte svojega farmacevta, kako zavreči zdravila, ki jih ne uporabljate več. Tako boste zaščitili okolje.
Kaj vsebuje Sutent
Sutentne 12,5 mg trde kapsule
Zdravilna učinkovina je sunitinib. Vsaka kapsula vsebuje 12,5 mg sunitiniba.
Druge sestavine so:
- Vsebina kapsule: manitol (E421), natrijeva kroskarmeloza, povidon (K-25) in magnezijev stearat.
- Ovojnica kapsule: želatina, rdeči železov oksid (E172) in titanov dioksid (E171).
- Črnilo: šelak, propilenglikol, natrijev hidroksid, povidon in titanov dioksid (E171).
Sutentne 25 mg trde kapsule
Zdravilna učinkovina je sunitinib. Vsaka kapsula vsebuje 25 mg sunitiniba.
Druge sestavine so:
- Vsebina kapsule: manitol (E421), natrijeva kroskarmeloza, povidon (K-25) in magnezijev stearat.
- Ovojnica kapsule: želatina, titanov dioksid (E171), rumeni železov oksid (E172), rdeči železov oksid (E172), črni železov oksid (E172).
- Črnilo: šelak, propilenglikol, natrijev hidroksid, povidon in titanov dioksid (E171)
Sutentne 37,5 mg trde kapsule
Zdravilna učinkovina je sunitinib. Vsaka kapsula vsebuje sunitinib malat, kar ustreza 37,5 mg sunitiniba.
Druge sestavine so:
- Vsebina kapsule: manitol (E421), natrijeva kroskarmeloza, povidon (K-25) in magnezijev stearat.
- Ovojnica kapsule: želatina, titanov dioksid (E171), rumeni železov oksid (E172).
- Črnilo: šelak, propilenglikol, kalijev hidroksid, črni železov oksid (E172).
Sutentne 50 mg trde kapsule
Zdravilna učinkovina je sunitinib. Ena kapsula vsebuje sunitinib malat, kar ustreza 50 mg sunitiniba.
Druge sestavine so:
- Vsebina kapsule: manitol (E421), natrijeva kroskarmeloza, povidon (K-25) in magnezijev stearat.
- Ovojnica kapsule: želatina, titanov dioksid (E171), rumeni železov oksid (E172), rdeči železov oksid (E172) in črni železov oksid (E172).
- Črnilo: šelak, propilenglikol, natrijev hidroksid, povidon in titanov dioksid (E171).
Opis izgleda Sutent in vsebina pakiranja
Sutent 12,5 mg je na voljo v obliki trdih želatinskih kapsul z oranžnim pokrovčkom in ohišjem, z napisom "Pfizer" v belem črnilu na pokrovčku in "STN 12,5 mg" na telesu, ki vsebuje obarvana zrnca. Rumeno-oranžna.
Sutent 25 mg je na voljo v obliki trdih želatinskih kapsul s karamelnim pokrovom in oranžnim telesom, z napisom "Pfizer" v belem črnilu na pokrovčku in "STN 25 mg" na telesu, ki vsebuje barvna zrnca. Rumeno-oranžna.
Sutent 37,5 mg je na voljo v obliki trdih želatinskih kapsul z rumeno kapico in ohišjem, z napisom "Pfizer" s črnim črnilom na pokrovčku in "STN 37,5 mg" na telesu, ki vsebuje obarvana zrnca. Rumeno-oranžna.
Sutent 50 mg je na voljo v obliki trdih želatinskih kapsul s pokrovčkom in ohišjem v karamelni barvi, z "Pfizer" v belem črnilu na pokrovčku in "STN 50 mg" na telesu, ki vsebuje rumeno-oranžna zrnca.. Na voljo je v steklenicah po 30 kapsul in perforiranih pretisnih omotih za eno dozo, ki vsebujejo 28 x 1 kapsulo.
Na trgu ni vseh navedenih pakiranj.
Navodilo za uporabo vira: AIFA (Italijanska agencija za zdravila). Vsebina, objavljena januarja 2016. Prisotne informacije morda niso posodobljene.
Za dostop do najnovejše različice je priporočljivo dostopati do spletnega mesta AIFA (Italijanska agencija za zdravila). Zavrnitev odgovornosti in koristne informacije.
01.0 IME ZDRAVILA
SUTENT 12,5 mg trdi kapsule
02.0 KAKOVOSTNA IN KOLIČINSKA SESTAVA
Ena kapsula vsebuje sunitinib malat, kar ustreza 12,5 mg sunitiniba.
Za celoten seznam pomožnih snovi glejte poglavje 6.1.
03.0 FARMACEVTSKA OBLIKA
Trda kapsula.
Želatinske kapsule z oranžnim pokrovom in telesom, označene z belim črnilom "Pfizer" na pokrovčku, "STN 12,5 mg" na telesu in vsebujejo rumeno-oranžna zrnca.
04.0 KLINIČNE INFORMACIJE
04.1 Terapevtske indikacije
Stromalni tumor prebavil (GIST)
Zdravilo SUTENT je indicirano za zdravljenje neoperabilnega in / ali metastatskega gastrointestinalnega stromalnega raka (GIST) pri odraslih po neuspešnem zdravljenju z imatinibom zaradi odpornosti ali nestrpnosti.
Metastatski karcinom ledvičnih celic (MRCC)
Zdravilo SUTENT je indicirano za zdravljenje napredovalega / metastatskega karcinoma ledvičnih celic (MRCC) pri odraslih.
Nevroendokrini tumorji trebušne slinavke (pNET)
Zdravilo SUTENT je indicirano za zdravljenje dobro diferenciranih, neresektabilnih ali metastatskih nevroendokrinih tumorjev trebušne slinavke (pNET) pri napredujoči bolezni pri odraslih.
Izkušnje z zdravilom SUTENT kot zdravilom prve izbire so omejene (glejte poglavje 5.1).
04.2 Odmerjanje in način uporabe
Zdravljenje s sunitinibom mora uvesti zdravnik, ki ima izkušnje z dajanjem zdravil proti raku.
Odmerjanje
Pri GIST in MRCC je priporočeni odmerek zdravila SUTENT 50 mg, ki ga je treba jemati peroralno enkrat na dan, 4 zaporedne tedne, čemur sledi 2 tedna počitka (urnik 4/2), da se izvede celoten tečaj 6 tednov.
Za pNET je priporočeni odmerek zdravila SUTENT 37,5 mg, ki ga je treba jemati peroralno enkrat na dan brez načrtovanega časa počitka.
Prilagoditev odmerka
Varnost in prenašanje
Za GIST in MRCC se lahko odmerek prilagodi v korakih po 12,5 mg glede na varnost in prenašanje posameznega bolnika. Dnevni odmerek ne sme presegati 75 mg in se ne sme zmanjšati pod 25 mg.
Za pNET se lahko odmerek spremeni v korakih po 12,5 mg glede na varnost in prenašanje posameznih pacientov. Največji odmerek v študiji 3. faze pNET je bil 50 mg na dan.
Morda bo treba prekiniti vnos nekaterih odmerkov glede na varnost in prenašanje posameznega bolnika.
Zaviralci / induktorji CYP3A4
Izogibati se je treba sočasni uporabi sunitiniba z močnimi induktorji CYP3A4, kot je rifampicin (glejte poglavji 4.4 in 4.5). Če to ni mogoče, bo morda treba odmerek sunitiniba povečati v korakih po 12,5 mg (do 87,5 mg / dan za GIST in MRCC ali 62,5 mg / dan za pNET) na podlagi skrbnega spremljanja prenašanja.
Izogibati se je treba sočasni uporabi sunitiniba z močnimi zaviralci CYP3A4, kot je ketokonazol (glejte poglavji 4.4 in 4.5). Če to ni mogoče, bo na podlagi skrbnega spremljanja prenašanja morda treba odmerek sunitiniba zmanjšati na najmanjši odmerek 37,5 mg na dan za GIST in MRCC ali 25 mg na dan za pNET.
Upoštevati je treba izbiro drugega sočasnega zdravila, ki nima ali ima minimalni potencial za indukcijo ali zaviranje CYP3A4.
Posebne populacije
Pediatrična populacija
Varnost in učinkovitost sunitiniba pri bolnikih, mlajših od 18 let, nista bili ugotovljeni.
Podatki niso na voljo.
Ni indikacij za posebno uporabo sunitiniba pri otrocih od rojstva do šestega leta starosti pri zdravljenju neresektabilnega in / ali metastatskega GIST po neuspešnem zdravljenju z imatinibom zaradi odpornosti ali nestrpnosti. Ni indikacij za posebno uporabo sunitiniba pri pediatrični populaciji pri zdravljenju MRCC in pri zdravljenju dobro diferenciranih, neoperabilnih ali metastatskih pNET pri napredovanju bolezni.
Uporaba sunitiniba pri pediatrični populaciji ni priporočljiva.
Starejši bolniki (stari ≥ 65 let))
Približno tretjina bolnikov, vključenih v klinična preskušanja, ki so prejemali sunitinib, je bila stara 65 let ali več.
Okvara jeter
Pri dajanju sunitiniba pri bolnikih z blago do zmerno okvaro jeter (stopnji A in B po Child-Pughovi stopnji) začetni odmerek ni potreben. Uporaba sunitiniba pri osebah s hudo okvaro jeter (stopnja C po Child-Pughu) ni bila raziskana, zato njegova uporaba pri bolnikih z okvaro jeter ni priporočljiva (glejte poglavje 5.2).
Ledvična okvara
Pri dajanju sunitiniba pri bolnikih z okvaro ledvic (zmerno do hudo) ali končno ledvično boleznijo (ESRD) na hemodializi ni potrebno prilagajati začetnega odmerka. Naknadne prilagoditve odmerka je treba opraviti glede na varnost in prenašanje posameznega bolnika (glejte poglavje 5.2).
Način dajanja
SUTENT je za peroralno dajanje. Lahko se jemlje s hrano ali brez nje.
Če odmerka ne vzamete, dodatnega odmerka ne smete dati. Pacient mora naslednji dan vzeti običajni predpisani odmerek.
04.3 Kontraindikacije
Preobčutljivost za zdravilno učinkovino ali katero koli pomožno snov, navedeno v poglavju 6.1.
04.4 Posebna opozorila in ustrezni previdnostni ukrepi za uporabo
Izogibati se je treba sočasni uporabi z močnimi induktorji CYP3A4, saj lahko zmanjša plazemsko koncentracijo sunitiniba (glejte poglavji 4.2 in 4.5).
Izogibati se je treba sočasni uporabi z močnimi zaviralci CYP3A4, saj lahko poveča plazemsko koncentracijo sunitiniba (glejte poglavji 4.2 in 4.5).
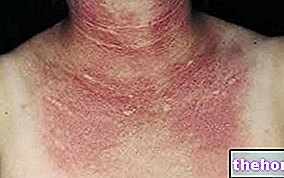
Bolezni kože in tkiva
Razbarvanje kože, ki je lahko posledica barve zdravilne učinkovine (rumene), je zelo pogost neželeni učinek, ki se pojavi pri približno 30% bolnikov. Bolnike je treba opozoriti, da lahko med zdravljenjem s sunitinibom obarvajo lase ali Lahko se pojavi tudi koža.Drugi možni dermatološki učinki lahko vključujejo suhost, odebelitev ali razpokanje kože, mehurje ali občasen izpuščaj na dlaneh ali podplatih.
Zgornje reakcije niso bile kumulativne, na splošno so bile reverzibilne in običajno niso vodile do prekinitve zdravljenja. Poročali so o primerih gangrenozne pioderme, ki je bila po prekinitvi zdravljenja na splošno reverzibilna. Poročali so o resnih kožnih reakcijah, vključno s primeri multiformnega eritema ( EM) in primeri, ki jih je mogoče pripisati Stevens-Johnsonovemu sindromu (SJS) in toksični epidermalni nekrolizi (NET), nekateri od njih so smrtni. Z znaki ali simptomi SJS, NET ali EM (npr. Kožni izpuščaj pogosto z mehurji ali lezijami sluznice) zdravljenje z Če je diagnoza SJS ali NET potrjena, se zdravljenja ne sme nadaljevati. V nekaterih primerih suma na EM so bolniki po odpravi reakcije ponovno uvedli zdravljenje s sunitinibom v manjših odmerkih, ki so jih prenašali; nekateri od teh bolnikov so prejemali tudi sočasno zdravljenje s kortikosteroidi ali antiseptiki tamini.
Krvavitve in krvavitve zaradi tumorjev
Po izkušnjah po prihodu zdravila na trg so poročali o hemoragičnih dogodkih, nekaterih s smrtnim izidom, vključno s krvavitvami iz prebavil, dihal, urina in možganov.
Do epizod krvavitve je prišlo pri 18% bolnikov, zdravljenih s sunitinibom, v primerjavi s 17% bolnikov v skupini, ki je prejemala placebo, v študiji GIST 3. faze. bolnikov, zdravljenih z IFN-α. Sedemnajst (4,5%) bolnikov, ki so prejemali sunitinib, je v primerjavi s 5 (1,7%) bolniki, ki so prejemali IFN-α, doživelo epizode krvavitve stopnje 3 ali višje. Šestindvajset odstotkov bolnikov, ki so prejemali sunitinib za odporno na citokine MRCC, je poročalo o epizodah krvavitve. Do krvavitve, razen epistaksa, je prišlo pri 21,7% bolnikov, zdravljenih s sunitinibom, v primerjavi s 9,85% bolnikov v skupini, ki je prejemala placebo, v študiji 3. faze pNET. Rutinska ocena tega dogodka mora vključevati popolno krvno sliko in fizični pregled.
Epistaksa je bila najpogostejša neželena hemoragična reakcija, o kateri so poročali pri približno polovici bolnikov s solidnimi tumorji, ki so poročali o krvavitvah. Nekatere od teh epizod epistaksije so bile resne, vendar zelo redko s smrtnim izidom.
Poročali so o krvavitvah v tumorju, včasih povezanih s tumorsko nekrozo; nekateri od teh krvavitev so bili usodni.
V kliničnih preskušanjih se je "krvavitev iz tumorja pojavila pri približno 2% bolnikov z GIST. Ti dogodki se lahko pojavijo nenadoma in se pri pljučnem raku lahko pojavijo v obliki" hude in smrtno nevarne krvavitve ali kot pljučne krvavitve.. V kliničnih preskušanjih so opazili primere pljučne krvavitve, nekatere s smrtnim izidom, poročali pa so tudi po prihodu zdravila na trg pri bolnikih, zdravljenih s sunitinibom zaradi MRCC, GIST in pljučnega raka. SUTENT ni odobren za uporabo pri bolnikih s pljučnim rakom.
Bolniki, ki se sočasno zdravijo z antikoagulanti (npr.varfarin, acenokumarol) je mogoče redno spremljati s popolno krvno sliko (trombociti), faktorji strjevanja krvi (PT / INR) in fizičnim pregledom.
Bolezni prebavil
Driska, slabost / bruhanje, bolečine v trebuhu, dispepsija in stomatitis / ustne bolečine so bili najpogosteje opisani gastrointestinalni neželeni učinki; Poročali so tudi o primerih ezofagitisa (glejte poglavje 4.8).
Podporna oskrba za gastrointestinalne neželene učinke, ki zahtevajo zdravljenje, lahko vključuje zdravila z antiemetičnimi, proti diarejo ali antacidnimi lastnostmi.
Pri bolnikih z intraabdominalno malignostjo, zdravljenih s sunitinibom, so se pojavili resni, včasih usodni prebavni zapleti, vključno s perforacijo prebavil. V študiji 3. faze GIST se je smrtna krvavitev iz prebavil pojavila pri 0,98% bolnikov, zdravljenih s placebom.
Hipertenzija
Hipertenzija je bil zelo pogost neželeni učinek, o katerem so poročali v kliničnih študijah. Odmerek sunitiniba se je zmanjšal ali je bila njegova uporaba začasno prekinjena pri približno 2,7% bolnikov, pri katerih se je pojavila hipertenzija. Pri nobenem od teh bolnikov je bilo zdravljenje s sunitinibom trajno prekinjeno. Huda hipertenzija (> 200 mmHg sistolični ali 110 mmHg diastolični) se je pojavil pri 4,7% bolnikov s solidnimi tumorji.V MRCC in predhodno nezdravljenih bolnikih so poročali o primerih hipertenzije pri 33,9% bolnikov na sunitinibu v primerjavi s 3,6% bolnikov na IFN-α. huda hipertenzija se je pojavila pri 12% predhodno nezdravljenih bolnikov v skupini s sunitinibom in pri manj kot 1% bolnikov iz skupine IFN-α. V študiji 3. faze pNET so o hipertenziji poročali pri 26,5% bolnikov, ki so jemali sunitinib, v primerjavi s 4,9% bolnikov v skupini, ki je prejemala placebo. Epizode hude hipertenzije so se pojavile pri bolnikih s pNET pri 10%. Bolnikov, zdravljenih s sunitinibom in 3% bolnike, ki se zdravijo s placebom. Bolnike je treba pregledati glede hipertenzije in jih ustrezno spremljati. Pri bolnikih s hudo nenadzorovano hipertenzijo, ki se zdravijo z zdravili, se priporoča začasna prekinitev zdravljenja. Zdravljenje se lahko nadaljuje, če je hipertenzija ustrezno nadzorovana.
Hematološke motnje
Absolutno zmanjšanje števila nevtrofilcev 3. in 4. stopnje so opazili pri 10% oziroma 1,7% bolnikov, vključenih v študijo GIST faze 3, in pri 16% oziroma 1,6% bolnikov, vključenih v študijo. Faza 3 MRCC in pri 13 % in 2,4% bolnikov, vključenih v študijo faze 3 pNET. Zmanjšanje števila trombocitov 3 in 4 stopnje so poročali pri 3,7% oziroma 0,4% bolnikov. Bolniki, vključeni v študijo GIST faze 3, pri 8,2% in 1,1% bolnikov, vključenih v študijo MRCC faze 3, ter v 3,7% in 1,2% bolnikov, vključenih v študijo faze 3 o pNET.
Zgoraj navedeni dogodki niso bili kumulativni, na splošno so bili reverzibilni in običajno niso vodili do prekinitve zdravljenja. Noben od teh dogodkov v študijah faze 3 ni bil usoden, vendar so v obdobju trženja zdravila poročali o redkih hematoloških dogodkih. vključno s krvavitvami, povezanimi s trombocitopenijo in nevtropeničnimi okužbami.
Opazili so anemijo v zgodnjih in poznih fazah zdravljenja s sunitinibom; poročali so o stopnjah 3 in 4.
Pri bolnikih, ki prejemajo sunitinib, je treba na začetku vsakega cikla zdravljenja opraviti popolno krvno sliko.
Srčne patologije
Pri bolnikih, zdravljenih s sunitinibom, so poročali o srčno -žilnih dogodkih, od katerih so bili nekateri smrtni, vključno s srčnim popuščanjem, kardiomiopatijo, miokardno ishemijo in miokardnim infarktom. Ti podatki kažejo, da sunitinib povečuje tveganje za kardiomiopatijo. Pri zdravljenih bolnikih razen specifičnega učinka zdravila niso bili ugotovljeni nobeni posebni dodatni dejavniki tveganja za kardiomiopatijo, ki jih povzroča sunitinib.
V kliničnih študijah se je zmanjšanje iztisne frakcije levega prekata (LVEF) ≥ 20% in pod spodnjo mejo normalne vrednosti pojavilo pri približno 2% bolnikov z GIST, zdravljenih s sunitinibom, pri 4% bolnikov z odpornostjo na MRCC na citokine, zdravljene s sunitinibom in pri 2 % bolnikov z GIST, ki so prejemali placebo. Zdi se, da to znižanje LVEF ni progresivno in se z nadaljevanjem zdravljenja pogosto izboljša. V študiji, izvedeni pri bolnikih z MRCC in nikoli prej zdravljenih, je 27% bolnikov, zdravljenih s sunitinibom in 15% bolnikov, zdravljenih z IFN-α, imelo vrednost LVEF pod spodnjo mejo normale. Za dva bolnika (
Pri bolnikih z GIST so epizode "srčnega popuščanja", "kongestivnega srčnega popuščanja" ali "odpovedi levega prekata" poročali pri 1,2% bolnikov, zdravljenih s sunitinibom, in pri 1% bolnikov, zdravljenih s placebom. V ključni študiji v fazi 3 na GIST (n = 312) so se srčne reakcije, povezane z zdravljenjem, pojavile pri 1% bolnikov v obeh študijah (v skupini s sunitinibom in v skupini s placebom). V študiji 2. faze bolnikov z odporno na citokine MRCC je 0,9 % bolnikov poročalo o smrtnem infarktu miokarda, povezanem z zdravljenjem, v študiji 3. faze pacientov z MRCC, ki še niso bili zdravljeni, pa 0,6 % bolnikov v kraku IFN-α in 0% bolnikov v skupini s sunitinibom je poročalo o usodnih srčnih dogodkih. V študiji 3. faze pNET je imel en bolnik (1%), ki je jemal sunitinib, srčno popuščanje, povezano s smrtjo. Možna povezava med zaviranjem receptorja tirozin kinaze (RTK) in srčno funkcijo ni jasna.
Bolniki, ki so poročali o srčnih dogodkih v 12 mesecih pred dajanjem sunitiniba, kot so miokardni infarkt (vključno s hudo / nestabilno angino pektoris), operacija koronarnega / perifernega obvoda, simptomatska CHF, cerebrovaskularni dogodek ali prehodni ishemični napad ali pljučna embolija, so bili izključeni iz klinična preskušanja s sunitinibom. Ni znano, ali je pri bolnikih s takšnimi sočasnimi stanji večje tveganje za razvoj z zdravili povezane disfunkcije levega prekata.
Treba je skrbno spremljati klinične znake in simptome kongestivnega srčnega popuščanja, zlasti pri bolnikih s srčnimi dejavniki tveganja in / ali z anamnezo bolezni koronarnih arterij.
Zdravnikom svetujemo, da to tveganje pretehtajo glede na možne koristi zdravila. Te bolnike je treba med zdravljenjem s sunitinibom skrbno spremljati glede kliničnih znakov in simptomov kongestivnega srčnega popuščanja. Pri zdravljenju s sunitinibom je treba upoštevati tudi izhodiščno in periodično oceno iztisne frakcije levega prekata. Pri bolnikih brez dejavnikov tveganja za srce je treba še vedno razmisliti o oceni iztisne frakcije prekata.
Ob prisotnosti kliničnih manifestacij CHF je priporočljivo prekiniti zdravljenje s sunitinibom. Pri bolnikih brez kliničnih znakov kongestivnega srčnega popuščanja, vendar z zmanjšanjem iztisne frakcije med 20% in 50% je treba prekiniti dajanje sunitiniba in / ali zmanjšati odmerek. od izhodišča.
Podaljšanje intervala QT
Podatki iz predkliničnih študij (in vitro In in vivo), izvedeni z odmerki, višjimi od priporočenih pri ljudeh, kažejo, da lahko sunitinib zavira procese srčne repolarizacije (npr. podaljšanje intervala QT).
Povečanje intervala QTc na več kot 500 msec se je zgodilo s hitrostjo 0,5%, spremembe od izhodišča pa za več kot 60 msec so se pojavile pri 1,1% od 450 bolnikov s solidnimi tumorji; oba parametra sta prepoznana kot potencialno pomembne spremembe. Pri koncentracijah, ki ustrezajo približno dvakrat terapevtskim koncentracijam, je bilo ugotovljeno, da sunitinib podaljšuje interval QTcF (popravljeno po Fredericini formuli).
Podaljšanje intervala QT so proučevali v študiji, v kateri je sodelovalo 24 bolnikov, starih od 20 do 87 let, z napredovalimi malignimi obolenji. zgornja meja 90% IZ = 15 msec) pri terapevtski koncentraciji (3. dan) z uporabo 24-urne korekcijske metode in pri koncentracijah nad terapevtsko (9. dan) z uporabo obeh korekcijskih metod na začetku. Noben bolnik ni poročal o vrednosti QTc> 500 msec.Čeprav je bil učinek na interval QTcF opažen 3. dan 24 ur po odmerjanju (tj. S pričakovano terapevtsko koncentracijo v plazmi po priporočenem začetnem odmerku 50 mg) s 24-urno korekcijsko metodo, klinični pomen te ugotovitve ni jasen .
Z uporabo celovitih serijskih ocen EKG, ki ustrezajo terapevtski izpostavljenosti ali izpostavljenosti nad terapevtsko, pri nobenem bolniku v populaciji, ki jo je bilo mogoče oceniti, ali ITT ni bilo opaziti podaljšanja "hudega" intervala QTc (torej enakega ali večjega od
3. stopnja CTCAE različice 3.0).
Pri terapevtskih koncentracijah v plazmi je bila povprečna največja sprememba intervala QTcF (popravljena po Fredericini formuli) od izhodišča 9,6 msek (90% IZ 15,1 msek). Pri terapevtskih koncentracijah, ki ustrezajo približno dvakratnim terapevtskim koncentracijam, je največja sprememba intervala QTcF glede na izhodiščno vrednost 15,4 msec (90% IZ 22,4 msec).
Moksifloksacin (400 mg), uporabljen kot pozitivna kontrola, je pokazal povprečno največjo spremembo intervala QTcF glede na izhodiščno vrednost 5,6 msek. Noben subjekt ni poročal o vplivu na interval QTc, večji od stopnje 2 (različica CTCAE 3.0).
Podaljšanje intervala QT lahko povzroči povečano tveganje za ventrikularne aritmije, vključno s Torsade de Pointes.
Sunitinib je treba uporabljati previdno pri bolnikih z podaljšanjem intervala QT, pri bolnikih, ki se zdravijo z antiaritmiki ali z zdravili, ki lahko podaljšajo interval QT, ali pri bolnikih z že obstoječo pomembno boleznijo srca, bradikardijo ali nepravilnostmi. Sočasno dajanje sunitiniba z močnimi zaviralci CYP3A4 je treba omejiti zaradi možnega povečanja plazemske koncentracije sunitiniba (glejte poglavji 4.2 in 4.5).
Venski trombembolični dogodki
V kliničnih študijah, vključno s študijama GIST in MRCC, so pri približno 1,0% bolnikov s solidnimi tumorji, zdravljenih s sunitinibom, opazili venske trombembolične dogodke, povezane z zdravljenjem.
V študiji GIST 3. faze je sedem bolnikov (3%), ki so prejemali sunitinib, in noben bolnik v skupini, ki je prejemala placebo, doživelo venske trombembolične dogodke; pet od sedmih bolnikov je imelo globoko vensko trombozo stopnje 3 (DVT), dva pa globoko vensko trombozo stopnje 1 ali 2. Štirje od teh sedmih bolnikov, zdravljenih zaradi GIST, so po opazovanju DVT prenehali.
Trinajst bolnikov (3%), zdravljenih s sunitinibom v študiji faze 3 MRCC in nikoli prej zdravljenih, in štirje bolniki (2%) iz dveh študij MRCC, neodpornih na citokine, so poročali o venskih trombemboličnih dogodkih. Devet od teh bolnikov je imelo venske trombembolične dogodke. A " pljučna embolija, eden z 2. stopnjo in osem s 4. stopnjo. Osem teh bolnikov je imelo DVT, eden s 1. stopnjo, dva z 2. stopnjo, štirje s 3. stopnjo in eden s 4. stopnjo. Pri bolniku s pljučno embolijo v študiji MRCC , neodzivno na citokine, je bil odmerek ustavljen.
Od predhodno nezdravljenih bolnikov z MRCC na IFN-α je šest (2%) poročalo o venskih trombemboličnih dogodkih, en bolnik (pljučna embolija, vse stopnje 4).
V študiji faze 3 pNET so pri 1 (1,2%) bolniku v skupini, ki je prejemala sunitinib, poročali o venskih trombemboličnih dogodkih in 5 (6,1%) bolnikih v skupini s placebom. Dva od teh preiskovancev, ki so prejemali placebo, sta poročali o DVT, ena stopnje 2 in ena stopnje 3.
V ključnih študijah GIST, MRCC in pNET niso opazili primerov s smrtnim izidom. V obdobju trženja zdravila so opazili primere s smrtnimi izidi (glejte dihalne dogodke in poglavje 4.8).
Arterijski trombembolični dogodki
Pri bolnikih, zdravljenih s sunitinibom, so poročali o primerih arterijskih trombemboličnih dogodkov (ATE), včasih usodnih. Najpogostejši dogodki so bili cerebrovaskularna nesreča, prehodni ishemični napad in možganska ishemija. Dejavniki tveganja, povezani z arterijskimi trombemboličnimi dogodki, so poleg že obstoječe malignosti in starosti 65 let ali več vključevali hipertenzijo, diabetes mellitus in prejšnji trombembolični dogodek.
Dihalni dogodki
Bolniki, ki so imeli v zadnjih 12 mesecih pljučno embolijo, so bili izključeni iz kliničnih preskušanj s sunitinibom.
Pri bolnikih, ki so v ključni študiji 3. faze prejemali sunitinib, so pljučne dogodke (dispnejo, plevralni izliv, pljučno embolijo ali pljučni edem) opazili pri približno 17,8% bolnikov z GIST, pri približno 26,7% bolnikov z MRCC in pri 12% bolniki s pNET.
Približno 22,2% bolnikov s solidnimi tumorji, vključno z GIST in MRCC, zdravljenih s sunitinibom v kliničnih študijah je poročalo o pljučnih dogodkih.
Primeri pljučne embolije so bili opaženi pri približno 3,1% bolnikov z GIST in približno 1,2% bolnikov z MRCC, zdravljenih s sunitinibom v študijah faze 3 (glejte poglavje 4.4. - venski trombembolični dogodki). Pri bolnikih s pNET niso opazili primerov pljučne embolije zdravljeni s sunitinibom v študiji faze 3. V obdobju trženja so opazili redke primere s smrtnim izidom (glejte poglavje 4.8).
Disfunkcija ščitnice
Priporoča se ocena delovanja ščitnice z merjenjem izhodiščnih laboratorijskih vrednosti pri vseh bolnikih. Bolnike s že obstoječim hipotiroidizmom ali hipertiroidizmom je treba pred začetkom zdravljenja s sunitinibom zdraviti v skladu s standardno klinično prakso. Med zdravljenjem s sunitinibom je treba vsake 3 mesece izvajati rutinsko preverjanje delovanja ščitnice. Poleg tega je treba vse bolnike med zdravljenjem natančno spremljati glede možnih znakov in simptomov disfunkcije ščitnice, bolnike, pri katerih se pojavijo kakršni koli znaki in / ali simptomi, ki kažejo na motnje delovanja ščitnice, pa je treba klinično pričakovati laboratorijsko testiranje delovanja ščitnice. Bolnike, pri katerih pride do disfunkcije ščitnice, je treba zdraviti v skladu s standardno klinično prakso.
Opazili so, da se na začetku ali koncu zdravljenja s sunitinibom pojavi hipotiroidizem.
O hipotiroidizmu so poročali kot o neželenem učinku pri 7 bolnikih (4%), ki so prejemali sunitinib, v dveh študijah MRCC, izvedenih pri bolnikih, neodpornih na citokine; pri 61 bolnikih (16%), ki so prejemali sunitinib, in pri treh bolnikih (
Poleg tega so pri 4 bolnikih (2%), zdravljenih zaradi MRCC, neodporne na citokine, poročali o zvišanju TSH. Na splošno je 7% populacije MRCC poročalo o kliničnih ali laboratorijskih dokazih o hipotiroidizmu, povezanem z zdravljenjem. Pridobljeni hipotiroidizem so opazili pri 6,2% bolnikov v študiji GIST, ki so jemali sunitinib, v primerjavi s 1% v skupini, ki je prejemala placebo. V študiji 3. faze pNET so o hipotiroidizmu poročali pri 6 bolnikih (7,2%), ki so prejemali sunitinib, in pri enem bolniku (1,2%), ki je prejemal placebo.
Funkcijo ščitnice smo prospektivno spremljali v dveh študijah pri bolnikih z rakom dojke; SUTENT ni odobren za zdravljenje raka dojke. V eni študiji so poročali o hipotiroidizmu pri 15 preiskovancih (13,6%), zdravljenih s sunitinibom, in pri 3 osebah (2,9%), zdravljenih s standardno terapijo. zdravimo s standardno terapijo. O hipertiroidizmu niso poročali pri nobenem od preiskovancev, zdravljenih s sunitinibom, poročali pa so pri 1 preiskovancu (1,0%), ki je prejemal standardno terapijo.V drugi študiji so o hipotiroidizmu poročali pri skupno 31 osebah (13%), zdravljenih s sunitinibom in 2 preiskovancev (0,8%), zdravljenih s kapecitabinom.Pri povečanju TSH v krvi so poročali pri 12 preiskovancih (5,0%), zdravljenih s sunitinibom, in pri nobenem preiskovancu, ki je bil zdravljen s kapecitabinom. O hipertiroidizmu so poročali pri 4 preiskovancih (1,7%), zdravljenih s sunitinibom, in pri nobenem preiskovancu, zdravljenem s kapecitabinom. Zmanjšan TSH v krvi so poročali pri 3 osebah (1,3%), zdravljenih s sunitinibom, in pri nobenem preiskovancu. Pri povečanju T4 so poročali pri 2 preiskovanca (0,8%) sta bila zdravljena s sunitinibom in pri 1 preiskovancu (0,4%), zdravljenih s kapecitabinom. Povečanje T3 so poročali pri 1 preiskovancu (0,8%), zdravljenem s sunitinibom, in pri nobenem preiskovancu, zdravljenem s kapecitabinom.Vsi poročani dogodki, povezani s ščitnico, so bili 1-2.
V kliničnih preskušanjih in v fazi trženja zdravila so občasno poročali o primerih hipertiroidizma, nekaterim je sledil hipotiroidizem in primerih tiroiditisa.
Pankreatitis
Pri bolnikih z več solidnimi tumorji, ki so prejemali sunitinib, so opazili povečanje aktivnosti lipaze in amilaze v serumu. Povečanje aktivnosti lipaze v serumu je bilo prehodno in na splošno ni bilo povezano z znaki in simptomi pankreatitisa pri osebah s solidnimi tumorji različnih vrst.
Občasno so opazili pankreatitis (
Poročali so o primerih resnih dogodkov trebušne slinavke, nekateri s smrtnim izidom.
Če se pojavijo simptomi pankreatitisa, je treba zdravljenje s sunitinibom prekiniti in bolnikom zagotoviti ustrezno podporno oskrbo. V študiji faze 3 pNET niso poročali o nobenem dogodku, povezanem z zdravljenjem pankreatitisa.
Hepatotoksičnost
Pri bolnikih, zdravljenih s sunitinibom, so opazili hepatotoksičnost. Pri jetrni funkciji so opazili primere odpovedi jeter, včasih s smrtnim izidom (alanin transaminaza [ALT], aspartat transaminaza [AST], ravni bilirubina). Znake ali simptome odpovedi jeter, Zdravljenje s sunitinibom je treba prekiniti in bolnikom zagotoviti ustrezno podporno zdravstveno oskrbo.
Bolezni jeter in žolčnika
Zdravljenje s sunitinibom je lahko povezano s holecistitisom, vključno z alitizijskim holecistitisom in entematoznim holecistitisom. V ključnih kliničnih študijah je bila incidenca holecistitisa 0,5%.
V obdobju trženja so poročali o primerih holecistitisa.
Ledvična funkcija
Poročali so o primerih okvare ledvic, odpovedi ledvic in / ali akutne odpovedi ledvic, v nekaterih primerih s smrtnim izidom.
Dejavniki tveganja, povezani z okvaro / odpovedjo ledvic pri bolnikih, ki so prejemali sunitinib, so poleg že obstoječega karcinoma ledvičnih celic vključevali: starejšo starost, diabetes mellitus, že obstoječo okvaro ledvic, srčno popuščanje, hipertenzijo, sepso, dehidracijo / hipovolemijo in rabdomiolizo.
Varnost nadaljevanja zdravljenja s sunitinibom pri bolnikih z zmerno do hudo proteinurijo ni bila sistematično ovrednotena.
Poročali so o primerih proteinurije in redkih primerih nefrotskega sindroma. Priporoča se izhodiščna analiza urina in bolnike je treba spremljati glede možnega razvoja ali poslabšanja proteinurije.
Pri bolnikih z nefrotskim sindromom je treba zdravljenje s sunitinibom prekiniti.
Fistule
Če se pojavi fistula, je treba zdravljenje s sunitinibom prekiniti. Podatki o dolgotrajnem zdravljenju s sunitinibom pri bolnikih s fistulami so omejeni.
Poslabšanje procesa celjenja ran
Med zdravljenjem s sunitinibom so poročali o primerih oslabljenega celjenja ran. Uradnih kliničnih študij o vplivu sunitiniba na celjenje ran niso izvedli. Zaradi previdnostnih razlogov je priporočljivo, da pri bolnikih na večji operaciji začasno prekinimo zdravljenje s sunitinibom. Zato mora odločitev o nadaljevanju zdravljenja s sunitinibom po večji operaciji temeljiti na klinični presoji okrevanja po operaciji.
Osteonekroza spodnje čeljusti / maksile
Pri bolnikih, zdravljenih z zdravilom SUTENT, so poročali o primerih osteonekroze čeljusti. V večini prijavljenih primerov so bili bolniki predhodno ali sočasno zdravljeni z intravenskimi bisfosfonati, pri katerih je osteonekroza čeljusti ugotovljeno tveganje.
Kot dejavnik tveganja so opredeljeni tudi invazivni zobozdravstveni posegi. Pred zdravljenjem z zdravilom SUTENT je treba pretehtati zobozdravniški pregled in ustrezno preventivno zobozdravstveno oskrbo. Če je mogoče, se je treba izogibati invazivnim zobozdravstvenim posegom pri bolnikih, ki so že jemali ali jemljejo intravenske bisfosfonate (glejte poglavje 4.8).
Preobčutljivost / angioedem
Če se zaradi preobčutljivostne reakcije pojavi edem, je treba zdravljenje s sunitinibom prekiniti in dati standardno zdravljenje.
Motnje živčnega sistema
Motnje okusa
O disgevziji so v kliničnih preskušanjih poročali pri približno 28% bolnikov, ki so prejemali sunitinib.
Konvulzije
V kliničnih preskušanjih s sunitinibom in v obdobju trženja so pri osebah z radiološkimi dokazi možganskih metastaz ali brez njih opazili epileptične napade. Poleg tega so poročali o omejenem številu poročil (glavobol, zmanjšano budnost, oslabljeno duševno funkcijo in izgubo vida, vključno s kortikalno slepoto, je treba nadzorovati z zdravljenjem, vključno z nadzorom hipertenzije. Priporoča se začasna prekinitev zdravljenja s sunitinibom; v primeru dogodka se lahko zdravljenje nadaljuje po presoji lečečega zdravnika.
Sindrom tumorske lize (TLS)
V kliničnih študijah so redko opazili primere sindroma tumorske lize (TLS), nekateri s smrtnim izidom, poročali pa so tudi po prihodu zdravila na trg pri bolnikih, zdravljenih s sunitinibom. Dejavniki tveganja za TLS vključujejo visoko tumorsko obremenitev, že obstoječo kronično ledvično odpoved, oligurijo, dehidracijo, hipotenzijo in kisli urin. Te bolnike je treba skrbno spremljati in zdraviti, kot je klinično indicirano; pri teh bolnikih je treba upoštevati profilaktično hidracijo.
Okužbe
Poročali so o primerih resnih okužb z nevtropenijo ali brez nje, vključno z nekaterimi primeri s smrtnim izidom.
Okužbe, ki jih pri zdravljenju s sunitinibom najpogosteje opazimo, so okužbe, značilne za bolnika z rakom, kot so dihala, sečila, koža in sepsa.
Poročali so o redkih, včasih usodnih primerih nekrotizirajočega fasciitisa, vključno s presredkom. Pri bolnikih, pri katerih se pojavi nekrotizirajoči fasciitis, je treba zdravljenje s sunitinibom prekiniti in takoj začeti ustrezno zdravljenje.
Hipoglikemija
Med zdravljenjem s sunitinibom so poročali o znižanju glukoze v krvi, nekateri klinično simptomatični in zaradi izgube zavesti potrebujejo hospitalizacijo. V primeru simptomatske hipoglikemije je treba zdravljenje s sunitinibom začasno prekiniti. Pri bolnikih s sladkorno boleznijo je treba redno preverjati raven glukoze v krvi, da se oceni, ali je treba odmerek zdravil za sladkorno bolezen prilagoditi, da se zmanjša tveganje za hipoglikemijo.
04.5 Interakcije z drugimi zdravili in druge oblike interakcij
Študije interakcij so bile izvedene samo pri odraslih.
Zdravila, ki lahko povečati plazemske koncentracije sunitiniba
Pri zdravih prostovoljcih je sočasna uporaba enkratnega odmerka sunitiniba s ketokonazolom, močnim zaviralcem CYP3A4, povzročila povečanje skupne Cmax [sunitinib + primarni presnovek] Cmax in AUC0-∞ za 49% oziroma 51%.
Uporaba sunitiniba z močnimi zaviralci CYP3A4 (npr. Ritonavirjem) , itrakonazol, eritromicin, klaritromicin, grenivkin sok) lahko povečajo koncentracije sunitiniba.
Zato se je treba izogibati kombinaciji z zaviralci CYP3A4 ali razmisliti o alternativnem zdravilu, ki nima ali ima minimalni potencial za zaviranje CYP3A4.
Če to ni mogoče, bo morda treba na podlagi skrbnega spremljanja prenašanja odmerek zdravila SUTENT zmanjšati na najmanj 37,5 mg / dan za GIST in MRCC ali 25 mg / dan za pNET (glejte poglavje 4.2).
Zdravila, ki lahko zmanjšati plazemske koncentracije sunitiniba
Pri zdravih prostovoljcih je sočasna uporaba enkratnega odmerka sunitiniba in induktorja CYP3A4 rifampicina povzročila zmanjšanje kombinirane Cmax [sunitinib + primarni presnovek] Cmax in AUC0-∞ za 23% oziroma 46%.
Uporaba sunitiniba z močnimi induktorji CYP3A4 (npr. Deksametazonom, fenitoinom, karbamazepinom, rifampicinom, fenobarbitalom ali zeliščnimi pripravki, ki vsebujejo šentjanževko)Hypericum perforatum) lahko zmanjša koncentracijo sunitiniba. Zato se je treba izogniti povezavi z induktorji CYP3A4 ali razmisliti o alternativnem zdravilu, ki nima ali ima minimalni potencial za indukcijo CYP3A4. Če to ni mogoče, se lahko odmerek zdravila SUTENT poveča za 12, 5 mg (navzgor). do 87,5 mg / dan za GIST in MRCC ali 62,5 mg / dan za pNET) na podlagi skrbnega spremljanja prenašanja (glejte poglavje 4.2).
04.6 Nosečnost in dojenje
Nosečnost
Študije pri nosečnicah, ki so prejemale sunitinib, niso bile izvedene. Študije na živalih so pokazale reproduktivno toksičnost, vključno z malformacijami ploda (glejte poglavje 5.3).
Zdravila SUTENT se ne sme uporabljati med nosečnostjo ali pri ženskah, ki ne uporabljajo učinkovitih kontracepcijskih sredstev, razen če možne koristi upravičujejo možno tveganje za plod. Če se zdravilo SUTENT uporablja med nosečnostjo ali če bolnica med zdravljenjem z zdravilom SUTENT zanosi, je treba bolnika obvestiti o možnih tveganjih za plod.
Ženskam v rodni dobi je treba svetovati, naj uporabljajo učinkovito kontracepcijo in naj se med zdravljenjem z zdravilom SUTENT izognejo zanositvi.
Čas hranjenja
Sunitinib in / ali njegovi presnovki se izločajo v mleko podgan. Ni znano, ali se sunitinib ali njegov glavni aktivni presnovek izloča v materino mleko. Ker se učinkovine na splošno izločajo v materino mleko in glede na možne resne neželene učinke pri dojenčkih, ženske med zdravljenjem z zdravilom SUTENT ne smejo dojiti.
Plodnost
Predklinični podatki kažejo, da bi lahko pri zdravljenju s sunitinibom plodnost moških in žensk poslabšala (glejte poglavje 5.3).
04.7 Vpliv na sposobnost vožnje in upravljanja s stroji
Študije o vplivu na sposobnost vožnje in upravljanja s stroji niso bile izvedene, bolnike je treba obvestiti o možnem pojavu omotice med zdravljenjem s sunitinibom.
04.8 Neželeni učinki
Povzetek varnostnega profila
Najresnejši neželeni učinki, povezani s zdravljenjem s sunitinibom, nekateri smrtni, so odpoved ledvic, srčno popuščanje, pljučna embolija, perforacija prebavil in krvavitve (npr.
Najpogostejši neželeni učinki katere koli stopnje (o katerih so poročali bolniki v ključnih kliničnih preskušanjih za RCC, GIST in pNET) so vključevali zmanjšan apetit, motnje okusa, hipertenzijo, utrujenost, prebavne motnje (npr. Drisko, slabost, stomatitis, dispepsijo in bruhanje), razbarvanje. sindroma kože in palmarno-plantarne eritrodisestezije. Ti simptomi se lahko z nadaljevanjem zdravljenja zmanjšajo. Med zdravljenjem se lahko pojavi hipotiroidizem. Hematološke motnje (npr. Nevtropenija, trombocitopenija in anemija) so bile med najpogostejšimi neželenimi učinki zdravila.
Smrtni neželeni učinki, ki niso navedeni v poglavju 4.4. ali v poglavju 4.8, za katerega velja, da je morda povezan s sunitinibom, vključujejo odpoved več organov, razširjeno intravaskularno koagulacijo, peritonealno krvavitev, insuficienco nadledvične žleze, pnevmotoraks, šok in nenadno smrt.
Tabela neželenih učinkov
Neželeni učinki, o katerih so poročali bolniki z GIST, MRCC in pNET v združenem naboru podatkov 7115 bolnikov, so navedeni spodaj in so razvrščeni po organskih sistemih, pogostnosti in resnosti (NCI-CTCAE). Poročali so tudi o neželenih učinkih po trženju, ugotovljenih v kliničnih študijah. V vsakem razredu pogostnosti se o neželenih učinkih poroča po padajoči resnosti.
Pogostnosti so opredeljene na naslednji način: zelo pogosti (≥1 / 10), pogosti (≥1 / 100a
Preglednica 1 - Neželeni učinki, o katerih so poročali v kliničnih študijah
Naslednji izrazi so združeni:
nazofaringitis in oralni herpes
b Bronhitis, okužba spodnjih dihal, pljučnica in okužba dihal
c Absces, absces okončin, analni absces, absces dlesni, jetrni absces, absces trebušne slinavke, perinealni absces, perirektalni absces, rektalni absces, podkožni absces in zobni absces
d Kandidiaza požiralnika in ustna kandidiaza
ter celulitis in kožna okužba
f Sepsa in septični šok
g Trebušni absces, trebušna sepsa, divertikulitis in osteomielitis
h Zmanjšan apetit in anoreksija
i disgevzija, starost in sprememba okusa
j Akutni koronarni sindrom, angina pektoris, nestabilna angina, okluzija koronarne arterije, miokardna ishemija
k Zmanjšanje / anomalija izmetne frakcije
l Akutni miokardni infarkt, miokardni infarkt, tihi miokardni infarkt
m Bolečine v žrelu in žrelu
n Stomatitis in aftozni stomatitis
o Bolečine v trebuhu, bolečine v spodnjem in zgornjem delu trebuha
p Perforacija prebavil in črevesja
q Holecistitis in alitski holecistitis
r Rumena koža, spremembe barve kože in pigmentacije
s psoriaziformni dermatitis, eksfoliativni izpuščaj, izpuščaj, eritematozni izpuščaj, folikularni izpuščaj, generaliziran izpuščaj, makularni izpuščaj, makulopapularni izpuščaj, papularni izpuščaj in srbeč izpuščaj
t Kožna reakcija in kožna patologija
u Patologija nohtov in razbarvanje nohtov
v Utrujenost in astenija
w Edem obraza, edem in periferni edem
x amilaze in povečane amilaze
* Vključuje usodne dogodke
Opis ugotovljenih neželenih učinkov
Okužbe in okužbe: Poročali so o primerih resnih okužb (z nevtropenijo ali brez nje), vključno s primeri s smrtnim izidom. Poročali so o primerih nekrotizirajočega fasciitisa, včasih s smrtnim izidom, ki bi lahko vplival tudi na območje presredka (glejte tudi poglavje 4.4).
Motnje krvnega in limfnega sistema: Poročali so o primerih trombotične mikroangiopatije. V teh primerih se priporoča začasna prekinitev uporabe zdravila SUTENT; po odpravi teh dogodkov se lahko zdravljenje po presoji zdravnika ponovno zažene.
Bolezni imunskega sistema: Poročali so o preobčutljivostnih reakcijah, vključno z angioedemom.
Bolezni živčevja: Poročali so o nekaj primerih, nekaj smrtnih, pri osebah z napadi in radiološkimi dokazi o sindromu reverzibilne posteriorne levkoencefalopatije (RPLS) (glejte tudi poglavje 4.4).
Presnovne in prehranske motnje: Pri bolnikih s pNET so poročali o večji pojavnosti hipoglikemičnih dogodkov v primerjavi z bolniki z MRCC in GIST. Vendar se za številne neželene učinke, opažene v kliničnih preskušanjih, ni štelo, da so povezani s študijskim zdravljenjem.
Bolezni jeter in žolčnika: Poročali so o disfunkciji jeter, ki lahko vključuje nenormalnosti testov delovanja jeter, hepatitis ali odpoved jeter.
Bolezni kože in podkožja: Poročali so o primerih gangrenozne pioderme, ki je bila po prekinitvi zdravljenja na splošno reverzibilna (glejte tudi poglavje 4.4).
Bolezni mišično -skeletnega sistema in vezivnega tkiva: Poročali so o primerih miopatije in / ali rabdomiolize, nekaterih povezanih z akutno odpovedjo ledvic. Bolnike, ki imajo znake ali simptome mišične toksičnosti, je treba zdraviti v skladu s standardno medicinsko prakso.
Poročali so o primerih nastanka fistule, včasih povezane s tumorsko nekrozo in regresijo, v nekaterih primerih s smrtnim izidom.
Pri bolnikih, zdravljenih z zdravilom SUTENT, so poročali o primerih osteonekroze čeljusti, od katerih so se številni pojavili pri bolnikih, ki so prepoznali dejavnike tveganja za osteonekrozo čeljusti, zlasti izpostavljenost intravenskim bisfosfonatom in / ali zgodovino zobne bolezni, ki zahteva invazivne zobozdravstvene posege (glejte tudi poglavje 4.4).
Poročanje o domnevnih neželenih učinkih
Poročanje o domnevnih neželenih učinkih, ki se pojavijo po odobritvi zdravila, je pomembno, saj omogoča stalno spremljanje razmerja med koristmi in tveganji zdravila. Zdravstvene delavce prosimo, da o vsakem sumu na neželene učinke poročajo prek nacionalnega sistema za poročanje. V "Prilogi V .
04.9 Preveliko odmerjanje
Za preveliko odmerjanje sunitiniba ni posebnega protistrupa in zdravljenje prevelikega odmerjanja mora vključevati splošne podporne ukrepe. Če je indicirano, lahko izločanje neabsorbirane učinkovine dosežemo s bruhanjem ali izpiranjem želodca. Opisani so bili primeri prevelikega odmerjanja; v nekaterih primerih v teh primerih so se neželeni učinki pojavili v skladu z znanim varnostnim profilom sunitiniba.
05.0 FARMAKOLOŠKE LASTNOSTI
05.1 Farmakodinamične lastnosti
Farmakoterapevtska skupina: zdravila proti raku, zaviralci proteinske kinaze.
Oznaka ATC: LO1XE04.
Mehanizem delovanja
Sunitinib zavira več receptorjev tirozin kinaze (RTK), ki sodelujejo pri rasti tumorjev, neoangiogenezi tumorja in metastatskem napredovanju raka. Sunitinib je bil identificiran kot zaviralec receptorjev rastnega faktorja, pridobljenega iz trombocitov (PDGFRα in PDGFRβ), receptorjev vaskularnega endotelijskega rastnega faktorja (VEGFR1, VEGFR2 in VEGFR3), receptorja faktorja matičnih celic (KIT), receptorja tirozin kinaze FLT3 (Fms podobno tirozin kinaza 3), receptor CSF-1R (receptor faktorja, ki stimulira kolonije (CSF-1R)) in receptor za nevtrofni faktor, pridobljen iz glije (RET). Glavni presnovek ima v biokemičnih in celičnih testih moč, ki je primerljiva z močjo sunitiniba.
Klinična učinkovitost in varnost
Varnost in klinično učinkovitost sunitiniba so preučevali pri zdravljenju bolnikov z GIST, odpornim na imatinib (tj. Tistih bolnikov, ki so napredovali med zdravljenjem z imatinibom ali po njem) ali intolerance na imatinib (tj. Tistih, ki so imeli med zdravljenjem z imatinibom pomembno toksičnost ki so preprečevali nadaljevanje zdravljenja), pri zdravljenju bolnikov z MRCC in pri zdravljenju bolnikov z neoperabilnim pNET.
Učinkovitost temelji na času do napredovanja tumorja in povečanju preživetja pri bolnikih z GIST, preživetja brez napredovanja bolezni in objektivne stopnje odziva pri predhodno nezdravljenih bolnikih z MRCC oziroma MRCC, neodzivnih na zdravljenje z citokini MRCC, in na preživetju brez napredovanja bolezni pri bolnikih s pNET -om.
Stromalni tumorji prebavil (GIST)
Začetna odprta stopnjujoča študija je bila izvedena pri bolnikih z GIST po odpovedi imatiniba (mediani največjega dnevnega odmerka 800 mg) zaradi odpornosti ali intolerance. Vpisanih je bilo 97 bolnikov z različnimi odmerki in režimi odmerjanja; 55 bolnikov je bilo zdravljenih s 50 mg zdravila SUTENT v skladu s priporočenim 4-tedenskim režimom zdravljenja in dvotedenskim odvzemom zdravil (urnik 4/2).
V tej študiji je bil mediani čas do napredovanja TTP 34,0 tedna (95% IZ = 22,0-46,0 tednov).
Naključno, dvojno slepo, s placebom kontrolirano študijo 3. faze sunitiniba so izvedli pri bolnikih z GIST, ki niso prenašali ali so med zdravljenjem z imatinibom ali po njem napredovali (mediana največjega dnevnega odmerka 800 mg). V tej študiji je bilo 312 bolnikov (2: 1) naključno izbranih za zdravljenje s 50 mg sunitiniba ali placeba, peroralno enkrat na dan po razporedu 4/2 do napredovanja bolezni ali izstopa iz študije iz drugega razloga (207 bolnikov je prejelo sunitinib in 105 placebo).
Primarni cilj študije je bil TTP, opredeljen kot čas od randomizacije do prve dokumentacije o objektivnem napredovanju tumorja. V času vnaprej določene vmesne analize je bil mediani TTP s sunitinibom 28,9 tedna (95% IZ = 21,3-34,1 tedna). ), ko ga je ocenil raziskovalec, in 27,3 tedna (95% IZ = 16,0-32,1 tedna), ko ga je ocenil neodvisni revizijski odbor in je bil statistično boljši od 5,1-tedenskega TTP, pridobljenega s placebom (95% IZ = 4,4-10,1 tedna, str
Neodvisna revizijska komisija. Razlika v skupnem preživetju je bila statistično v prid sunitinibu [razmerje nevarnosti0,491 95% (CI 0,290-0,831)]; tveganje smrti je bilo pri bolnikih v skupini, ki je prejemala placebo, 2 -krat večje kot pri tistih v skupini, ki je prejemala sunitinib.
Po vmesni analizi učinkovitosti in varnosti je bila študija na priporočilo neodvisnega DSMB slepa in bolnikom v skupini, ki je prejemala placebo, je bilo ponujeno, da preide na odprto zdravljenje s sunitinibom.
V odprti fazi študije je bilo s sunitinibom zdravljenih 255 bolnikov, od tega 99 bolnikov, ki so bili na začetku zdravljeni s placebom.
Analiza primarnih in sekundarnih končnih točk v odprti fazi študije je ponovno potrdila rezultate, pridobljene v času vmesne analize, kot je prikazano v spodnji tabeli.
Tabela 2 - Povzetek končnih točk učinkovitosti (populacija ITT)
Mediana celotnega preživetja (OS) v populaciji ITT je bila 72,7 tedna oziroma 64,9 tedna (HR 0,876, 95% IZ 0,679 - 1,129, p = 0,306) v skupini, ki je prejemala sunitinib, in skupini, ki je prejemala placebo. V tej analizi je skupina s placebom vključevala tiste bolnike, ki so bili randomizirani na placebo in so nato prešli na odprto zdravljenje s sunitinibom.
Metastatski karcinom ledvičnih celic (MRCC) pri predhodno nezdravljenih bolnikih
Za oceno učinkovitosti in varnosti sunitiniba v primerjavi z interferonom IFN-α pri predhodno nezdravljenih bolnikih z MRCC je bila izvedena randomizirana, multicentrična, mednarodna študija 3. faze. ponavljajočih se 6-tedenskih ciklov. Vsak cikel je sestavljen iz 4 tednov s 50 mg na dan peroralno, čemur sledijo 2 tedna brez jemanja zdravila (shema 4/2) ali s peroralno subkutano uporabo IFN-α v odmerku 3 milijone enot (MU ) prvi teden, 6 MU drugi teden in od tretjega tedna dalje v odmerku 9 MU glede na zdravljenje 3 zaporedne dni vsak teden.
Povprečno trajanje zdravljenja je bilo 11,1 meseca (razpon: 0,4 - 46,1) za zdravljenje s sunitinibom in 4,1 meseca (razpon 0,1 - 45,6) za zdravljenje z IFN -α. O resnih neželenih učinkih, povezanih z zdravljenjem (TRSAE), so poročali pri 23,7% bolnikov, ki so prejemali sunitinib, in pri 6,9% bolnikov, ki so prejemali IFN-α. Vendar pa je bila stopnja prekinitve zaradi neželenih učinkov 20% pri sunitinibu in 23% pri IFN-α. Prekinitev zdravljenja je bila pri 202 bolnikih (54%) v skupini, ki je prejemala sunitinib, in pri 141 bolnikih (39%) v skupini, ki je prejemala IFN-α.
Do zmanjšanja odmerka je prišlo pri 194 bolnikih (52%), zdravljenih s sunitinibom, in 98 bolnikih (27%), zdravljenih z IFN-α. Bolnike so zdravili do napredovanja bolezni ali umika študije. Primarni cilj učinkovitosti je bilo preživetje brez napredovanja bolezni (PFS).
Načrtovana vmesna analiza je pokazala statistično pomembno prednost za SUTENT pred IFN-α. V tej študiji je bila mediana PFS za skupino sunitiniba 47,3 tedna v primerjavi s 22,0 tedna za skupino IFN-α; razmerje nevarnosti je bilo 0,415 (95% IZ: 0,320-0,539, p-vrednost
Zdravljenje s sunitinibom je bilo povezano z daljšim preživetjem kot zdravljenje z IFN-α. Mediana celotnega preživetja je bila 114,6 tedna za skupino sunitiniba (95% IZ: 100,1 - 142,9 tedna) in 94,9 tedna za skupino IFN -α (95% IZ: 77,7 - 117,0 tednov) z razmerje nevarnosti 0,821 (95% IZ: 0,673-1,001; p = 0,0510 na podlagi testa nestratificiranega log-ranga).
Preživetje brez napredovanja bolezni (PFS) in splošno preživetje (OS), opaženo pri namenu zdravljenja (ITT) populacije in določeno z radiološko laboratorijsko oceno, sta povzeti v naslednjih tabelah:
Povzetek končnih točk učinkovitosti (populacija ITT)
Metastatski karcinom ledvičnih celic, odporen na citokine (MRCC)
Študija 2. faze je bila izvedena z zdravilom SUTENT pri bolnikih, ki niso bili odporni na predhodno zdravljenje s citokini, zdravljeni z interlevkinom-2 ali IFN-α. Triinštirideset bolnikov je prejelo peroralni začetni odmerek 50 mg sunitiniba enkrat na dan 4 zaporedne tedne, čemur je sledil 2-tedenski počitek za dokončanje celotnega 6-tedenskega tečaja (shema zdravljenja 4/2). Primarna končna točka učinkovitosti je bila objektivna stopnja odziva (Objektivno
Stopnja odziva (ORR)) v skladu z merili RECIST (Merila za oceno odziva pri trdnih tumorjih).
V tej študiji je bila objektivna stopnja odziva 36,5% (95% IZ 24,7% -49,6%), mediana časa do napredovanja (TTP) pa 37,7 tedna (95% IZ 24,0-46,4 tedna).
Odprta, multicentrična, potrditvena študija z eno roko, ki je ocenila učinkovitost in varnost sunitiniba, je bila izvedena pri bolnikih z MRCC, neodzivno na predhodno zdravljenje s citokini. Sto šest bolnikov je prejelo vsaj en odmerek 50 sunitiniba v mg okvir sheme 4/2.
Primarni cilj učinkovitosti te študije je bila stopnja ORR, sekundarni cilji pa so bili TTP, trajanje odziva (DR) in splošno preživetje (OS).
V tej študiji je bil ORR 35,8% (95% IZ 26,8% -47,5%). DR in mediana OS še nista bila dosežena.
Nevroendokrini tumorji trebušne slinavke (pNET)
Odprta, multicentrična, podporna študija druge faze je ocenila učinkovitost in varnost monoterapije s sunitinibom pri 50 mg dnevnih odmerkih po razporedu 4/2 [4 tedne zdravljenja, 2 tedna počitka] pri bolnikih z neoperabilnim pNET v skupini 66 pri bolnikih z rakom otočkov trebušne slinavke je bil primarni cilj odziva 17%.
Izvedena je bila osrednja, multicentrična, mednarodna, randomizirana, dvojno slepa, s placebom nadzorovana študija monoterapije s sunitinibom v fazi 3 pri bolnikih z neoperabilnim pNET.
Bolniki, pri katerih je bilo treba v zadnjih 12 mesecih dokumentirati napredovanje bolezni na podlagi RECIST, so bili naključno izbrani (1: 1), da so prejemali 37,5 mg sunitiniba enkrat na dan brez predvidene karence (n = 86) ali placeba (n = 85) .
Primarni cilj je bila ocena preživetja brez napredovanja bolezni (PFS) pri bolnikih, ki so prejemali sunitinib, v primerjavi s tistimi, ki so prejemali placebo. Drugi cilji so bili OS, odstotek ORR, rezultati, o katerih so poročali bolniki) in varnost.
Z vidika demografskih značilnosti so bile skupine bolnikov, zdravljenih s sunitinibom in placebom, primerljive.Poleg tega je 49% bolnikov, zdravljenih s sunitinibom, in 52% bolnikov, ki so prejemali placebo, imelo nefunkcionalne tumorje, 92% bolnikov na obeh rokah pa je imelo metastaze v jetrih. Študija je dovoljevala uporabo analogov somatostatina. 66% bolnikov, zdravljenih s sunitinibom in 72% bolnikov, zdravljenih s placebom, je bilo predhodno zdravljenih s sistemsko terapijo. Poleg tega je bilo 24% bolnikov v skupini, ki je prejemalo sunitinib, in 22% bolnikov, ki so prejemali placebo. skupina je prejemala analoge somatostatina. Klinično pomembna prednost sunitinib PFS v primerjavi s placebom je bila opažena pri oceni raziskovalca. Mediana PFS je bila v skupini s sunitinibom 11,4 meseca v primerjavi s 5,5 meseca v skupini s placebom [razmerje nevarnosti: 0,418 (95% IZ 0,263 , 0,662), p-vrednost = 0,0001]; podobni rezultati so bili opaženi, ko so bile za ugotavljanje napredovanja bolezni, kot je prikazano v tabeli 3., uporabljene ocene odziva tumorja, ki temeljijo na uporabi RECIST pri meritvah tumorja, ki so jih izvedli raziskovalci. razmerje nevarnosti v korist sunitiniba so opazili v vseh podskupinah, ocenjenih glede na izhodiščne značilnosti, vključno z analizo po številu predhodnih sistemskih terapij. Skupaj 29 bolnikov v skupini, ki je prejemala sunitinib, in 24 v skupini, ki je prejemala placebo, niso prejemali predhodnih sistemskih terapij; pri teh bolnikih ni bilo "razmerje nevarnosti za PFS je bilo 0,365 (95% IZ 0,156, 0,857), p = 0,0156.
Podobno je bilo med 57 bolniki v skupini, ki je prejemala sunitinib (od tega 28 pri enem predhodnem sistemskem zdravljenju in 29 pri dveh ali več sistemskih terapijah) in 61 bolnikov v skupini, ki je prejemala placebo (od tega 25 pri 1 predhodni sistemski terapiji in 36 pri 2 ali več sistemskih terapijah) ) l "razmerje nevarnosti za PFS je bilo 0,456 (95% IZ 0,264, 0,787), p = 0,0036.
Analiza občutljivosti PFS je bila izvedena, ko je PFS temeljil na meritvah raziskovalca tumorja in ko so se za vse subjekte, ki so bili cenzurirani zaradi razlogov, ki niso bili zaključeni, šteli dogodki PFS. Ta analiza je dala konzervativno oceno učinka zdravljenja s sunitinibom in potrdila primarno analizo, ki je pokazala "razmerje nevarnosti 0,507 (95% IZ, 0,350, 0,733), p = 0,000193. Ključna študija v sistemu PET trebušne slinavke je bila predčasno zaključena na podlagi priporočila neodvisne komisije za ocenjevanje zdravil, primarna končna točka pa je temeljila na oceni raziskovalca: oba stanja sta lahko vplivala na oceno učinka zdravljenja.
Da bi izključili pristranskost pri presoji raziskovalcev o PFS, je bil opravljen neodvisen, slep osrednji pregled diagnostičnega slikanja; ta pregled je podprl oceno raziskovalca, kot je prikazano v tabeli 3.
Tabela 3 - Rezultati učinkovitosti študije faze 3 pNET
CI = interval zaupanja, HR = razmerje nevarnosti, NA = se ne uporablja, NR = ni doseženo
dvostranski nestratificiran preskus log-rank
b Fisherjev natančen test
Celotna številka preživetja med izvedbo analize ni bila zrela. V skupini, ki je prejemala sunitinib, je bilo 9 smrtnih primerov, v skupini s placebom pa 21 smrtnih primerov. V objektivni stopnji odziva na sunitinib so opazili statistično pomembno razliko v primerjavi s placebom.
V primeru napredovanja bolezni so bili bolniki obveščeni o zdravljenju, ki so ga prejemali, bolnikom, ki so prejemali placebo, pa je bila ponujena možnost, da se vključijo v drugo odprto podaljšano študijo s sunitinibom. Zaradi zgodnjega zaključka študije so bili preostali bolniki obveščeni o zdravljenju, ki so ga prejemali, in jim je bil na voljo dostop do odprte razširitvene študije s sunitinibom. podaljšanja.
Rezultati vprašalnika o kakovosti življenja Evropske organizacije za raziskave in zdravljenje raka (EORTC QLQ-C30) so pokazali, da je splošna zdravstvena kakovost življenja in pet funkcionalnih področij (fizično, vlogo, kognitivno, čustveno in socialni) so bili pri bolnikih, ki so prejemali sunitinib, v primerjavi s tistimi, ki so prejemali placebo, ohranjeni z malo simptomatskimi stranskimi učinki.
Pediatrična populacija
Evropska agencija za zdravila je odložila obveznost predložitve rezultatov študij z zdravilom SUTENT v eni ali več podskupinah pediatrične populacije za zdravljenje GIST (za informacije o pediatrični uporabi glejte poglavje 4.2).
Evropska agencija za zdravila se je odpovedala obveznosti predložitve rezultatov študij z zdravilom SUTENT v vseh podskupinah pediatrične populacije za zdravljenje ledvičnih in ledvičnih karcinomov medenice (z izključitvijo nefroblastoma, nefroblastomatoze, jasnih celic sarkoma, mezoblastnega nefroma, ledvične medule) karcinom in rabdoidni tumor ledvic) (za informacije o pediatrični uporabi glejte poglavje 4.2).
Evropska agencija za zdravila se je odpovedala obveznosti predložitve rezultatov študij z zdravilom SUTENT v vseh podskupinah pediatrične populacije za zdravljenje gastroenteropankreatičnih nevroendokrinih tumorjev (z izključitvijo nevroblastoma, nevroganglioblastoma, feokromocitoma) (za informacije o uporabi pri otrocih glejte poglavje 4.2 ).
05.2 "Farmakokinetične lastnosti
Farmakokinetiko sunitiniba so ocenjevali pri 135 zdravih prostovoljcih in pri 266 bolnikih s solidnimi tumorji. Farmakokinetika je bila pri vseh testiranih populacijah solidnih tumorjev in pri zdravih prostovoljcih podobna.
V shemah odmerjanja 25-100 mg se površina pod krivuljo (AUC) in Cmax povečata sorazmerno z odmerkom. Ob ponavljajočem se dnevnem dajanju se sunitinib kopiči 3-4 krat, glavni aktivni presnovek pa 7-10 krat. Koncentracije sunitiniba in njegovega glavnega aktivnega presnovka v stanju dinamičnega ravnovesja so dosežene v 10-14 dneh. Do 14. dne so skupne plazemske koncentracije sunitiniba in njegovega glavnega aktivnega presnovka 62,9 - 101 ng / ml in predstavljajo predvidene ciljne koncentracije, ki temeljijo na predkliničnih podatkih za zaviranje fosforilacije receptorjev. in vitro in vodijo do zmanjšanja zastoja / rasti tumorja in vivo.
Glavni aktivni presnovek predstavlja 23-37% celotne izpostavljenosti zdravilu. Pri ponavljajočih se enkrat na dan ali ponavljajočih se tečajih pri preskušenih režimih odmerjanja niso opazili pomembnih sprememb v farmakokinetiki sunitiniba ali glavnega aktivnega presnovka.
Absorpcija
Po peroralnem dajanju sunitiniba največje koncentracije (Cmax) običajno opazimo v 6-12 urah (Tmax) po zaužitju zdravila.
Hrana nima vpliva na biološko uporabnost sunitiniba.
Distribucija
V preskusih se vezava sunitiniba in njegovega glavnega aktivnega presnovka na beljakovine človeške plazme v vitro teh je bilo 95% oziroma 90% brez očitne odvisnosti od koncentracije.
Navidezni volumen porazdelitve (Vd) sunitiniba je bil velik - 2.230 l - kar kaže na porazdelitev v tkiva.
Presnovne interakcije
Izračunane vrednosti Ki in vitro za vse pregledane izoforme citokroma (CYP) (CYP1A2, CYP2A6, CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP2D6, CYP2E1, CYP3A4 / 5 in CYP4A9 / 11) je malo verjetno, da bi sunitinib in njegov pomemben aktivni metabolit a presnovo drugih učinkovin, ki jih lahko presnavljajo ti encimi.
Biotransformacija
Sunitinib se presnavlja predvsem s CYP3A4, izoformo citokroma P450, ki proizvaja njegov glavni aktivni presnovek, desetil sunitinib, ki ga ta isti izoencim nadalje presnavlja.
Izogibati se je treba sočasni uporabi sunitiniba in močnih induktorjev ali zaviralcev CYP3A4, ker se lahko koncentracija sunitiniba v plazmi spremeni (glejte poglavji 4.4 in 4.5).
Odprava
Izloča se predvsem z blatom (61%), ledvica pa izloči nespremenjeno učinkovino in njene presnovke 16% uporabljenega odmerka.Sunitinib in njegov glavni aktivni presnovek sta bili glavni spojini, ugotovljeni v plazmi, urinu in blatu ter predstavljali 91,5%, 86,4%oziroma 73,8%radioaktivnosti, odkrite v združenih vzorcih. Manjši presnovki so bili ugotovljeni v urinu in blatu, običajno pa v plazmi niso zaznani. Skupni peroralni očistek (CL / F) je bil 34-62 L / h.
Po peroralni uporabi pri zdravih prostovoljcih je razpolovni čas izločanja sunitiniba in njegovega glavnega aktivnega presnovka desetila približno 40-60 ur oziroma 80-110 ur.
Posebne populacije
Okvara jeter: Sunitinib in njegov glavni presnovek se presnavljajo predvsem v jetrih. Sistemska izpostavljenost po enkratnem odmerku sunitiniba je bila podobna pri osebah z blago ali zmerno okvaro jeter (stopnji A in B po Child-Pughu) v primerjavi z osebami z normalnim delovanjem jeter. Zdravila SUTENT niso preučevali pri osebah s hudo okvaro jeter (stopnja C po Child-Pughu).
Študije raka so izključile bolnike z ALT ali AST> 2,5 x ZMN (zgornja meja normale) ali če so bile te vrednosti> 5,0 x ZMN zaradi jetrnih metastaz.
Ledvična okvara: Populacijske farmakokinetične analize so pokazale, da očistek kreatinina v obravnavanem razponu (42-347 ml / min) ni vplival na očistek sunitiniba (CL / F). Sistemska izpostavljenost po enem samem odmerku sunitiniba je bila pri osebah s hudo okvaro ledvic podobna ( CLcr80 ml / min) Čeprav se pri osebah z ESRD sunitinib in njegov glavni presnovek pri hemodializi nista očistila, je bila skupna sistemska izpostavljenost sunitinibu za 47% nižja, pri njegovem glavnem presnovku pa za 31%.
Teža, stanje zmogljivosti: Farmakokinetične analize prebivalstva kažejo, da za težo in stanje uspešnosti Vzhodne zadružne onkološke skupine (ECOG) niso potrebne prilagoditve začetnega odmerka.
Spol pripadnosti: Razpoložljivi podatki kažejo, da imajo lahko samice 30% manjši navidezni očistek sunitiniba (CL / F) kot samci; ta razlika pa ne zahteva prilagoditve začetnega odmerka.
05.3 Predklinični podatki o varnosti
Študije toksičnosti pri ponavljajočih se odmerkih pri podganah in opicah, ki so trajale do 9 mesecev, so pokazale, da so glavni učinki na ciljne organe v prebavnem traktu (bruhanje in driska pri opicah); nadledvične žleze (kortikalna zastoj in / ali krvavitev pri podganah in opicah z nekrozo, ki ji sledi fibroza pri podganah); krvni in limfni sistem (hipocelularnost kostnega mozga in izčrpanost limfnega dela timusa, vranice in bezgavk); eksokrina trebušna slinavka (degranulacija acinarnih celic z enocelično nekrozo); žleze slinavke (acinarna hipertrofija); kostni sklepi (odebelitev rastne plošče); maternico (atrofija) in jajčnike (zmanjšanje razvoja foliklov). Vsi rezultati so bili ugotovljeni s klinično pomembnimi koncentracijami izpostavljenosti sunitiniba v plazmi. Drugi učinki, opaženi v študijah, so: podaljšanje intervala QTc, zmanjšanje iztisne frakcije levega prekata (LVEF) in testisov cevasta atrofija, povečane mesangialne celice v ledvicah, krvavitve v prebavnem traktu in ustni sluznici ter hipertrofija celic sprednje hipofize. endometrij) in rastna plošča kosti (odebelitev epifize ali displazija hrustanca) so povezane s farmakološkim delovanjem sunitiniba. Večina teh dogodkov je bila po prekinitvi zdravljenja za 2-6 tednov reverzibilna.
Genotoksičnost
Genotoksični potencial sunitiniba so ovrednotili in vitro in in vivo. Sunitinib pri presnovi, ki jo zagotavljajo jetra podgan, ni pokazal mutagenih učinkov na bakterije. Sunitinib ni povzročil strukturnih kromosomskih aberacij v človeških perifernih limfocitih in vitro. Pri človeških perifernih limfocitih so opazili poliploidijo (aberacije v številu kromosomov) v vitro, tako v prisotnosti kot v odsotnosti presnovne aktivacije. Sunitinib ni pokazal klastogenega potenciala v kostnem mozgu podgan in vivo. Glavni aktivni presnovek ni bil ocenjen glede genotoksičnega potenciala.
Rakotvornost
V enomesečni študiji za iskanje razpona odmerkov (0, 10, 25, 75 ali 200 mg / kg / dan), v katerem so transgene miši rasH2 krmili s peroralno sondo z dnevnim in neprekinjenim odmerjanjem odmerka pri so opazili najvišje odmerke (200 mg / kg / dan) karcinoma in hiperplazijo Brunnerjevih žlez dvanajstnika.
Izvedena je bila 6-mesečna študija za oceno rakotvornosti pri rasH2 transgenih miših, hranjenih s peroralno cevko, z odmerjanjem danega odmerka dnevno (0, 8, 25, 75 [zmanjšano na 50] mg / kg / dan). Pri odmerkih ≥ 25 mg / kg / dan, ki so jih dajali 1 ali 6 mesecev (≥ 7,3 -kratnik AUC pri bolnikih, ki so prejemali priporočeni dnevni odmerek [RDD]), so opazili povečano pojavnost v ozadju gastroduodenalnih karcinomov. Hemangiosarkom in / ali hiperplazijo želodčne sluznice.
V 2-letni študiji za oceno rakotvornosti pri podganah (0, 0,33, 1 ali 3 mg / kg / dan), ko so dajali sunitinib v 28-dnevnih ciklih, čemur so sledila 7-dnevna obdobja brez dajanja, je bilo ugotovljeno povečanje incidence feokromocitom in medularna hiperplazija nadledvične žleze pri samcih podgan, ki so več kot 1 leto prejemali odmerek 3 mg / kg / dan (≥ 7,8 -kratna AUC pri bolnikih, ki so prejemali RDD). Brunnerjev karcinom žleze se je pojavil v dvanajstniku v odmerkih ≥ 1 mg / kg / dan pri samicah, pri odmerkih 3 mg / kg / dan pri samcih in v želodčnih žlezah je bila pri enakih odmerkih očitna hiperplazija celic sluznice pri 3 mg / kg / dan dan pri moških; ti dogodki so se pojavili pri odmerkih 0,9, 7,8 in 7,8 -kratnik AUC pri bolnikih, ki so prejemali RDD. Pomen teh neoplastičnih ugotovitev v študijah kancerogenosti pri miših (rasH2) in podganah za ljudi, zdravljenih s sunitinibom, je negotov.
Strupenost za razmnoževanje in razvoj
V študijah reproduktivne toksičnosti niso opazili nobenih učinkov na plodnost samcev ali samic. Vendar so študije toksičnosti pri ponavljajočih se odmerkih, opravljene pri podganah in opicah, pokazale učinke na plodnost samic v obliki folikularne atrezije, degeneracije rumenega telesa, endometrijskih sprememb v maternici in zmanjšanja teže maternice in jajčnikov na ravni klinično pomembnih sistemska izpostavljenost. Učinke na plodnost samcev podgan so opazili v obliki cevaste atrofije v modih, zmanjšanega števila spermijev v epididimisu in koloidnega izčrpavanja v prostati in semenskih mešičkih pri izpostavljenosti plazmi 25 -kratni sistemski izpostavljenosti pri ljudeh.
Pri podganah je umrljivost zarodkov in plodov povzročila znatno zmanjšanje števila živih plodov, povečano število resorpcij, povečane izgube po implantaciji in skupne izgube potomcev pri 8 od 28 brejih samic pri izpostavljenosti plazmi 5,5-kratni sistemski izpostavljenosti pri ljudeh . Pri kuncih je bilo zmanjšanje teže noseče maternice in števila živih plodov posledica povečanja resorpcije ploda, izgube po implantaciji in skupne izgube potomcev pri 4 od 6 brejih samic pri 3-kratni izpostavljenosti plazmi. Sistemska izpostavljenost pri ljudeh. Zdravljenje s sunitinibom pri podganah med organogenezo je povzročilo razvojne učinke pri odmerkih ≥ 5 mg / kg / dan, ki jih je sestavljala povečana incidenca malformacij skeleta ploda, za katere je značilna predvsem zapoznela okostenelost prsnih / ledvenih vretenc in se pojavijo pri izpostavljenosti plazmi 5,5 krat sistemska izpostavljenost ljudi. Pri kuncih so razvojni učinki obsegali povečano pojavnost razcepa ustnice pri koncentracijah v plazmi, ki so približno enake tistim, ki so jih opazili v kliniki, ter razpoke ustnice in neba pri 2,7 -kratni sistemski izpostavljenosti pri človeku.
V študiji na brejih samicah podgan so ovrednotili učinke sunitiniba (0,3; 1,0; 3,0 mg / kg / dan) na pred- in postnatalni razvoj. Povečanje telesne mase mater med nosečnostjo in dojenjem se je zmanjšalo pri odmerkih> 1 mg / kg / dan, vendar do dojk 3 mg / kg / dan niso opazili reproduktivne toksičnosti pri materi (ocenjena izpostavljenost> 2, 3 -kratna AUC pri bolnikih) prejemanje RDD) Zmanjšano telesno težo potomcev so opazili pri odmerkih 3 mg / kg / dan v obdobjih pred odstavitvijo in po odstavitvi.Pri odmerkih 1 mg / kg / dan niso opazili razvojne toksičnosti (izpostavljenost približno ≥ 0,9 -kratna AUC pri bolnikih, ki so prejemali RDD).
06.0 FARMACEVTSKE INFORMACIJE
06.1 Pomožne snovi
Vsebina kapsule
Manitol (E421)
Natrijeva kroskarmeloza
Povidon (K-25)
Magnezijev stearat
Lupina kapsule
Žele
Rdeči železov oksid (E172)
Titanov dioksid (E171)
Črnilo
Šelak
Propilen glikol
Natrijev hidroksid
Povidon
Titanov dioksid (E171)
06.2 Nezdružljivost
Ni pomembno.
06.3 Obdobje veljavnosti
3 leta.
06.4 Posebna navodila za shranjevanje
Za shranjevanje tega zdravila niso potrebni posebni pogoji.
06.5 Vrsta ovojnine in vsebina pakiranja
Steklenice iz polietilena visoke gostote (HDPE) z zapiralom iz polipropilena, ki vsebuje 30 trdih kapsul.
Prozorni pretisni omoti iz poli (klorotrifluoroetilena) / PVC z perforiranimi enkratnimi odmerki in z aluminijasto folijo s toplotno tesnilnim lakom, ki vsebuje 28 x 1 trde kapsule.
Na trgu ni vseh navedenih pakiranj.
06.6 Navodila za uporabo in rokovanje
Brez posebnih navodil.
07.0 IMETNIK DOVOLJENJA ZA PROMET
Pfizer Ltd
Ramsgate Road
Sendvič, Kent CT13 9NJ
UK
08.0 ŠTEVILKA DOVOLJENJA ZA PROMET
EU/1/06/347/001
037192022
EU/1/06/347/004
09.0 DATUM PRVEGA DOVOLJENJA ALI PODALJŠANJA DOVOLJENJA
Datum prve odobritve: 19. julij 2006
Datum zadnje obnove: 09. januar 2012
10.0 DATUM REVIZIJE BESEDILA
11.0 ZA RADIOZDRAVILA POPOLNI PODATKI O DOSIMETRIJI INTERNEGA SEVANJA
12.0 ZA RADIOZDRAVILA, DODATNA PODROBNA NAVODILA O ZGODBENI PRIPRAVI IN NADZORU KAKOVOSTI