Da bi lahko razumljivo govorili o "hemoglobin (Hb), koristno je skrbeti za prvega mioglobin (Mb) ki je zelo podoben hemoglobinu, vendar je veliko enostavnejši.Med hemoglobinom in mioglobinom obstajajo tesni sorodstveni odnosi: oba sta konjugirana proteina in njihova protetična skupina (ne-beljakovinski del) je skupina heme.
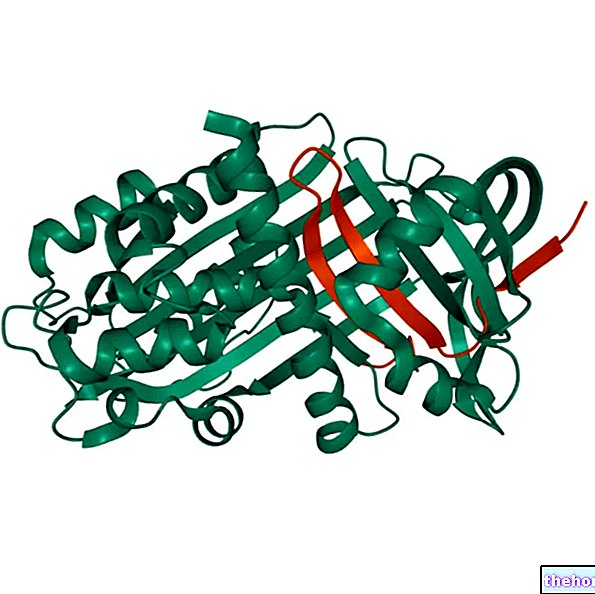
Mioglobin je kroglasta beljakovina, sestavljena iz ene same verige s približno sto petdeset aminokislinami (odvisno od organizma), njegova molekulska masa pa je približno 18 Kd.
Kot je omenjeno, je opremljen s skupino hema, ki je vstavljena v hidrofobni (ali lipofilni) del proteina, sestavljen iz gub, ki jih je mogoče pripisati strukturam α-vijačnic vlaknastih beljakovin.
Mioglobin je večinoma sestavljen iz segmentov α-vijačnic, ki jih je prisotnih v osmih in so skoraj izključno sestavljeni iz nepolarnih ostankov (levcin, valin, metionin in fenilalanin), polarnih ostankov pa praktično ni (asparaginska kislina, glutaminska kislina, lizin in arginin); edina polarna ostanka sta dva histidina, ki igrata temeljno vlogo pri vezavi kisika na skupino hema.
Skupina hema je kromoforna skupina (absorbira v vidnem) in je funkcionalna skupina mioglobina.
Glej tudi: glikiran hemoglobin - hemoglobin v urinu
Malo kemije

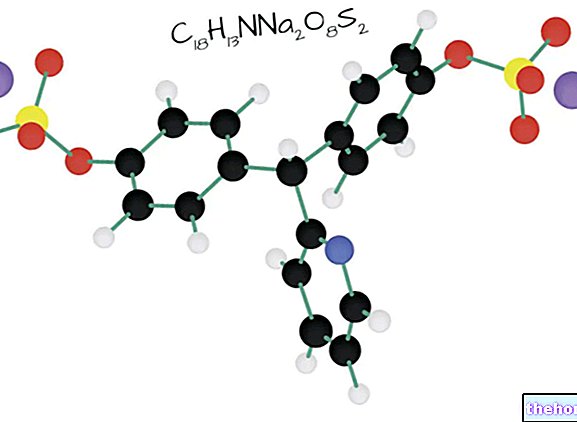
Vez med protoporfirinom in železom je tipična vez koordinacijskih spojin, ki so kemične spojine, v katerih osrednji atom (ali ion) tvori vezi z drugimi kemičnimi vrstami v številu, ki je večja od njegovega oksidacijskega števila (električni naboj). V primeru hema so te vezi reverzibilne in šibke.
Koordinacijsko število (število koordinacijskih vezi) železa je šest: okoli železa je lahko šest molekul, ki si delijo vezne elektrone.
Za tvorbo koordinacijske spojine sta potrebni dve orbitali s pravilno orientacijo: ena lahko "pridobi" elektrone, druga pa jih lahko podari.
V hemu železo tvori štiri ravninske vezi s štirimi dušikovimi atomi v središču protoporfirinskega obroča in peto vezjo s proksimalnim histidinskim dušikom; železo ima šesto prosto koordinacijsko vez in se lahko veže na kisik.
Ko je železo v obliki prostega iona, je njegov tip orbitale d vsi imajo enako energijo; v mioglobinu je železov ion vezan na protoporfirin in histidin: te vrste magnetno motijo orbitale d nekaj železa; obseg motenj bo različen za različne orbitale d odvisno od njihove prostorske usmerjenosti in orientacije motečih vrst. Ker mora biti celotna energija orbitalov konstantna, motnja povzroči energijsko ločitev med različnimi orbitalami: energija, ki jo pridobijo nekatere orbitale, je enakovredna energiji, ki jo izgubijo druge.
Če ločitev, ki se pojavi med orbitalami, ni zelo velika, je prednostna elektronska razporeditev z visokim spinom: vezni elektroni se poskušajo razporediti v vzporednih vrtljajih v čim več podnivojih (največja množica); če je po drugi strani motnja zelo močna in obstaja velika ločitev med orbitalami, bi bilo morda bolj priročno združiti vezne elektrone v orbitalah z nižjo energijo (nizki spin).
Ko se železo veže na kisik, molekula prevzame nizko spinsko razporeditev, medtem ko ima železo brez šeste koordinacijske vezi molekula visoko razporeditev spina.
Zahvaljujoč tej spinski razliki lahko s spektralno analizo mioglobina razumemo, ali je nanjo vezan kisik (MbO2) ali ne (Mb).
Mioglobin je tipičen mišični protein (vendar ga ne najdemo le v mišicah).
Mioglobin se ekstrahira iz kita, v katerem je prisoten v velikih količinah, in se nato očisti.
Kitovi imajo dihanje, podobno kot pri ljudeh: s pljuči morajo absorbirati zrak skozi dihalni proces; kitov mora prinesti čim več kisika v mišice, ki so sposobne kopičiti kisik, tako da ga vežejo na prisotni mioglobin; kisik se nato počasi sprošča, ko je kitov potopljen, ker njegov metabolizem potrebuje kisik: večja je količina kisika, ki ga lahko spermatozoid absorbira, in več kisika je na voljo med potopom.
Mioglybin veže kisik na reverzibilen način in je v večjem odstotku prisoten v perifernih tkivih, bolj ko je tkivo navajeno delati s časovno oddaljenimi zalogami kisika.
<--- Mioglobin je beljakovina, prisotna v mišicah, katere funkcija je ravno funkcija "rezervoarja" kisika.
Kar je meso bolj ali manj rdeče, je vsebnost hemoproteinov (rdeč je hem).
Hemoglobin ima veliko strukturnih podobnosti z mioglobinom in je sposoben reverzibilno vezati molekularni kisik; toda čeprav je mioglobin omejen na mišice in periferna tkiva na splošno, se hemoglobin nahaja v eritrocitih ali rdečih krvnih celicah (so psevdocelice, torej niso prave celice), ki sestavljajo 40% krvi.
V nasprotju z mioglobinom je delo hemoglobina vzeti kisik v pljučih, ga sprostiti v celice, kjer je to potrebno, vzeti ogljikov dioksid in ga sprostiti v pljuča, kjer se cikel začne znova.
L "hemoglobina gre za tetrameter, to pomeni, da je sestavljen iz štirih polipeptidnih verig, vsaka s hemsko skupino in enakih po dva (pri človeku sta dve alfa verigi in dve beta verigi).
Glavna funkcija hemoglobina je transport kisika; druga funkcija krvi, v kateri sodeluje hemoglobin, je transport snovi v tkiva.
Na poti od pljuč (bogatih s kisikom) do tkiv hemoglobin prenaša kisik (hkrati druge snovi pridejo do tkiv), medtem ko na obratni poti nosi s seboj odpadke, ki jih zbirajo tkiva, zlasti ogljik dioksid, ki nastaja pri presnovi.
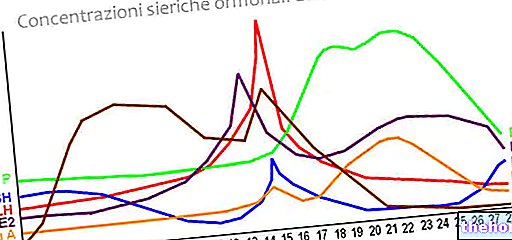
V razvoju človeka obstajajo geni, ki se izražajo le za določeno časovno obdobje; zato obstajajo različni hemoglobini: plodni, embrionalni, odraslega moškega.
Verige, ki sestavljajo te različne hemoglobine, imajo različne strukture, vendar so v resnici nekatere podobnosti v resnici bolj ali manj enake.
Razlaga prisotnosti več različnih verig je naslednja: med evolucijskim procesom organizmov se je razvil celo hemoglobin, specializiran za transport kisika z območij, ki so bogata z njim, na območja, kjer je pomanjkanje. Na začetku evolucijske verige "hemoglobin je prenašal kisik v majhnih organizmih; med razvojem so organizmi dosegli večje dimenzije, zato je bil hemoglobin spremenjen, da je lahko prenašal kisik na območja, ki so bolj oddaljena od točke, kjer je bil z njim bogat; za to so bile med evolucijskim procesom kodirane nove strukture verig, ki sestavljajo hemoglobin.
Mioglobin veže kisik tudi pri skromnih tlakih; v perifernih tkivih je tlak (PO2) približno 30 mmHg: mioglobin pri tem tlaku ne sprošča kisika, zato bi bil kot nosilec kisika neučinkovit. Po drugi strani pa hemoglobin , ima bolj elastično vedenje: veže kisik na visoke tlake in ga sprosti, ko se tlak zmanjša.
Ko je protein funkcionalno aktiven, lahko nekoliko spremeni obliko; na primer, oksigeniran mioglobin ima drugačno obliko kot neoksigeniran mioglobin in ta mutacija ne vpliva na sosede.
Drugače je pri povezanih beljakovinah, kot je hemoglobin: ko veriga oksigenira, se spremeni njena oblika, vendar je ta sprememba tridimenzionalna, zato so prizadete tudi druge verige tetrametra. Dejstvo, da so verige povezane med seboj., kaže, da sprememba enega vpliva na druge sosede, čeprav v drugačni meri; ko veriga oksigenira, druge verige tetrametra prevzamejo "manj sovražen odnos" do kisika: težave, s katerimi veriga oksigenati se zmanjšujejo, ko verige blizu njega oksigenirajo. Enako velja za deoksigenacijo.
Četrtinska struktura deoksihemoglobina se imenuje T (napeta) oblika, medtem ko se struktura oksihemoglobina imenuje R (sproščena) oblika; v napetem stanju obstaja vrsta precej močnih elektrostatičnih interakcij med kislimi aminokislinami in bazičnimi aminokislinami, ki vodijo v togo strukturo deoksihemoglobina (zato "napeta oblika"), medtem ko je kisik povezan, interakcije se zmanjšajo (od tod "sproščena oblika"). Poleg tega se v odsotnosti kisika naboj histidina (glej strukturo) stabilizira z nasprotnim nabojem asparaginske kisline, medtem ko v prisotnosti kisika beljakovine nagibajo k izgubi protona; vse to vključuje, da je oksigeniran hemoglobin močnejša kislina od deoksigeniranega hemoglobina: borov učinek.
Glede na pH se skupina hema bolj ali manj enostavno veže na kisik: v kislem okolju hemoglobin lažje sprošča kisik (napeta oblika je stabilna), medtem ko je v osnovnem okolju vez s kisikom trša.

Vsak hemoglobin sprosti 0,7 protona na mol kisika (O2), ki vstopa.
Bohrov učinek omogoča hemoglobinu, da izboljša svojo sposobnost prenašanja kisika.
Hemoglobin, ki potuje iz pljuč v tkiva, se mora uravnotežiti kot funkcija pritiska, pH in temperature.
Poglejmo učinek temperature.
Temperatura v pljučnih alveolah je za približno 1-1,5 ° C nižja od zunanje temperature, medtem ko je v mišicah temperatura približno 36,5-37 ° C; ko se temperatura dvigne, faktor nasičenosti pade (pri istem tlaku): to se zgodi, ker se kinetična energija poveča in daje prednost disociaciji.

Obstajajo še drugi dejavniki, ki lahko vplivajo na sposobnost hemoglobina, da se veže na kisik, eden od njih je koncentracija 2,3 bisfosfoglicerata.
2,3 bisfosfoglicerat je presnova, prisotna v eritrocitih v koncentraciji 4-5 mM (v nobenem drugem delu organizma ni v tako visoki koncentraciji).
Pri fiziološkem pH se 2,3 bisfosfoglicerat deprotonira in ima na sebi pet negativnih nabojev; vpet je med dve beta verigi hemoglobina, ker imajo te verige visoko koncentracijo pozitivnih nabojev. Elektrostatične interakcije med beta verigami in 2,3 bisfosfogliceratom dajejo sistemu določeno togost: dobimo napeto strukturo, ki ima majhno afiniteto do kisika; med oksigenacijo se 2,3 bisfosfoglicerat izloči.
V eritrocitih je c "poseben aparat, ki pretvori 1,3 bisfosfoglicerat (proizveden s presnovo) v 2,3 bisfosfoglicerat, tako da doseže koncentracijo 4-5 mM, zato lahko hemoglobin izmenja" kisik v tkivih.
Hemoglobin, ki prihaja v tkivo, je v sproščenem stanju (vezan na kisik), vendar je v bližini tkiva karboksiliran in prehaja v napeto stanje: beljakovine v tem stanju so manj nagnjene k vezavi s kisikom v sproščeno stanje, zato hemoglobin sprošča kisik v tkivo; poleg tega z reakcijo med vodo in ogljikovim dioksidom nastajajo ioni H +, zato je zaradi borovega učinka še več kisika.
Ogljikov dioksid se razprši v eritrocit, ki prehaja skozi plazemsko membrano; ker eritrociti sestavljajo približno 40% krvi, bi morali pričakovati, da vanj vstopi le 40% ogljikovega dioksida, ki se razprši iz tkiv, pravzaprav 90% ogljikovega dioksida vstopi v eritrocite, ker vsebujejo encim, ki pretvarja ogljikov dioksid v ogljikovi kislini povzroči, da je stacionarna koncentracija ogljikovega dioksida v eritrocitih nizka, zato je hitrost vstopa velika.

Drug pojav, ki se pojavi, ko eritrocit doseže tkivo, je naslednji: po gradientu "HCO3- (derivat ogljikovega dioksida) zapusti" eritrocit in za uravnoteženje izhoda negativnega naboja imamo "vstop kloridov, ki določa zvišanje osmotskega tlaka: za uravnoteženje te variacije obstaja tudi vstop vode, ki povzroči otekanje eritrocita (učinek HAMBURGER). Nasprotni pojav se pojavi, ko eritrocit doseže pljučne alveole: izpuhtenje eritrocitov (učinek HALDANE) Zato so venski eritrociti (usmerjeni v pljuča) okroglejši od arterijskih.