Zdravilne učinkovine: Denosumab
Prolia 60 mg raztopina za injiciranje v napolnjeni injekcijski brizgi
Paketni vložki Prolia so na voljo za velikosti pakiranj:- Prolia 60 mg raztopina za injiciranje v napolnjeni injekcijski brizgi
- Prolia 60 mg raztopina za injiciranje
Zakaj se zdravilo Prolia uporablja? Za kaj je to?
Kaj je zdravilo Prolia in kako deluje
Zdravilo Prolia vsebuje denosumab, beljakovino (monoklonsko protitelo), ki moti delovanje drugega proteina, za zdravljenje izgube kosti in osteoporoze.Z zdravljenjem z zdravilom Prolia so kosti močnejše in manj nagnjene k zlomom.
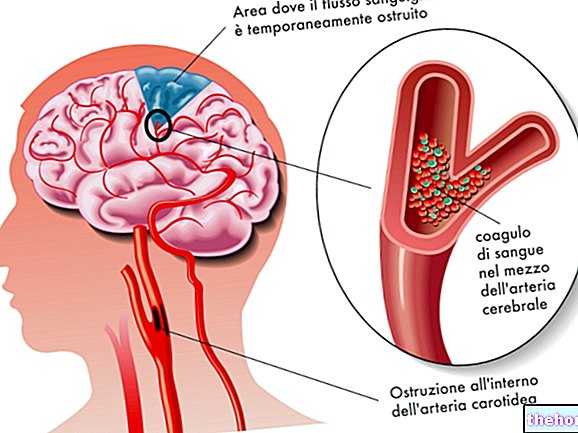
Kost je živo tkivo, ki se nenehno obnavlja. Estrogen pomaga ohranjati kosti zdrave. Po menopavzi lahko zaradi znižanja ravni estrogena kosti postanejo tanke in krhke, kar lahko privede do razvoja stanja, imenovanega osteoporoza. Osteoporoza se lahko pojavi tudi pri moških zaradi različnih vzrokov, vključno s staranjem in / ali nizko ravnijo moškega hormona, testosterona. Mnogi bolniki z osteoporozo nimajo simptomov, vendar še vedno ogrožajo zlome kosti, zlasti v hrbtenici, stegnenici in zapestjih.
Operacija ali zdravila, ki ustavijo proizvodnjo estrogena ali testosterona za zdravljenje bolnikov z rakom dojke ali prostate, lahko povzročijo tudi izgubo kosti. Kosti postanejo bolj krhke in se lažje zlomijo.
Za kakšno zdravljenje se uporablja zdravilo Prolia
Zdravilo Prolia se uporablja za zdravljenje:
- osteoporozo pri ženskah po menopavzi (postmenopavzalna osteoporoza) in pri moških, pri katerih je tveganje za zlome (zlomljene kosti) večje, da se zmanjša tveganje za zlome vretenc, nevretenc in kolkov.
- izguba kosti pri moških zaradi zmanjšane ravni hormonov (testosterona) zaradi operacije ali terapije z zdravili pri bolnikih z rakom prostate.
Kontraindikacije Ko se zdravila Prolia ne sme uporabljati
Ne uporabljajte zdravila Prolia
- če imate nizko raven kalcija v krvi (hipokalciemijo).
- če ste alergični na denosumab ali katero koli sestavino tega zdravila
Previdnostni ukrepi pri uporabi Kaj morate vedeti, preden boste vzeli zdravilo Prolia
Pred uporabo zdravila Prolia se posvetujte s svojim zdravnikom ali farmacevtom.
Med zdravljenjem z zdravilom Prolia lahko opazite pordelost in otekanje kože, najpogosteje v spodnjem delu noge, z občutkom vročine in bolečine (celulit) in po možnosti z vročinskimi simptomi. Če opazite katerega od teh simptomov, takoj obvestite svojega zdravnika.
Povejte svojemu zdravniku, če ste alergični na lateks (pokrovček igle napolnjene injekcijske brizge vsebuje derivat lateksa).
Med zdravljenjem z zdravilom Prolia morate jemati tudi dodatke kalcija in vitamina D. Zdravnik se bo o tem pogovoril z vami.
Morda imate med zdravljenjem z zdravilom Prolia nizko raven kalcija v krvi. Takoj obvestite svojega zdravnika, če opazite katerega od naslednjih simptomov: krče, trzanje ali krče v mišicah in / ali odrevenelost ali mravljinčenje v prstih, prstih na nogah ali okoli ust in / ali epileptične napade, zmedenost ali izgubo zavesti.
Povejte svojemu zdravniku, če imate ali ste kdaj imeli hude težave z ledvicami, okvaro ledvic ali če ste bili na dializi, kar lahko poveča tveganje za nizko raven kalcija v krvi, če ne jemljete dodatkov kalcija.
O neželenem učinku, imenovanem osteonekroza čeljusti (huda kostna degeneracija čeljusti), so pri bolnikih, ki so prejemali zdravilo Prolia zaradi osteoporoze, poročali redko (pojavijo se lahko pri največ 1 od 1.000 ljudi.) Osteonekroza čeljusti. Lahko se pojavi tudi po prekinitvi zdravljenja.
Pomembno je, da poskusite preprečiti razvoj osteonekroze čeljusti, saj je to boleče stanje, ki ga je težko zdraviti. Da bi zmanjšali tveganje za nastanek osteonekroze čeljusti, morate sprejeti nekatere previdnostne ukrepe.
Preden se zdravite, povejte svojemu zdravniku ali medicinski sestri (zdravstvenemu delavcu), če:
- imate težave z usti ali zobmi, na primer slaba zobna higiena, bolezni dlesni ali nameravate odstraniti zob;
- nimate rednega zobozdravstvenega zdravljenja ali že dolgo niste imeli zobozdravstvenega pregleda;
- ste kadilec (saj lahko to poveča tveganje za težave z zobmi);
- so bili predhodno zdravljeni z bisfosfonatom (uporablja se za zdravljenje ali preprečevanje kostnih motenj);
- jemljete zdravila, imenovana kortikosteroidi (na primer prednizolon ali deksametazon);
- ima raka.
Pred začetkom zdravljenja z zdravilom Prolia vas bo zdravnik morda zaprosil za zobozdravniški pregled (pri zobozdravniku).
Med zdravljenjem je treba vzdrževati dobro ustno higieno in redno obiskovati zobozdravnike. Če nosite proteze, se morate prepričati, da so pravilno vstavljeni. Če se zdravite pri zobozdravniku ali nameravate opraviti zobozdravstveno operacijo (npr. Odstranitev zoba), obvestite svojega zobozdravnika in obvestite zobozdravnika, da se zdravite z zdravilom Prolia.
Takoj se obrnite na svojega zdravnika in zobozdravnika, če opazite kakršne koli težave z usti ali zobmi, kot so padajoči zobje, bolečina ali oteklina ali nezdravljenje ustnih razjed ali izcedek, saj so to lahko znaki stranskega učinka, imenovanega osteonekroza spodnje čeljusti / maksile (ONJ).
Otroci in mladostniki
Zdravilo Prolia ni priporočljivo za otroke in mladostnike, mlajše od 18 let. Uporaba zdravila Prolia pri otrocih in mladostnikih ni raziskana.
Interakcije Katera zdravila ali živila lahko spremenijo učinek zdravila Prolia
Povejte svojemu zdravniku ali farmacevtu, če jemljete, ste pred kratkim jemali ali pa boste morda začeli jemati katero koli drugo zdravilo. Posebej pomembno je, da zdravniku poveste, če jemljete katerokoli drugo zdravilo, ki vsebuje denosumab.
Zdravila Prolia ne smete jemati skupaj z drugimi zdravili, ki vsebujejo denosumab
Opozorila Pomembno je vedeti, da:
Zdravila Prolia niso preučevali pri nosečnicah. Pomembno je, da zdravniku poveste, če ste noseči; če mislite, da bi lahko bili noseči; ali če načrtujete nosečnost.
Uporaba Prolije ni priporočljiva, če ste noseči. Če med jemanjem zdravila Prolia zanosite, povejte svojemu zdravniku. Morda vas bodo spodbudili k sodelovanju v Amgenovem programu za spremljanje nosečnosti. Lokalni kontaktni podatki so navedeni v odstavku 6 te brošure.
Ni znano, ali zdravilo Prolia prehaja v materino mleko. Pomembno je, da zdravniku poveste, če dojite ali nameravate dojiti. Zdravnik vam bo nato pomagal pri odločitvi, ali boste prenehali dojiti ali prenehati jemati zdravilo Prolia, glede na korist dojenja za otroka in korist jemanja zdravila Prolia za mater.
Če med jemanjem zdravila Prolia dojite, obvestite svojega zdravnika. Morda vas bodo spodbudili k sodelovanju v Amgenovem programu za spremljanje dojenja. Lokalni kontaktni podatki so navedeni v poglavju 6 te brošure.
Vpliv na sposobnost upravljanja vozil in strojev
Zdravilo Prolia nima vpliva ali ima zanemarljiv vpliv na sposobnost vožnje in upravljanja s stroji.
Prolia vsebuje sorbitol (E420)
Če vam je zdravnik povedal, da imate intoleranco za nekatere sladkorje (sorbitol E420), se pred jemanjem tega zdravila posvetujte z zdravnikom.
Če ste na dieti z nizko vsebnostjo natrija
To zdravilo vsebuje manj kot 1 mmol (23 mg) natrija na 60 mg, torej v bistvu "brez natrija".
Odmerjanje, način in čas dajanja Kako uporabljati zdravilo Prolia: Odmerjanje
Priporočeni odmerek je 60 mg napolnjena injekcijska brizga, ki se daje enkrat na 6 mesecev kot enkratna injekcija pod kožo (podkožno). Najprimernejša mesta za injiciranje so zgornji del stegen in trebuh. Če vam nekdo, ki vam pomaga pri injiciranju, lahko uporabi tudi zunanjo roko.Vsak paket Prolia vsebuje spominsko kartico z odstranljivimi nalepkami, ki jih lahko odstranite iz škatle. Z odstranljivimi nalepkami označite datum naslednjega injiciranja v koledarju in / ali uporabite opomnik za sledenje datumu naslednje injekcije.
Med zdravljenjem z zdravilom Prolia morate jemati tudi dodatke kalcija in vitamina D. Zdravnik se bo o tem pogovoril z vami.
Vaš zdravnik se lahko odloči, ali je najbolje, da vi ali negovalec injicirate zdravilo Prolia. Vaš zdravnik ali medicinska sestra vam ali vašemu negovalcu pokažeta, kako jemati zdravilo Prolia.
Pred uporabo napolnjene injekcijske brizge Prolia s samodejnim ščitnikom igle preberite te pomembne informacije:
- Pomembno je, da si injekcije ne poskušate dati, razen če ste od zdravnika ali zdravstvenega delavca prejeli ustreznih navodil.
- Zdravilo Prolia se daje kot injekcija v tkivo tik pod kožo (podkožna injekcija).
- Povejte svojemu zdravniku, če ste alergični na lateks (pokrovček igle na napolnjeni injekcijski brizgi vsebuje derivat lateksa). Ne odstranite sivega pokrovčka igle iz napolnjene injekcijske brizge, dokler niste pripravljeni za injiciranje.
- Napolnjene injekcijske brizge ne uporabljajte, če je padla na trdo površino. Uporabite novo napolnjeno injekcijsko brizgo in se obrnite na svojega zdravnika ali zdravstvenega delavca.
- Pred injiciranjem ne poskušajte aktivirati napolnjene injekcijske brizge.
- Ne poskušajte odstraniti prozornega varnostnega ščita iz napolnjene injekcijske brizge.
Za vsa vprašanja se obrnite na svojega zdravnika ali zdravstvenega delavca.
1. korak: Priprava
A) Iz embalaže odstranite napolnjeni ovoj brizge in pripravite materiale, potrebne za injiciranje: alkoholne robčke, vato ali blazinico iz gaze, obliž in posodo za odstranjevanje ostrih predmetov (niso priloženi).
Za bolj udobno injiciranje pred injiciranjem pustite napolnjeno injekcijsko brizgo pri sobni temperaturi približno 30 minut. Temeljito si umijte roke z milom in vodo.
Novo napolnjeno injekcijsko brizgo in druge potrebne materiale položite na čisto, dobro osvetljeno delovno površino.
- Injekcijske brizge ne poskušajte segreti z virom toplote, kot je vroča voda ali mikrovalovna pečica.
- Napolnjene injekcijske brizge ne puščajte izpostavljene neposredni sončni svetlobi. Ne.
- Napolnjene injekcijske brizge ne pretresite pretirano.
- Napolnjeno injekcijsko brizgo shranjujte nedosegljivo otrokom!
B) Odprite vrečko in odtrgajte pokrovček. Primite varnostni ščit napolnjene injekcijske brizge, da odstranite napolnjeno brizgo iz vrečke.
Iz varnostnih razlogov:
- Ne primite za bat.
- Ne primite sivega pokrovčka igle.
C) Preverite zdravilo in napolnjeno injekcijsko brizgo.
- Napolnjene injekcijske brizge ne uporabljajte, če:
- Zdravilo je motno ali vsebuje delce, mora biti bistra, brezbarvna do rahlo rumena raztopina.
- Nekateri deli so razpokani ali zlomljeni.
- Sivi pokrovček igle manjka ali ni varno pritrjen.
- Rok uporabnosti, natisnjen na nalepki, je potekel zadnji dan v navedenem mesecu.
V vseh primerih se obrnite na svojega zdravnika ali zdravstvenega delavca.
2. korak: Priprava
A) Roke si temeljito umijte. Pripravite in očistite mesto injiciranja.
Lahko uporabi:
- Zgornji del stegna.
- Trebuh, razen območja 5 centimetrov tik okoli popka.
- Zunanji del nadlakti (samo če vam injekcijo daje nekdo drug).
- Mesto injiciranja očistite z alkoholno krpo. Kožo pustite suho.
- Pred injiciranjem se ne dotikajte mesta injiciranja.
- Ne injicirajte na območja, kjer je koža občutljiva, ranjena, rdeča ali trda. Izogibajte se injiciranju na območja z brazgotinami ali strijami.
B) Siv pokrovček igle previdno izvlecite in ga odmaknite od telesa
C) Dvignite mesto injiciranja, da ustvarite stabilno površino.
- Pomembno je, da med injiciranjem kožo stisnete
3. korak: Injekcija
A) Naj bo koža stisnjena. Vstavite iglo v kožo
- Ne dotikajte se čistega področja kože
B) Počasi in enakomerno pritiskajte bat, dokler ne začutite ali zaslišite "klika". Potisnite do konca, dokler ne klikne
- Za injiciranje celotnega odmerka je pomembno, da pritisnete vse do "tac".
C) Spustite palec. Nato brizgo odmaknite stran od kože
Ko sprostite bat, bo varnostni ščit napolnjene injekcijske brizge varno pokril injekcijsko iglo.
- Sivega pokrovčka igle ne nameščajte nazaj na napolnjene injekcijske brizge.
4. korak: Dokončaj
A Odstranite napolnjeno injekcijsko brizgo in druge materiale v posodo za odstranjevanje ostrih predmetov.
Zdravila je treba odstraniti v skladu z lokalnimi predpisi. Vprašajte svojega farmacevta, kako zavreči zdravila, ki jih ne uporabljate več. Ti ukrepi bodo pomagali varovati okolje.
Injekcijsko brizgo in posodo za odstranjevanje ostrih predmetov hranite izven pogleda in dosega otrok.
- Napolnjene injekcijske brizge ne uporabljajte ponovno.
- Napolnjenih injekcijskih brizg ne reciklirajte in jih ne odvrzite med gospodinjske odpadke.
B) Preglejte mesto injiciranja.
Če opazite kri, pritisnite vato ali gazo na mesto injiciranja. Ne drgnite mesta injiciranja. Po potrebi namestite obliž.
Preveliko odmerjanje Kaj storiti, če ste vzeli preveč zdravila Prolia
Če ste pozabili vzeti zdravilo Prolia
Če ste izpustili odmerek zdravila Prolia, je treba injekcijo dati čim prej, nato pa injekcije vsakih 6 mesecev od datuma zadnje injekcije.
Če ste prenehali jemati zdravilo Prolia
Da bi imeli od svojega zdravljenja največ koristi, je pomembno, da jemljete zdravilo Prolia toliko časa, kot vam je predpisal zdravnik. Preden se odločite za prekinitev zdravljenja, se posvetujte s svojim zdravnikom.
Neželeni učinki Kakšni so stranski učinki zdravila Prolia
Kot vsa zdravila ima lahko tudi to zdravilo neželene učinke, ki pa se ne pojavijo pri vseh bolnikih.
Občasno se lahko pri bolnikih, zdravljenih z zdravilom Prolia, razvijejo kožne okužbe (predvsem celulitis). Takoj obvestite svojega zdravnika, če med jemanjem zdravila Prolia opazite katerega od teh simptomov: pordelost in otekanje kože, najpogosteje v spodnjem delu noge, z občutkom vročine in bolečine ter po možnosti zvišano telesno temperaturo.
Redko se lahko pri bolnikih, ki se zdravijo z zdravilom Prolia, pojavijo bolečine v ustih in / ali čeljusti, oteklina ali neozdravljive lezije v ustih ali čeljusti, izcedek, odrevenelost ali občutek teže v čeljusti / čeljusti ali nihanje zoba. To so lahko znaki hude kostne degeneracije čeljusti (osteonekroza). Takoj obvestite svojega zdravnika in zobozdravnika, če se med zdravljenjem z zdravilom Prolia ali po prekinitvi zdravljenja pojavijo takšni simptomi.
Redko imajo lahko bolniki, ki se zdravijo z zdravilom Prolia, nizko raven kalcija v krvi (hipokalciemija). Simptomi vključujejo mišične krče, trzanje ali krče in / ali odrevenelost ali mravljinčenje v prstih, prstih na nogah ali okoli ust in / ali epileptične napade, zmedenost ali izgubo zavesti. Če se pojavi kateri od teh simptomov, se takoj posvetujte z zdravnikom. Nizke ravni kalcija v krvi lahko povzročijo tudi spremembo srčnega ritma, imenovano podaljšanje intervala QT, kar opazimo na elektrokardiografiji (EKG).
Zelo pogosti neželeni učinki (pojavijo se lahko pri več kot 1 od 10 bolnikov):
- bolečine v kosteh, sklepih in / ali mišicah, včasih hude,
- bolečine v rokah ali nogah (bolečine v okončinah).
Pogosti neželeni učinki (pojavijo se lahko pri največ 1 od 10 bolnikov):
- pogosta in boleča potreba po uriniranju, kri v urinu, urinska inkontinenca,
- okužbe zgornjih dihal,
- bolečine, mravljinčenje ali odrevenelost, ki sevajo v spodnje okončine (išias),
- zamegljenost leče (katarakta),
- zaprtje,
- nelagodje v trebuhu,
- izpuščaj,
- srbenje, pordelost in / ali suhost kože (ekcem).
Občasni neželeni učinki (pojavijo se lahko pri največ 1 od 100 bolnikov):
- zvišana telesna temperatura, bruhanje in bolečine v trebuhu ali nelagodje v trebuhu (divertikulitis),
- ušesne okužbe.
Redki neželeni učinki (pojavijo se lahko pri največ 1 od 1.000 bolnikov):
- alergijske reakcije (npr. otekanje obraza, ustnic, jezika, grla ali drugih delov telesa; izpuščaj, srbenje, koprivnica, piskanje ali težave z dihanjem).
Redko se lahko pojavijo občasni zlomi stegnenice.
Če se med zdravljenjem z zdravilom Prolia pojavijo nove ali nenavadne bolečine v kolku, dimljah ali stegnih, se obrnite na svojega zdravnika, saj je to lahko zgodnji znak možnega zloma stegnenice.
Če opazite kateri koli neželeni učinek, se posvetujte z zdravnikom ali farmacevtom, kar vključuje morebitne neželene učinke, ki niso navedeni v tem navodilu.
Poročanje o stranskih učinkih
Če opazite kateri koli neželeni učinek, se posvetujte z zdravnikom ali farmacevtom, kar vključuje morebitne neželene učinke, ki niso navedeni v tem navodilu. O neželenih učinkih lahko poročate tudi neposredno prek nacionalnega sistema poročanja, navedenega v Dodatku V. S poročanjem o neželenih učinkih lahko pomagate zagotoviti več informacij o varnosti tega zdravila.
Potek in hramba
Zdravilo shranjujte nedosegljivo otrokom!
Tega zdravila ne smete uporabljati po datumu izteka roka uporabnosti, ki je naveden na nalepki in škatli poleg oznake EXP. Rok uporabnosti se nanaša na zadnji dan navedenega meseca.
Shranjujte v hladilniku (2 ° C - 8 ° C).
Ne zamrzujte.
Shranjujte v originalni ovojnini za zaščito zdravila pred svetlobo.
Ne pretresite pretirano.
Napolnjeno injekcijsko brizgo lahko pred injiciranjem pustite iz hladilnika, da doseže sobno temperaturo (do 25 ° C). Tako bo injiciranje bolj udobno. Ko brizga doseže sobno temperaturo (do 25 ° C), jo je treba uporabiti v 30 dneh.
Ne mečite nobenih zdravil v odpadne vode ali med gospodinjske odpadke. Vprašajte svojega farmacevta, kako zavreči zdravila, ki jih ne uporabljate več. Tako boste zaščitili okolje.
6. Vsebina pakiranja in drugi podatki
Kaj vsebuje zdravilo Prolia
- Zdravilna učinkovina je denosumab. Vsaka 1 ml napolnjena injekcijska brizga vsebuje 60 mg denosumaba (60 mg / ml).
- Pomožne snovi so ledeni ocetna kislina, natrijev hidroksid, sorbitol (E420), polisorbat 20 in voda za injekcije.
Izgled zdravila Prolia in vsebina pakiranja
Prolia je bistra, brezbarvna do rahlo rumena raztopina za injiciranje v napolnjeni injekcijski brizgi, pripravljeni za uporabo.
Vsako pakiranje vsebuje eno napolnjeno injekcijsko brizgo z ščitnikom za iglo.Vsako pakiranje vsebuje eno napolnjeno injekcijsko brizgo.
Pomembno
Pred uporabo napolnjene injekcijske brizge Prolia s samodejnim ščitnikom igle preberite te pomembne informacije:
- Pomembno je, da si injekcije ne poskušate dati, razen če ste od zdravnika ali zdravstvenega delavca prejeli ustreznih navodil.
- Zdravilo Prolia se daje kot injekcija v tkivo tik pod kožo (podkožna injekcija).
- Povejte svojemu zdravniku, če ste alergični na lateks (pokrovček igle na napolnjeni injekcijski brizgi vsebuje derivat lateksa).
- Ne odstranite sivega pokrovčka igle iz napolnjene injekcijske brizge, dokler niste pripravljeni na injiciranje.
- Napolnjene injekcijske brizge ne uporabljajte, če je padla na trdo površino. Uporabite novo napolnjeno injekcijsko brizgo in se obrnite na svojega zdravnika ali zdravstvenega delavca.
- Pred injiciranjem ne poskušajte aktivirati napolnjene injekcijske brizge.
- Ne poskušajte odstraniti prozornega varnostnega ščita iz napolnjene injekcijske brizge.
Za vsa vprašanja se obrnite na svojega zdravnika ali zdravstvenega delavca.
1. korak: Priprava
A Odstranite napolnjeni ovoj brizge iz embalaže in pripravite materiale, potrebne za injiciranje: alkoholne robčke, bombažno palčko ali gazno blazinico, obliž in posodo za odstranjevanje ostrih predmetov (niso priloženi).
Za bolj udobno injiciranje pred injiciranjem pustite napolnjeno injekcijsko brizgo pri sobni temperaturi približno 30 minut. Temeljito si umijte roke z milom in vodo.
Novo napolnjeno injekcijsko brizgo in druge potrebne materiale položite na čisto, dobro osvetljeno delovno površino.
- Injekcijske brizge ne poskušajte segreti z virom toplote, kot je vroča voda ali mikrovalovna pečica.
- Napolnjene injekcijske brizge ne puščajte izpostavljene neposredni sončni svetlobi.
- Napolnjene injekcijske brizge ne pretresite pretirano.
- Napolnjeno injekcijsko brizgo shranjujte nedosegljivo otrokom!
B Odprite ovoj in odtrgajte pokrov. Primite varnostni ščit napolnjene injekcijske brizge, da odstranite napolnjeno brizgo iz ovoja.
Iz varnostnih razlogov:
- Ne primite za bat.
- Ne primite sivega pokrovčka igle.
C Preverite zdravilo in napolnjeno injekcijsko brizgo.
Napolnjene injekcijske brizge ne uporabljajte, če:
- Zdravilo je motno ali vsebuje delce, mora biti bistra, brezbarvna do rahlo rumena raztopina.
- Nekateri deli so razpokani ali zlomljeni.
- Sivi pokrovček igle manjka ali ni varno pritrjen.
- Rok uporabnosti, natisnjen na nalepki, je potekel zadnji dan v navedenem mesecu.
V vseh primerih se obrnite na svojega zdravnika ali zdravstvenega delavca.
2. korak: Priprava
A Temeljito si umijte roke. Pripravite in očistite mesto injiciranja. Lahko uporabi:
- Zgornji del stegna. Zgornji del trebuha Zgornji del stegna
- Trebuh, razen območja 5 centimetrov tik okoli popka.
- Zunanji del nadlakti (samo če vam injekcijo daje nekdo drug).
Mesto injiciranja očistite z alkoholno krpo. Kožo pustite suho.
- Pred injiciranjem se ne dotikajte mesta injiciranja.
- Ne injicirajte na območja, kjer je koža občutljiva, ranjena, rdeča ali trda. Izogibajte se injiciranju na območja z brazgotinami ali strijami.
B Sivi pokrovček igle previdno odstranite navzven in stran od telesa.
C Dvignite mesto injiciranja, da ustvarite stabilno površino.
Pomembno je, da med injiciranjem kožo stisnete
3. korak: Injekcija
A Naj bo koža dvignjena. Vstavite iglo v kožo.
- Ne dotikajte se čistega področja kože
B Z počasnim in enakomernim pritiskom pritiskajte bat, dokler ne začutite ali zaslišite "klika". Potisnite do konca, dokler ne klikne.
- Za injiciranje celotnega odmerka je pomembno, da pritisnete vse do "tac".
C Spustite palec. Nato brizgo odmaknite stran od kože
Ko sprostite bat, bo varnostni ščit napolnjene injekcijske brizge varno pokril injekcijsko iglo.
- Sivega pokrovčka igle ne nameščajte nazaj na napolnjene injekcijske brizge.
4. korak: Dokončaj
A Odstranite napolnjeno injekcijsko brizgo in druge materiale v posodo za odstranjevanje ostrih predmetov.
Zdravila je treba odstraniti v skladu z lokalnimi predpisi. Vprašajte svojega farmacevta, kako zavreči zdravila, ki jih ne uporabljate več. Ti ukrepi bodo pomagali varovati okolje.
Injekcijsko brizgo in posodo za odstranjevanje ostrih predmetov hranite izven pogleda in dosega otrok.
- Napolnjene injekcijske brizge ne uporabljajte ponovno.
- Napolnjenih injekcijskih brizg ne reciklirajte in jih ne odvrzite med gospodinjske odpadke.
B Preglejte mesto injiciranja.
Če opazite kri, pritisnite vato ali gazo na mesto injiciranja. Ne drgnite mesta injiciranja. Po potrebi namestite obliž.
Navodila za injiciranje zdravila Prolia z napolnjeno injekcijsko brizgo
Ta razdelek vsebuje informacije o uporabi napolnjene injekcijske brizge Prolia. Pomembno je, da vi ali vaš skrbnik ne injicirate, preden prejmete ustrezna navodila svojega zdravnika ali medicinske sestre. Umijte si roke pred vsako injekcijo. Če imate kakršna koli vprašanja o injiciranju, se za pomoč obrnite na svojega zdravnika ali medicinsko sestro.
Pred začetkom
Pred uporabo napolnjene injekcijske brizge natančno preberite vsa navodila.
Napolnjene injekcijske brizge ne uporabljajte, če ste odstranili pokrovček igle.
Kako se uporablja napolnjena injekcijska brizga Prolia?
Zdravnik vam je predpisal napolnjeno injekcijsko brizgo za injiciranje zdravila Prolia pod kožo (podkožno). Vbrizgati morate celotno vsebino (1 ml) napolnjene injekcijske brizge Prolia, ki jo morate injicirati enkrat na 6 mesecev v skladu s predpisi zdravnik.
Kaj je potrebno:
Za injiciranje boste potrebovali:
- Nova napolnjena injekcijska brizga Prolia; In
- Bombažne kroglice, namočene v alkoholu, ali podobna razkužila.
Kaj morate storiti pred podkožno injekcijo zdravila Prolia
- Napolnjeno injekcijsko brizgo vzemite iz hladilnika. Napolnjene injekcijske brizge NE dvigujte za stran igle ali pokrovčka, ker jo lahko poškodujete.
- Napolnjeno injekcijsko brizgo pustite iz hladilnika, dokler ne doseže sobne temperature. Tako bo injiciranje bolj udobno. NE segrevajte brizge na noben drug način (na primer v mikrovalovni pečici ali vroči vodi). NE izpostavljajte brizge neposredni sončni svetlobi.
- Napolnjene injekcijske brizge NE pretresite pretirano.
- NE odstranite pokrovčka igle iz napolnjene injekcijske brizge, dokler niste pripravljeni za injiciranje.
- Preverite rok uporabnosti na nalepki napolnjene injekcijske brizge (EXP). NE uporabljajte je, če je to po zadnjem dnevu v prikazanem mesecu.
- Preverite videz zdravila Prolia. To mora biti bistra, brezbarvna do rahlo rumena tekočina. Raztopine ne injicirajte, če vsebuje delce ali če je motna ali razbarvana.
- Poiščite udobno, dobro osvetljeno in čisto površino in imejte pri roki vse, kar potrebujete.
- Temeljito si umijte roke.
Kam injicirati?
Najprimernejša mesta za injiciranje so zgornji del stegen in trebuh.
Če vam nekdo, ki vam pomaga pri injiciranju, lahko uporabi tudi zunanjo roko.
Kako injicirati?
- Kožo razkužite z alkoholno krpico.
- Da bi se izognili upogibanju igle, nežno potegnite pokrovček z igle vodoravno, ne da bi ga obrnili. NE dotikajte se igle in ne pritiskajte bata.
- V napolnjeni injekcijski brizgi lahko opazite majhen zračni mehurček. Pred injiciranjem ne smete odstraniti zračnega mehurčka. Injiciranje raztopine z zračnim mehurčkom je neškodljivo.
- Dvignite kožo med palcem in kazalcem (ne da bi ga stisnili). Potisnite iglo do konca v kožo, kot vam je pokazal zdravnik ali medicinska sestra.
- Bat počasi in enakomerno pritiskajte, pri tem pa kožo vedno držite stisnjeno. Bat potisnite do konca, dokler ne vbrizgate vse raztopine.
- Izvlecite iglo in sprostite kožo.
- Če opazite kapljico krvi, jo lahko nežno odstranite z vato ali gazo. Ne drgnite mesta injiciranja. Po potrebi lahko mesto injiciranja prekrijete z obližem
- Vsako napolnjeno injekcijsko brizgo uporabite samo za eno injekcijo. NE uporabljajte zdravila Prolia, ki je ostala v brizgi.
Ne pozabite: če imate kakršne koli težave, se za pomoč ali nasvet obrnite na svojega zdravnika ali medicinsko sestro.
Odstranitev rabljenih brizg
- Pokrovčka NE nameščajte nazaj na uporabljene igle.
- Uporabljene brizge shranjujte nedosegljivo otrokom!
- Uporabljene brizge je treba odstraniti v skladu z lokalnimi predpisi. Vprašajte svojega farmacevta, kako zavreči zdravila, ki jih ne uporabljate več. To bo pomagalo zaščititi okolje.
Navodilo za uporabo vira: AIFA (Italijanska agencija za zdravila). Vsebina, objavljena januarja 2016. Prisotne informacije morda niso posodobljene.
Za dostop do najnovejše različice je priporočljivo dostopati do spletnega mesta AIFA (Italijanska agencija za zdravila). Zavrnitev odgovornosti in koristne informacije.
01.0 IME ZDRAVILA
PROLIA 60 MG raztopina za injiciranje v predhodno napolnjeni brizgalni brizgi
02.0 KAKOVOSTNA IN KOLIČINSKA SESTAVA
Vsaka napolnjena injekcijska brizga vsebuje 60 mg denosumaba v 1 ml raztopine (60 mg / ml).
Denosumab je človeško monoklonsko protitelo tipa IgG2, proizvedeno v celični liniji sesalcev (CHO) s tehnologijo rekombinantne DNA.
Pomožne snovi z znanim učinkom:
Vsak ml raztopine vsebuje 47 mg sorbitola (E420) (glejte poglavje 4.4).
Za celoten seznam pomožnih snovi glejte poglavje 6.1.
03.0 FARMACEVTSKA OBLIKA
Raztopina za injiciranje (injiciranje).
Bistra, brezbarvna do rahlo rumena raztopina.
04.0 KLINIČNE INFORMACIJE
04.1 Terapevtske indikacije
Zdravljenje osteoporoze pri ženskah po menopavzi in pri moških s povečanim tveganjem za zlome.
Pri ženskah po menopavzi Prolia znatno zmanjša tveganje za zlome vretenc, nevretenc in kolka.
Zdravljenje izgube kosti, povezane s hormonsko ablativno terapijo pri moških z rakom prostate pri povečanem tveganju zlomov (glejte poglavje 5.1). Pri moških z rakom prostate, ki se zdravijo s hormonsko ablativno terapijo, zdravilo Prolia znatno zmanjša tveganje za zlome vretenc.
04.2 Odmerjanje in način uporabe
Odmerjanje
Priporočeni odmerek zdravila Prolia je 60 mg v enkratni podkožni injekciji enkrat na 6 mesecev v stegno, trebuh ali nadlakti.
Bolniki morajo prejemati ustrezne dodatke kalcija in vitamina D (glejte poglavje 4.4).
Bolnikom, ki se zdravijo z zdravilom Prolia, je treba dati navodilo za uporabo in opomnik za bolnika.
Bolniki z okvaro ledvic
Pri bolnikih z okvaro ledvic prilagoditev odmerka ni potrebna (za priporočila o spremljanju kalcija glejte poglavje 4.4).
Bolniki z okvaro jeter
Varnosti in učinkovitosti denosumaba pri bolnikih z okvaro jeter niso preučevali (glejte poglavje 5.2).
Starejši bolniki (starost ≥ 65)
Pri starejših bolnikih prilagoditev odmerka ni potrebna.
Pediatrična populacija
Zdravilo Prolia ni priporočljivo pri pediatričnih bolnikih (starost
Način dajanja
Za podkožno uporabo.
Dajanje mora opraviti oseba, ki je ustrezno usposobljena za injiciranje.
Za navodila o uporabi, ravnanju in odstranjevanju glejte poglavje 6.6.
04.3 Kontraindikacije
• Hipokalciemija (glejte poglavje 4.4).
• Preobčutljivost za zdravilno učinkovino ali katero koli pomožno snov, navedeno v poglavju 6.1.
04.4 Posebna opozorila in ustrezni previdnostni ukrepi za uporabo
Vnos kalcija in vitamina D
Pomembno je, da vsi bolniki dobijo ustrezen vnos kalcija in vitamina D.
Previdnostni ukrepi za uporabo
Hipokalcemija
Pomembno je prepoznati bolnike, pri katerih obstaja tveganje za hipokalcemijo. Hipokalciemijo je treba odpraviti z ustreznim vnosom kalcija in vitamina D. Pred začetkom zdravljenja je priporočljivo klinično spremljanje ravni kalcija pred vsakim odmerkom, pri bolnikih, ki so nagnjeni k razvoju hipokalciemije, pa v dveh tednih po odmerku. Če nekateri bolniki doživijo sum na simptome hipokalciemijo med zdravljenjem (za seznam simptomov glejte poglavje 4.8) je treba izmeriti ravni kalcija. Bolnike je treba spodbujati, da poročajo o simptomih, ki kažejo na hipokalciemijo.
V obdobju trženja zdravila so poročali o hudi simptomatski hipokalciemiji (glejte poglavje 4.8), ki se je v večini primerov pojavila v prvih tednih po začetku zdravljenja, lahko pa tudi kasneje.
Kožne okužbe
Pri bolnikih, zdravljenih z zdravilom Prolia, se lahko pojavijo kožne okužbe (predvsem celulitis), ki zahtevajo hospitalizacijo (glejte poglavje 4.8). Bolnikom je treba povedati, naj nemudoma poiščejo zdravniško pomoč, če razvijejo znake ali simptome celulitisa.
Osteonekroza čeljusti (ONJ)
O ONJ so redko poročali pri bolnikih, zdravljenih z zdravilom Prolia za zdravljenje osteoporoze (glejte poglavje 4.8).
Začetek zdravljenja / novo zdravljenje je treba pri bolnikih z neozdravljenimi, odprtimi lezijami mehkih tkiv v ustih odložiti. Pred zdravljenjem z zdravilom Prolia pri bolnikih s spremljajočimi dejavniki tveganja je priporočljiv zobozdravniški pregled z zobno profilakso in individualna ocena koristi / tveganja.
Pri ocenjevanju bolnikovega tveganja za razvoj ONJ je treba upoštevati naslednje dejavnike tveganja:
• jakost zdravila, ki zavira resorpcijo kosti (tveganje je večje pri močnejših zdravilih), način dajanja (tveganje je večje pri parenteralni uporabi) in kumulativni odmerek terapije resorpcije kosti.
• tumor, sočasna obolenja (npr. Anemija, koagulopatije, okužbe), kajenje.
• sočasne terapije: kortikosteroidi, kemoterapija, zaviralci angiogeneze, radioterapija v predelu glave in vratu.
• slaba ustna higiena, parodontalna bolezen, nepravilno vstavljene zobne proteze, že obstoječa zobna bolezen, invazivni zobozdravstveni posegi, kot so ekstrakcije zob.
Vse bolnike je treba spodbujati, da vzdržujejo dobro ustno higieno, redno opravljajo zobozdravstvene preglede in takoj poročajo o kakršnih koli ustnih simptomih, kot so gibljivost zob, bolečina ali oteklina ali neozdravljenje ustnih ran ali prisotnost izločkov med zdravljenjem z zdravilom Prolia. Med zdravljenjem je treba invazivne zobozdravstvene posege izvesti šele po skrbnem premisleku in se jim je treba izogibati v neposredni bližini dajanja zdravila Prolia.
Načrt zdravljenja bolnikov, pri katerih se razvije ONJ, je treba opredeliti v tesnem sodelovanju med zdravnikom, ki se zdravi, in zobozdravnikom ali oralnim kirurgom, ki ima izkušnje z ONJ. Razmisliti je treba o začasni prekinitvi zdravljenja, dokler se stanje ne razreši, in po možnosti za ublažitev dejavnikov tveganja kar je prispevalo k njegovemu nastanku.
Atipični zlomi stegnenice
Pri bolnikih, zdravljenih z zdravilom Prolia, so poročali o primerih atipičnih zlomov stegnenice (glejte poglavje 4.8). Atipični zlomi stegnenice se lahko pojavijo z minimalno ali brez poškodb v subtrohanteričnih in diafiznih predelih stegnenice. Za te dogodke so značilne posebne radiografske ugotovitve. Poročali so tudi o atipičnih zlomih stegnenice
pri bolnikih z nekaterimi sočasnimi boleznimi (npr. pomanjkanjem vitamina D, revmatoidnim artritisom, hipofosfatazijo) in v primeru uporabe nekaterih zdravil (npr. bisfosfonatov, glukokortikoidov, zaviralcev protonske črpalke). Ti dogodki so se pojavili tudi v odsotnosti antiresorpcijske terapije. Podobni zlomi, o katerih so poročali v povezavi z uporabo bisfosfonatov, so pogosto dvostranski; zato je treba pri bolnikih, zdravljenih z zdravilom Prolia, pri katerih je prišlo do zloma stegnenice, oceniti kontralateralno stegnenico. Pri bolnikih s sumom na atipičen zlom stegnenice je treba razmisliti o ukinitvi L. zdravljenja z zdravilom Prolia, čaka na oceno bolnika na podlagi individualne analize koristi in tveganja.Med zdravljenjem z zdravilom Prolia je treba bolnikom svetovati, naj poročajo o novih ali nenavadnih bolečinah v stegnu, kolku ali v dimljah. Bolnike s takšnimi simptomi je treba pregledati zaradi nepopolnega zloma stegnenice.
Sočasno zdravljenje z drugimi zdravili, ki vsebujejo denosumab
Bolnikov, ki se zdravijo z zdravilom Prolia, ne smemo zdraviti hkrati z drugimi zdravili, ki vsebujejo denosumab (za preprečevanje okostja pri odraslih s kostnimi metastazami iz solidnih tumorjev).
Ledvična okvara
Bolniki s hudo okvaro ledvic (dializa z očistkom kreatinina poveča tveganje za nastanek hipokalciemije. Tveganje za nastanek hipokalciemije in posledično zvišanje ravni obščitničnega hormona se povečuje s povečanjem stopnje okvare ledvic. Ustrezen vnos kalcija, vitamin D in redno spremljanje kalcija so še posebej pomembni pri teh bolnikih, kot je navedeno zgoraj.
Suha naravna guma
Pokrovček igle napolnjene injekcijske brizge vsebuje suh naravni kavčuk (derivat lateksa), ki lahko povzroči alergijske reakcije.
Opozorila za pomožne snovi
To zdravilo vsebuje sorbitol. Bolniki z redkimi dednimi intolerancami za fruktozo ne smejo jemati zdravila Prolia.
To zdravilo vsebuje manj kot 1 mmol (23 mg) natrija na 60 mg, torej v bistvu "brez natrija".
04.5 Interakcije z drugimi zdravili in druge oblike interakcij
V študiji interakcij zdravilo Prolia ni vplivalo na farmakokinetiko midazolama, ki se presnavlja s citokromom P450 3A4 (CYP3A4). To kaže, da ni pričakovati, da bi zdravilo Prolia spremenilo farmakokinetiko zdravil, ki se presnavljajo s CYP3A4.
Kliničnih podatkov o sočasni uporabi denosumaba in nadomestnega hormonskega zdravljenja (estrogena) ni, kljub temu pa je potencialno tveganje za farmakodinamično interakcijo majhno.
V prehodni klinični študiji (od alendronata do denosumaba) pri ženskah po menopavzi z osteoporozo se farmakokinetika in farmakodinamika denosumaba s prejšnjo terapijo z alendronatom nista spremenila.
04.6 Nosečnost in dojenje
Nosečnost
Ni ustreznih podatkov o uporabi zdravila Prolia pri nosečnicah. Reprodukcijska toksičnost je bila dokazana v študiji, izvedeni pri opicah cynomolgus, zdravljenih med nosečnostjo z odmerki denosumaba, kar je povzročilo 119-kratno sistemsko izpostavljenost glede na AUC. (glejte poglavje 5.3).
Uporaba zdravila Prolia pri nosečnicah ni priporočljiva.
Ženske, ki med zdravljenjem z zdravilom Prolia zanosijo, se vabijo, da se vpišejo v program Amgenovega nadzora nosečnosti. Kontaktni podatki so navedeni v poglavju 6 navodila za uporabo - Podatki za uporabnika.
Čas hranjenja
Ni znano, ali se denosumab izloča v materino mleko pri ljudeh. Študije, izvedene na gensko spremenjenih miših, pri katerih je bil odstranjen gen, ki kodira RANKL (miši z izločanjem), kažejo, da bi lahko odsotnost RANKL (tarča denosumaba - glejte poglavje 5.1) med nosečnostjo vplivala na zorenje mlečne žleze in povzročila spremembe v laktaciji po porodu (glejte poglavje 5.3). Odločiti se je treba, ali se vzdržati dojenja ali zdravljenja z zdravilom Prolia, ob upoštevanju koristi dojenja za novorojenčka / dojenčka in koristi zdravljenja z zdravilom Prolia za žensko.
Ženske, ki dojijo med zdravljenjem z zdravilom Prolia, se vabijo, da se vključijo v program Amgenovega nadzora laktacije. Kontaktni podatki so navedeni v poglavju 6 navodil za uporabo - Informacije za uporabnico.
Plodnost
Podatkov o učinkih denosumaba na plodnost pri ljudeh ni. Študije na živalih ne kažejo neposrednih ali posrednih škodljivih učinkov na plodnost (glejte poglavje 5.3).
04.7 Vpliv na sposobnost vožnje in upravljanja s stroji
Zdravilo Prolia nima vpliva ali ima zanemarljiv vpliv na sposobnost vožnje in upravljanja s stroji.
04.8 Neželeni učinki
Povzetek varnostnega profila
Splošni varnostni profil zdravila Prolia je bil pri petih s placebom kontroliranih kliničnih preskušanjih III. Faze podoben pri bolnikih z osteoporozo in pri bolnikih z rakom dojke ali prostate, zdravljenih s hormonsko ablativno terapijo.
Najpogostejša neželena učinka zdravila Prolia (opažena pri več kot enem od desetih bolnikov) sta mišično -skeletna bolečina in bolečine v okončinah. Pri bolnikih, zdravljenih z zdravilom Prolia, so občasno opazili primere celulita; redki primeri hipokalciemije, preobčutljivosti, osteonekroze čeljusti in atipičnih zlomov stegnenice (glejte poglavje 4.4 in poglavje 4.8 - opis izbranih neželenih učinkov).
Tabela neželenih učinkov
Podatki, prikazani v preglednici 1, opisujejo neželene učinke, o katerih so poročali v kliničnih preskušanjih faze II in III pri bolnikih z osteoporozo in pri bolnikih z rakom dojke ali prostate, ki so prejemali ablativno hormonsko terapijo in / ali iz spontanih poročil.
Za razvrstitev neželenih učinkov je bila uporabljena naslednja konvencija (glej tabelo 1): zelo pogosti (≥ 1/10), pogosti (≥ 1/100,
Preglednica 1 Neželeni učinki, o katerih so poročali pri bolnikih z osteoporozo in bolnikih z rakom dojke ali prostate, zdravljenih s hormonsko ablativno terapijo
1 Glejte poglavje Opis izbranih neželenih učinkov
V združeni analizi podatkov iz vseh s placebom nadzorovanih kliničnih preskušanj II in III faze so poročali o gripi podobnem sindromu s surovo incidenco 1,2% pri preiskovancih, zdravljenih z denosumabom, in 0,7% pri osebah, zdravljenih s placebom. Čeprav se je ta razlika pojavila v "združeni analizi različnih študij ni bila opažena v" stratificirani analizi.
Opis izbranih neželenih učinkov
Hipokalcemija
V dveh s placebom nadzorovanih kliničnih preskušanjih faze III pri ženskah s postmenopavzalno osteoporozo je približno 0,05% (2 od 4.050) bolnikov poročalo o znižanju koncentracije kalcija v serumu (manj kot 1,88 mmol / l) po uporabi zdravila Prolia. Po drugi strani pa v dveh s placebom nadzorovanih kliničnih preskušanjih faze III pri bolnikih, zdravljenih s hormonsko ablativno terapijo, ali v placebo kontroliranem kliničnem preskušanju faze III pri moški z osteoporozo.
V obdobju trženja so redki primeri simptomatske hude hipokalciemije poročali predvsem pri bolnikih, zdravljenih z zdravilom Prolia, s povečanim tveganjem za hipokalciemijo, kar se je v večini primerov pojavilo v prvih nekaj tednih po začetku zdravljenja. Primeri kliničnih manifestacij huda simptomatska hipokalciemija, vključno s podaljšanjem intervala QT, tetanijo, napadi in spremenjenim duševnim stanjem (glejte poglavje 4.4). Simptomi hipokalciemije v kliničnih preskušanjih z denosumabom so vključevali odrevenelost ali otrplost mišic, trzanje mišic, krče in krče.
Kožne okužbe
V s placebom nadzorovanih kliničnih preskušanjih faze III pri ženskah s postmenopavzalno osteoporozo je bila skupna incidenca kožnih okužb podobna v skupini, ki je prejemala placebo in Prolia (placebo [1,2%, 50 od 4.041] v primerjavi s Prolijo [1,5%, 59 od 4.050] pri moških z osteoporozo (placebo [0,8%, 1 od 120] v primerjavi s Prolijo [0%, 0 od 120]. Podobne dokaze so opazili tudi v kliničnih študijah s placebom kontroliranih preskušanjih III. faze pri bolnikih z rakom dojke ali prostate, zdravljenih z hormonsko ablativno zdravljenje (placebo [1,7%, 14 od 845] v primerjavi s Prolijo [1,4%, 12 od 860]). da je bila potrebna hospitalizacija pri 0,1%(3 od 4.041) žensk s postmenopavzalno osteoporozo, zdravljenih s placebom, v primerjavi z 0,4% (16 od 4.050) žensk, ki so prejemale zdravilo Prolia. Večinoma so bili to primeri celulita. in kožne okužbe, o katerih so poročali kot o resnih neželenih učinkih, so bile podobne v skupini, ki je prejemala placebo (0,6%, 5 od 845) in Prolia (0,6%, 5 od 860).
Osteonekroza spodnje čeljusti / maksile
V kliničnih preskušanjih pri osteoporozi in pri bolnikih z rakom dojke ali prostate, ki so prejemali hormonsko ablativno zdravljenje, je pri 14 bolnikih redko poročali o ONJ (glejte poglavje 4.4).
Atipični zlomi stegnenice
V kliničnem razvojnem programu za osteoporozo so pri bolnikih, zdravljenih z zdravilom Prolia, redko poročali o atipičnih zlomih stegnenice (glejte poglavje 4.4).
Katarakta
V enem samem s placebom kontroliranem kliničnem preskušanju faze III pri bolnikih z rakom prostate, ki so prejemali zdravljenje z odvzemom androgenov (ADT), so opazili razliko v pojavnosti katarakte (4,7% denosumaba, 1,2% placeba). Pri ženskah s postmenopavzalno osteoporozo niso opazili nobene razlike ali pri moških z osteoporozo ali pri ženskah, zdravljenih z zaviralci aromataze zaradi nemetastatskega raka dojke.
Divertikulitis
Razliko v incidenci divertikulitisa (1,2% denosumaba, 0% placeba) so opazili v enem samem s placebom kontroliranem kliničnem preskušanju faze III pri bolnikih z rakom prostate, ki so prejemali zdravljenje z odvzemom androgenov (ADT). L Incidenca divertikulitisa je bila primerljiva med skupinami zdravljenja pri ženskah s postmenopavzalno osteoporozo ali moških z osteoporozo in pri ženskah, zdravljenih z zaviralci aromataze za nemetastatski rak dojke.
Preobčutljivostne reakcije na zdravilo
V poročilih o trženju pri bolnikih, ki so prejemali zdravilo Prolia, so poročali o redkih preobčutljivosti na zdravilo, vključno z izpuščajem, urtikarijo, otekanjem obraza, eritemom in anafilaktičnimi reakcijami.
Mišično -skeletne bolečine
V obdobju trženja so pri bolnikih, zdravljenih z zdravilom Prolia, poročali o mišično-skeletnih bolečinah, vključno s hudimi primeri. V kliničnih preskušanjih so bile mišično-skeletne bolečine zelo pogoste tako v skupinah z denosumabom kot tudi v skupini, ki je prejemala placebo. Bolečine v mišično-skeletnem sistemu, ki so jih prekinitve v študijah bile redke.
Druge posebne populacije
V kliničnih preskušanjih so sodelovali bolniki s hudo ledvično okvaro (očistek kreatinina
Poročanje o domnevnih neželenih učinkih
Poročanje o domnevnih neželenih učinkih, ki se pojavijo po odobritvi zdravila, je pomembno, saj omogoča stalno spremljanje razmerja med koristmi in tveganji zdravila. Zdravstvene delavce prosimo, da o vsakem sumu na neželene učinke poročajo prek nacionalnega sistema za poročanje (Italijanska agencija za zdravila - spletna stran: https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse).
04.9 Preveliko odmerjanje
V kliničnih študijah niso poročali o primerih prevelikega odmerjanja. V kliničnih preskušanjih so denosumab dajali v odmerkih do 180 mg vsake 4 tedne (kumulativni odmerki do 1.080 mg v 6 mesecih) in nadaljnjih neželenih učinkov niso opazili.
05.0 FARMAKOLOŠKE LASTNOSTI
05.1 Farmakodinamične lastnosti
Farmakoterapevtska skupina: Zdravila za zdravljenje bolezni kosti - Druga zdravila, ki vplivajo na strukturo in mineralizacijo kosti, oznaka ATC: M05BX04
Mehanizem delovanja
Denosumab je človeško monoklonsko protitelo (IgG2), usmerjeno proti RANKL, na katerega se veže z visoko afiniteto in specifičnostjo ter preprečuje aktivacijo njegovega receptorja RANK, prisotnega na površini osteoklastov in njihovih prekurzorjev. Blokiranje interakcije med RANKL in RANK zavira nastanek, delovanje in preživetje osteoklastov, s čimer se zmanjša kostna resorpcija, tako na kortikalni kot na trabekularni ravni.
Farmakodinamični učinki
Zdravljenje z zdravilom Prolia je hitro zmanjšalo kostno obnovo in doseglo najvišjo vrednost serumskega markerja kostne resorpcije C-terminalnega kolapegena tipa I kolapeptida (CTX) v treh dneh (85-odstotno zmanjšanje) v 3 dneh. Na koncu vsakega odmernega intervala je bilo zmanjšanje CTX delno oslabljeno z največjega zmanjšanja za ≥ 87% na približno ≥ 45% (razpon 45-80%), kar odraža reverzibilnost učinkov zdravila Prolia na preoblikovanje kosti, ko se koncentracija v serumu zniža. Ti učinki so se ohranili z nadaljevanjem zdravljenja z zdravilom Prolia. Označevalci kostnega obnavljanja so običajno dosegli raven pred zdravljenjem v 9 mesecih po zadnjem odmerku.
Imunogenost
V kliničnih študijah niso opazili nevtralizirajočih protiteles proti Prolii. Na podlagi rezultatov občutljivega imunskega testa je bilo manj kot 1% bolnikov, zdravljenih z denosumabom do 5 let, pozitivno na nevtralizirajoča protitelesa brez dokazov o spremenjenem farmakokinetičnem, toksikološkem ali kliničnem profilu odziva.
Zdravljenje postmenopavzalne osteoporoze
Učinkovitost in varnost zdravila Prolia, danega vsakih 6 mesecev 3 leta, so ocenjevali pri ženskah po menopavzi (7.808 žensk, starih med 60 in 91 let, od tega 23,6% prevladujočih zlomov vretenc) z izhodiščno vrednostjo BMD (mineralna gostota kosti), izražena v ledvenem delu hrbtenice ali skupni T-rezultati stegnenice od -2,5 do -4,0 in z 10-letno povprečno absolutno verjetnostjo zloma 18,60% (decili: 7,9-32,4%) za večje osteoporozne zlome in 7,22% (decili: 1,4-14,9%) za zlomi kolka, ki vplivajo na presnovo kosti, so bili izključeni iz študije. Bolniki so dnevno prejemali dodatek kalcija (najmanj 1.000 mg) in vitamina D (najmanj 400 ie).
Učinki na zlome vretenc
Prolia je znatno zmanjšala tveganje za nove zlome vretenc pri 1, 2 in 3 letih (str
Tabela 2 Učinki zdravila Prolia na tveganje novih zlomov vretenc
* str
Učinki na zlome kolka
Zdravilo Prolia je pokazalo 40-odstotno relativno zmanjšanje (0,5-odstotno zmanjšanje absolutnega tveganja) pri 3-letnem tveganju zlomov kolka (str
V post-hoc analizi pri ženskah, starejših od 75 let, je zdravilo Prolia pokazalo relativno zmanjšanje tveganja za 62% (absolutno zmanjšanje tveganja za 1,4%, p
Učinki na vse klinične zlome
Zdravilo Prolia je znatno zmanjšalo vse vrste / skupine zlomov (glej tabelo 3).
Tabela 3 Učinki zdravila Prolia na 3-letno tveganje kliničnih zlomov
* p ≤ 0,05; ** p = 0,0106 (sekundarna končna točka po popravku večkratnosti), *** p ≤ 0,0001
+ Incidenca dogodkov na podlagi 3-letnih Kaplan-Meierjevih ocen.
1 Vključno s kliničnimi zlomi vretenc in nevretenčarji.
2 Razen tistih, ki prizadenejo vretenca, lobanjo, obraz, čeljust, metakarpus in falange prstov na rokah in nogah.
3 Vključuje medenico, distalno stegno, proksimalno golenico, rebra, proksimalni nadlahtnik, podlaket in stegnenico.
4 Vključno s kliničnimi zlomi vretenc, stegnenice, podlakti in nadlahtnice, kot jih opredeljuje WHO.
Pri ženskah z izhodiščno vrednostjo BMD, izraženo v vratu stegnenice, T-rezultat ≤-2,5 Prolia je zmanjšala tveganje zlomov brez vretenc (relativno zmanjšanje tveganja za 35%, absolutno zmanjšanje tveganja za 4,1%, p
Prolijino 3-letno zmanjšanje pojavnosti novih zlomov vretenc, zlomov kolka in nevretenčnih zlomov je ostalo konstantno, ne glede na izhodiščno tveganje zlomov pri 10 letih.
Učinki na mineralno gostoto kosti
V primerjavi s placebom je zdravilo Prolia znatno povečalo BMD na vseh skeletnih mestih, merjeno pri 1, 2 in 3 letih. Prolia je povečala BMD za 9,2% v ledvenem delu hrbtenice, za 6,0% v celotni stegnenici, za 4,8% v vratu stegnenice, za 7,9% v trohanterju, za 3,5% na ravni distalne tretjine polmera in 4,1% na ravni celotnega telesa v 3 letih (vse str
V kliničnih preskušanjih, ki so ocenjevali učinke prekinitve zdravljenja z zdravilom Prolia, se je BMD v 18 mesecih po zadnjem odmerku vrnila na približno raven pred zdravljenjem in ostala nad placebom. Ti podatki kažejo, da je za ohranitev učinka zdravljenja potrebno nadaljevanje zdravljenja z zdravilom Prolia.Z nadaljevanjem zdravljenja z zdravilom Prolia se je povečala BMD, podobno kot pri prvi uporabi zdravila Prolia.
Odprta podaljšana študija za zdravljenje postmenopavzalne osteoporoze
Skupaj 4.550 žensk (2.343 Prolia in 2.207 placebo), ki v zgoraj opisani ključni študiji niso zamudile več kot ene uporabe zdravil in so obisk zaključile v 36. mesecu študije, je dalo soglasje za vključitev v študijo Multinational, multicentrično, odprto, podaljšanje z eno roko, ki traja 7 let za oceno dolgoročne varnosti in učinkovitosti zdravila Prolia. Vse ženske v razširitveni študiji so prejemale zdravilo Prolia v odmerku 60 mg vsakih 6 mesecev, prav tako pa so prejemale dnevni kalcij ( vsaj 1 g) in vitamin D (najmanj 400 ie) .V 60. mesecu podaljšane študije se je po 8 letih zdravljenja z zdravilom Prolia v dolgotrajni skupini (n = 1542) BMD povečala za 18,4% pri ledvenem delu hrbtenice, 8,3% pri celotni stegnenici, 7,8% pri vratu stegnenice in 11,6% pri trohanterju od izhodišča v prvotni ključni študiji.
Incidenco zlomov so ocenili kot varnostno končno točko.
Od 4. do 8. leta se pojavnost novih zlomov vretenc in nevretenčarjev sčasoma ni povečala; incidenca na letni ravni je bila približno 1,1% oziroma 1,3%.
Med podaljšano študijo se je pojavilo osem potrjenih primerov osteonekroze čeljusti (ONJ) in dva atipična zloma stegnenice.
Zdravljenje osteoporoze pri moških
Učinkovitost in varnost zdravila Prolia, ki so ga jemali enkrat na 6 mesecev v enem letu, so ocenjevali pri 242 moških, starih od 31 do 84. let. in dodatek vitamina D (najmanj 800 ie).
Primarna spremenljivka učinkovitosti je bila odstotna sprememba BMD ledvene hrbtenice; Učinkovitost proti zlomom ni bila ovrednotena. Prolia je znatno povečala BMD na vseh skeletnih mestih v primerjavi s placebom pri 12 mesecih: 4,8% v ledvenem delu hrbtenice, 2,0% v celotni stegnenici, 2,2% v ravni vratu stegnenice, 2,3% v ravni trohanterja in 0,9% na ravni distalne tretjine polmera (vse str
Kostna histologija
Kostno histologijo so ovrednotili po 1-3 letih zdravljenja z zdravilom Prolia pri 62 ženskah s postmenopavzalno osteoporozo ali nizko kostno maso, ki niso prejemale osteoporoze ali so bile predhodno zdravljene z alendronatom. Enaindvajset žensk je sodelovalo v pod študiji biopsije kosti v 24. mesecu razširitvene študije. Kostno histologijo so ovrednotili tudi pri 17 moških z osteoporozo po 1 letu zdravljenja z zdravilom Prolia, rezultati biopsije kosti pa so pokazali kost normalne strukture in kakovosti brez dokazov o mineralizacijskih napakah, nelamelarni kosti ali medularni fibrozi.
Zdravljenje izgube kosti, povezane s terapijo pomanjkanja androgenov
Učinkovitost in varnost zdravila Prolia, ki se daje enkrat na 6 mesecev 3 leta, so ocenjevali pri moških s histološko potrjenim, nemetastatskim rakom prostate, zdravljenim z ADT (1468 moških, starih od 48 do 97 let), s povečanim tveganjem za zlom (opredeljeno kot starost). > 70 let oz
V primerjavi s placebom je zdravilo Prolia znatno povečalo BMD na vseh skeletnih mestih, merjeno pri 3 letih za 7,9% na ravni ledvene hrbtenice, za 5,7% na celotni ravni stegnenice, za 4,9% na vratu stegnenice, 6,9% na ravni trohanterja, 6,9% na distalni tretjini polmera in 4,7% na celotni ravni telesa (vse str
Zdravilo Prolia je pokazalo znatno zmanjšanje relativnega tveganja za nove zlome vretenc: 85% (absolutno zmanjšanje tveganja za 1,6%) po enem letu, 69% (absolutno zmanjšanje tveganja za 2,2%) po 2 letih in 62% (zmanjšanje absolutnega tveganja za 2,4%) ) pri 3 letih (vse str
Zdravljenje izgube kosti, povezane z adjuvantno terapijo z zaviralci aromataze
Učinkovitost in varnost zdravila Prolia, danega enkrat na 6 mesecev 2 leti, so ocenjevali pri ženskah z nemetastatskim rakom dojke (252 žensk, starih od 35 do 84 let), pri čemer so bile izhodiščne vrednosti BMD izražene v T-rezultatih. -2,5 na ravni ledvene hrbtenice, celotne stegnenice ali stegnenice. Vse ženske so dnevno prejemale dodatek kalcija (najmanj 1.000 mg) in vitamina D (najmanj 400 ie).
Primarni cilj študije o učinkovitosti je bila odstotna sprememba BMD v ledvenem delu hrbtenice, medtem ko učinkovitost zloma ni bila ovrednotena. , 4,7% na ravni celotne stegnenice, 3,6% na ravni vratu stegnenice, 5,9% na ravni trohanterja, 6,1% na ravni distalne tretjine polmera in 4,2% na ravni celotnega telesa (vse str
Pediatrična populacija
Evropska agencija za zdravila se je odpovedala obveznosti predložitve rezultatov študij z zdravilom Prolia v vseh podskupinah pediatrične populacije za zdravljenje izgube kosti, povezane s hormonsko ablativno terapijo, in v podskupinah pediatrične populacije mlajše starosti. zdravljenje osteoporoze. Za informacije o pediatrični uporabi glejte poglavje 4.2.
05.2 Farmakokinetične lastnosti
Absorpcija
Po subkutanem dajanju odmerka 1,0 mg / kg, kar ustreza približno odobrenemu odmerku 60 mg, je bila izpostavljenost na podlagi AUC 78% v primerjavi z intravenskim dajanjem istega odmerka.Za podkožni odmerek 60 mg je največja serumska koncentracija (Cmax) denosumaba 6 mcg / ml (razpon 1-17 mcg / ml) je bil dosežen v 10 dneh (razpon 2-28 dni).
Biotransformacija
Denosumab je sestavljen izključno iz aminokislin in ogljikovih hidratov, kot so nativni imunoglobulini, in ga s presnovo v jetrih verjetno ne bo izločil. Pričakuje se, da bo presnova in izločanje zdravila sledilo poti očistka imunoglobulina, kar ima za posledico razgradnjo v majhne peptide in posamezne aminokisline.
Odprava
Po doseganju Cmax se je koncentracija v serumu znižala s "razpolovno dobo 26 dni (razpon 6-52 dni) v obdobju 3 mesecev (razpon 1,5-4,5 mesecev). 53% bolnikov ni imelo količino merljivega denosumaba, ki bi ga bilo mogoče zaznati pri 6 mesecih" po dajanju odmerka.
Po večkratnem subkutanem odmerjanju 60 mg enkrat na 6 mesecev niso opazili kopičenja ali spremembe farmakokinetike denosumaba. Na farmakokinetiko denosumaba ni vplivalo nastajanje protiteles, ki se vežejo na zdravila, in so bile pri moških in ženskah podobne. Zdi se, da starost (28–87 let), rasa in stanje bolezni (zmanjšana kostna masa ali osteoporoza; rak prostate ali dojke) nimajo pomembnega vpliva na farmakokinetiko denosumaba.
Na podlagi AUC in Cmax je prišlo do trenda med večjo telesno težo in manjšo izpostavljenostjo zdravilu, vendar se ta trend ni obravnaval kot klinično pomemben, saj so bili farmakodinamični učinki, ki temeljijo na označevalcih kostnega preoblikovanja, in povečanju BMD konstantni v širokem razponu telesne mase. .
Linearnost / Nelinearnost
V študijah z razponom odmerkov je imel denosumab nelinearno, od odmerka odvisno farmakokinetiko, z manjšim očistkom pri večjih odmerkih ali koncentracijah, vendar s približno sorazmerno povečanjem izpostavljenosti za odmerke, ki so enaki ali večji do 60 mg.
Ledvična okvara
V študiji pri 55 bolnikih z različnimi stopnjami ledvične funkcije, vključno z bolniki na dializi, stopnja okvare ledvic ni vplivala na farmakokinetiko denosumaba.
Okvara jeter
Posebnih študij pri bolnikih z okvarjenim delovanjem jeter niso izvedli. Na splošno se monoklonska protitelesa ne odstranijo s presnovo v jetrih. Pričakuje se, da okvarjeno delovanje jeter ne vpliva na farmakokinetiko denosumaba.
Pediatrična populacija
Farmakokinetični profil pri pediatrični populaciji ni bil ovrednoten.
05.3 Predklinični podatki o varnosti
V študijah toksičnosti pri enkratnih in ponavljajočih se odmerkih pri opicah cynomolgus odmerki denosumaba, ki so povzročili sistemsko izpostavljenost do 100-150-krat večji od priporočenega odmerka pri ljudeh, niso vplivali na kardiovaskularno fiziologijo, plodnost samcev ali samic ali na produkt strupenosti za določene organe.
Standardni testi za raziskovanje potencialne genotoksičnosti denosumaba niso bili izvedeni, saj ti testi niso pomembni za to molekulo. Vendar glede na njegove značilnosti denosumab verjetno ne bo imel genotoksičnega potenciala.
Karcinogeni potencial denosumaba ni bil ocenjen v dolgotrajnih študijah na živalih.
V predkliničnih študijah, izvedenih pri izločenih miših, ki niso izražale RANK ali RANKL, so opazili oslabljeno tvorbo bezgavk pri plodu. Odsotnost laktacije zaradi zaviranja zorenja mlečne žleze (razvoj lobulo-alveolarnih struktur žleze med nosečnostjo) so opazili tudi pri izločenih miših, ki niso izrazile RANK ali RANKL.
V študiji, izvedeni pri opicah cynomolgus, zdravljenih v obdobju, enakovrednem prvemu trimesečju nosečnosti, z odmerki denosumaba, kar je povzročilo sistemsko izpostavljenost v smislu AUC do 99 -kratnega odmerka pri človeku (60 mg vsakih 6 mesecev), ne da bi to škodilo materi ali poročali so o plodu. Fetalne bezgavke v tej študiji niso bile pregledane.
V drugi študiji pri opicah cynomolgus, ki so bile med nosečnostjo zdravljene z odmerki denosumaba, kar je povzročilo sistemsko izpostavljenost glede na AUC 119 -krat večjo od odmerka, uporabljenega pri ljudeh (60 mg vsakih 6 mesecev), so opazili povečanje plodov. nenormalna rast kosti z zmanjšano trdnostjo kosti, zmanjšano hematopoezo in nepravilno postavitvijo zob; odsotnost perifernih bezgavk in zmanjšana rast novorojenčkov. Ni ugotovljena raven, pri kateri ne bi opazili škodljivih učinkov na reprodukcijo. Šest mesecev po rojstvu so opažene kostne nepravilnosti nazadovale in ni vplival na izbruh zob. Vendar so učinki na bezgavke in nepravilno poravnavo zob ostali, pri eni živali pa so opazili blago do zmerno mineralizacijo v različnih tkivih (negotova povezava z zdravljenjem). Pred porodom ni bilo dokazov o škodi pri materi; med porodom so redko poročali o neželenih dogodkih pri materi.Razvoj mlečnih žlez pri materi je bil normalen.
V predkliničnih študijah kakovosti kosti, opravljenih pri opicah, ki so bile dolgotrajno zdravljene z denosumabom, je zmanjšan kostni promet spremljala izboljšana trdnost kosti in normalna histologija. Ravni kalcija so se začasno znižale, medtem ko se je pri opicah, zdravljenih z denosumabom, pri jajčnikih, oprijemljenih s ščitnico, začasno povečalo.
Pri samcih miši, gensko spremenjenih za izražanje človeških RANKL (knockin miši) in podvrženih transkortikalnemu zlomu, je denosumab odložil odstranitev hrustanca in preoblikovanje kalusa v primerjavi s kontrolno skupino, vendar na biomehansko moč to ni negativno vplivalo.
Izločene miši (glejte poglavje 4.6), ki niso izrazile RANK ali RANKL, so pokazale izgubo teže, zmanjšano rast kosti in pomanjkanje izrastka zob. Pri neonatalnih podganah je bila inhibicija RANKL (tarča terapije z denosumabom) z visokimi odmerki Fc-vezanega osteoprotegerina (OPG-Fc) povezana z zaviranjem rasti kosti in zobnimi izbruhi. V tem modelu so bile te spremembe po prekinitvi dajanja zaviralca RANKL delno reverzibilne. Mladostni primati, zdravljeni z odmerki denosumaba 27 in 150 -krat (odmerki 10 in 50 mg / kg), višji od odmerkov, uporabljenih v kliniki, so pokazali nepravilnosti. Zato lahko zdravljenje z denosumabom poslabša rast kosti pri otrocih z odprtimi rastnimi ploščami in zavira izraščanje zob.
06.0 FARMACEVTSKE INFORMACIJE
06.1 Pomožne snovi
Ledena ocetna kislina *
Natrijev hidroksid (za uravnavanje pH) *
Sorbitol (E420)
Polisorbat 20
Voda za injekcije
* Acetatni pufer dobimo z mešanjem ocetne kisline in natrijevega hidroksida
06.2 Nezdružljivost
Ker študij združljivosti ni, se tega zdravila ne sme mešati z drugimi zdravili.
06.3 Obdobje veljavnosti
3 leta.
Prolia se lahko shranjuje pri sobni temperaturi (do 25 ° C) do 30 dni v originalni embalaži. Ko odstranite zdravilo iz hladilnika, ga morate uporabiti v tem 30 -dnevnem obdobju.
06.4 Posebna navodila za shranjevanje
Shranjujte v hladilniku (2 ° C - 8 ° C).
Ne zamrzujte.
Napolnjeno injekcijsko brizgo shranjujte v zunanji ovojnini, da zdravilo zaščitite pred svetlobo.
06.5 Vrsta ovojnine in vsebina pakiranja
1 ml raztopine v napolnjeni injekcijski brizgi iz stekla tipa I za enkratno uporabo z iglo iz nerjavečega jekla 27, z ali brez ščitnika za iglo.
Pokrovček igle napolnjene injekcijske brizge vsebuje suh naravni kavčuk, ki je derivat lateksa (glejte poglavje 4.4).
Velikost pakiranja ene brizge z pretisnim omotom (napolnjena injekcijska brizga z ali brez ščitnika za iglo) ali brez pretisnega omota (samo napolnjena injekcijska brizga).
06.6 Navodila za uporabo in rokovanje
Pred uporabo je treba raztopino pregledati. Raztopine ne injicirajte, če vsebuje vidne delce ali če je motna ali razbarvana. Ne pretresite pretirano. Da bi se izognili reakcijam na mestu injiciranja, pustite, da napolnjena injekcijska brizga pred injiciranjem doseže sobno temperaturo (do 25 ° C) in jo injicirajte počasi. Injicirajte celotno vsebino napolnjene injekcijske brizge. Zavrzite vse ostanke zdravila, ki so ostali v napolnjeni injekcijski brizgi.
Neuporabljeno zdravilo in odpadke, pridobljene iz tega zdravila, je treba odstraniti v skladu z lokalnimi predpisi.
07.0 IMETNIK DOVOLJENJA ZA PROMET
Amgen Europe B.V.
Minervum 7061
NL-4817 ZK Breda
Nizozemska
08.0 ŠTEVILKA DOVOLJENJA ZA PROMET
EU/1/10/618/001
EU/1/10/618/002
EU/1/10/618/003
040108019
040108033
040108021
09.0 DATUM PRVEGA DOVOLJENJA ALI PODALJŠANJA DOVOLJENJA
Datum prve odobritve: 26. maj 2010
Datum zadnje obnove: 15. januar 2015
10.0 DATUM REVIZIJE BESEDILA
Junija 2015