Aktivne sestavine: Tizanidin
Tablete Navizan
Navodilo za uporabo vira: AIFA (Italijanska agencija za zdravila). Vsebina, objavljena januarja 2016. Prisotne informacije morda niso posodobljene.
Za dostop do najnovejše različice je priporočljivo dostopati do spletnega mesta AIFA (Italijanska agencija za zdravila). Zavrnitev odgovornosti in koristne informacije.
01.0 IME ZDRAVILA -
NAVIZAN
02.0 KAKOVOSTNA IN KOLIČINSKA SESTAVA -
Ena tableta vsebuje 2 mg tizanidina (v obliki tizanidinijevega klorida)
Ena tableta vsebuje 4 mg tizanidina (v obliki tizanidinijevega klorida)
Pomožne snovi z znanimi učinki: laktoza v obliki brezvodne laktoze, 47,21 mg na tableto
Pomožne snovi z znanimi učinki: laktoza v obliki brezvodne laktoze, 94,42 mg na tableto
Za celoten seznam pomožnih snovi glejte poglavje 6.1.
03.0 FARMACEVTSKA OBLIKA -
Tablete.
Bele do sivobele, ovalne, ravne table s poševnim robom, z vtisnjeno oznako "R179" na eni strani in prepolovljeno z "razrezom na drugi strani".
Bele do umazano bele, ovalne, ravne table s poševnim robom, z vtisnjenim napisom "R180" na eni strani in četrtino z "razrezom na drugi strani".
Črta na tableti je namenjena olajšanju lomljenja za lažje požiranje in ne razdelitvi na enake odmerke.
04.0 KLINIČNE INFORMACIJE -
04.1 Terapevtske indikacije -
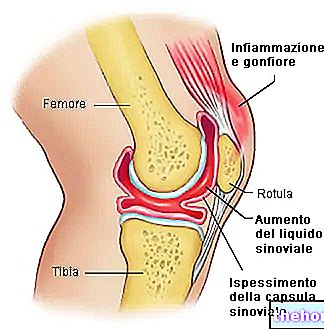
Tizanidin je pri odraslih indiciran za zdravljenje spastičnih stanj, povezanih z multiplo sklerozo ali poškodbo ali boleznijo hrbtenice.
04.2 Odmerjanje in način uporabe -
Odmerjanje
Učinek tinazidina na spastičnost je največji v 2 do 3 urah po dajanju in ima relativno kratko delovanje. Čas in pogostost dajanja je zato treba individualno prilagoditi, tizanidin pa je treba dajati v razdeljenih odmerkih do 3-4 krat na dan, odvisno od bolnikovih potreb. Odziv med bolniki je precej različen, zato je potrebna previdna prilagoditev odmerka. Paziti je treba, da ne presežete odmerka, ki povzroči želeni terapevtski učinek.Ponavadi se začne enkratni odmerek 2 mg in poveča v korakih po 2 mg v presledkih, ki niso krajši od pol tedna.
Skupni dnevni odmerek ne sme presegati 36 mg, čeprav običajno ni potrebno preseči 24 mg / dan. Sekundarni farmakološki učinki (glejte poglavje 4.8) se lahko pojavijo pri terapevtskih odmerkih, vendar jih je mogoče zmanjšati s počasnim prilagajanjem odmerka, tako da pri veliki večini bolnikov to ni omejevalni dejavnik.
Upokojenci
Izkušnje pri starejših so omejene in uporaba tizanidina ni priporočljiva, razen če korist zdravljenja očitno odtehta tveganje. Farmakokinetični podatki kažejo, da se ledvični očistek pri starejših lahko zmanjša do 3-krat.
Bolniki z okvaro ledvic
Pri bolnikih z ledvično insuficienco (očistek kreatinina je treba ustrezno spremljati.
Bolniki z okvaro jeter
Tizanidin je kontraindiciran pri bolnikih z znatno okvarjenim delovanjem jeter. Tizanidina se ne sme uporabljati pri bolnikih z zmerno okvaro jeter, razen če možna korist odtehta možno tveganje za bolnika. Začnite kakršno koli zdravljenje z najnižjim odmerkom, nato pa previdno povečajte odmerek in glede na bolnikovo prenašanje.
Pediatrična populacija
Izkušnje s tizanidinom pri bolnikih, mlajših od 18 let, uporabe tizanidina pri otrocih niso priporočljive.
Način dajanja
Ustno dajanje
04.3 Kontraindikacije -
Preobčutljivost za zdravilno učinkovino ali katero koli pomožno snov, navedeno v poglavju 6.1.
Uporaba tizanidina pri bolnikih z znatno okvarjenim delovanjem jeter je kontraindicirana, saj se tizanidin v veliki meri presnavlja v jetrih (glejte poglavje 5.2).
Sočasna uporaba tizanidina z močnimi zaviralci CYP1A2 (kot sta fluvoksamin ali ciprofloksacin) je kontraindicirana (glejte poglavji 4.4 in 4.5).
04.4 Posebna opozorila in ustrezni previdnostni ukrepi pri uporabi -
Sočasna uporaba tizanidina z zaviralci CYP1A2 ni priporočljiva (glejte poglavji 4.3 in 4.5).
Med zdravljenjem s tizandinom se lahko pojavi hipotenzija (glejte poglavje 4.8) in tudi kot posledica medsebojnega delovanja zdravil z zaviralci CYP1A2 in / ali antihipertenzivnimi zdravili (glejte poglavje 4.5). Opazili so hude manifestacije hipotenzije, kot sta izguba zavesti in srčno -žilni kolaps.
Po nenadni prekinitvi zdravljenja s tizanidinom pri kronični uporabi in / ali pri visokih dnevnih odmerkih in / ali v kombinaciji z drugimi antihipertenzivnimi zdravili so opazili povratno hipertenzijo in tahikardijo (glejte poglavje 4.5). V skrajnih primerih lahko povratna hipertenzija povzroči cerebrovaskularne dogodke.Tizanidina ne smemo prekiniti nenadoma, ampak postopoma in z rednimi kontrolami krvnega tlaka.
Odpoved ledvic
Bolniki z ledvično insuficienco bodo morda potrebovali manjše odmerke, zato je pri teh bolnikih potrebna previdnost (glejte poglavje 4.2).
Bolezni jeter
V povezavi s tizanidinom so poročali o jetrni disfunkciji. Priporočljivo je, da se v prvih 4 mesecih zdravljenja pri vseh bolnikih in pri tistih s kliničnimi simptomi, ki kažejo na disfunkcijo jeter, kot so nepojasnjena slabost, anoreksija ali utrujenost, mesečno spremljajo jetrne teste. Zdravljenje s tizanidinom je treba prekiniti, če so serumske koncentracije glutaminske piruvične transaminaze (SGPT) v serumu in / ali glutaminske oksaloacetia transaminaze (SGOT) v serumu dosledno nad 3 -kratno najvišjo normalno vrednostjo.
Pediatrična populacija
Tizanidin je treba hraniti izven dosega in pogleda otrok.
Pomožne snovi
Tablete Navizan vsebujejo laktozo. To zdravilo ni priporočljivo pri bolnikih z redkimi dednimi težavami, kot so intoleranca za galaktozo, hudo pomanjkanje laktaze ali malabsorpcija glukoze-galaktoze.
04.5 Interakcije z drugimi zdravili in druge oblike interakcij -
Tizanidin se skoraj izključno presnavlja z izoencimom citokroma P450 CYP1A2. Sočasna uporaba zdravil, za katera je znano, da zavirajo ali inducirajo aktivnost CYP1A2, lahko poveča plazemske ravni tizanidina.
Opažene interakcije, ki vodijo do kontraindikacij
Sočasna uporaba tizanidina s fluvoksaminom ali ciprofloksacinom, ki sta močna zaviralca CYP1A2, je kontraindicirana. Sočasna uporaba tizanidina s fluvoksaminom oziroma ciprofloksacinom je povzročila 33-kratno oziroma 10-kratno povečanje AUC tizanidina, klinično pomembno in podaljšano hipotenzijo. lahko povzroči zaspanost, omotico in zmanjšano psihomotorično zmogljivost (glejte poglavji 4.3 in 4.4).
Opažene interakcije, ki ne priporočajo sočasne uporabe
Sočasna uporaba tizanidina z drugimi zaviralci CYP1A2, kot so nekateri antiaritmiki (amiodaron, meksiletin, propafenon), cimetidin, nekateri fluorokinoloni (enoksacin, norfloksacin,) in tiklopidin, ni priporočljiva (glejte poglavje 4.4).
Povišane koncentracije tizanidina v plazmi lahko povzročijo simptome prevelikega odmerjanja, na primer podaljšanje intervala QT (c) (glejte poglavje 4.9).
Sočasna uporaba tizanidina (v velikih odmerkih) z drugimi zdravili, ki lahko podaljšajo QT (c) (npr. Amitriptilin in azitromicin), ni priporočljiva.
Zaradi možnih aditivnih hipotenzivnih učinkov sočasna uporaba tizanidina z drugimi adrenergičnimi agonisti alfa-2 (kot je klonidin) ni priporočljiva.
Peroralni kontraceptivi
Farmakokinetični podatki po enkratnih in večkratnih odmerkih tizanidina kažejo, da se očistek tizanidina zmanjša za približno 50% pri ženskah, ki sočasno jemljejo peroralne kontraceptive.
Čeprav ni bila izvedena nobena posebna farmakokinetična študija za preučitev možne interakcije med peroralnimi kontraceptivi in tizanidinom, je treba pri predpisovanju tizanidina bolniku, ki jemlje kontracepcijske tablete, upoštevati možnost kliničnega odziva in / ali neželenih učinkov na nizke odmerke tizanidina. V kliničnih preskušanjih niso poročali o nobenih klinično pomembnih interakcijah z zdravili.
Interakcije, ki jih je treba upoštevati
Rifampicin
Sočasna uporaba tizanidina in rifampicina povzroči 50 -odstotno zmanjšanje koncentracij tizanidina. Zato se lahko med zdravljenjem z rifampicinom terapevtski učinek tizanidina zmanjša, kar je pri nekaterih bolnikih lahko klinično pomembno. ).
Dim cigaret Izpostavljenost policikličnim aromatskim ogljikovodikom iz cigaretnega dima vodi do indukcije CYP1A2.
Dajanje tizanidina moškim kadilcem (> 10 cigaret na dan) povzroči približno 30% zmanjšanje sistemske izpostavljenosti tizanidinu.
Antihipertenzivi
Tizanidin lahko povzroči hipotenzijo (glejte poglavje 4.4) in poveča učinek hipotenzivnih zdravil, vključno z diuretiki, zato je pri bolnikih na hipotenzivnem zdravljenju potrebna previdnost.
Alkohol
Med zdravljenjem s tizanidinom je treba uživanje alkohola zmanjšati ali se mu izogniti, saj lahko poveča potencialne neželene učinke (npr. Sedacijo in hipotenzijo). Tizanidin lahko poveča depresivni učinek alkohola na centralni živčni sistem.
Prav tako je potrebna previdnost pri uporabi tizanidina z zaviralci adrenergičnih receptorjev beta ali digoksinom, saj lahko kombinacija poveča hipotenzijo ali bradikardijo.
Pri sočasni uporabi tizanidina s pomirjevalnimi zdravili, vključno s hipnotiki (npr. Benzodiazepini), antihistaminiki (npr. Klorfenamin) in baklofenom, je potrebna previdnost zaradi možnega povečanja sedativnega učinka tizanidina.
04.6 Nosečnost in dojenje -
Nosečnost
Podatkov o uporabi tizanidina pri nosečnicah ni ali so omejeni.Študije na živalih so pokazale reproduktivno strupenost (glejte poglavje 5.3).
Tizanidin ni priporočljiv med nosečnostjo in pri ženskah v rodni dobi, ki ne uporabljajo kontracepcijskih sredstev.
Čas hranjenja
Majhne količine tizanidina se izločajo v mleko podgan (glejte poglavje 5.3). Ker tveganja za dojenega dojenčka ni mogoče izključiti, se tizanidina med dojenjem ne sme uporabljati.
Plodnost
Študije na živalih pri podganah samcih in samicah niso pokazale vpliva na plodnost pri odmerkih 10 mg / kg / dan oziroma 3 mg / kg / dan (glejte poglavje 5.3).
04.7 Vpliv na sposobnost vožnje in upravljanja s stroji -
Bolnikom z zamegljenim vidom, zaspanostjo, utrujenostjo ali drugimi simptomi hipotenzije je treba odsvetovati opravljanje dejavnosti, ki zahtevajo visoko stopnjo pozornosti, na primer vožnjo ali upravljanje strojev.
04.8 Neželeni učinki -
Neželeni učinki (preglednica 1) so navedeni po pogostnosti, najprej najpogostejši, v skladu z naslednjo konvencijo: zelo pogosti (≥1 / 10), pogosti (≥1 / 100 in
1 Halucinacije so samoomejujoče, brez dokazov o psihozi in so se vedno pojavljale pri bolnikih, ki sočasno jemljejo potencialno halucinogena zdravila, kot so antidepresivi.
2 Prišlo je do povišanja jetrnih serumskih transaminaz, ki so po prekinitvi zdravljenja reverzibilne.
Pri majhnih odmerkih so poročali o zaspanosti, utrujenosti, omotici, suhih ustih, znižanem krvnem tlaku, slabosti, prebavnih motnjah in povišanih transaminazah, na splošno kot blagih in prehodnih dogodkih.
Pri večjih odmerkih so bili dogodki, o katerih so poročali pri majhnih odmerkih, pogostejši in izrazitejši, vendar le redko dovolj hudi, da bi upravičili prekinitev zdravljenja.
Prekinitvena povratna hipertenzija lahko v hudih primerih povzroči cerebrovaskularne dogodke.
Poročanje o domnevnih neželenih učinkih
Poročanje o domnevnih neželenih učinkih, ki se pojavijo po odobritvi zdravila, je pomembno, saj omogoča stalno spremljanje razmerja med koristjo in tveganjem zdravila.
Zdravstvene delavce prosimo, da o vsakem domnevnem neželenem učinku poročajo prek nacionalnega sistema poročanja na naslovu www.agenziafarmaco.gov.it/it/responsabili
04.9 Preveliko odmerjanje -
Klinične izkušnje so omejene. V enem primeru odrasle osebe, ki je zaužila 400 mg tizanidina, okrevanje ni potekalo. Bolnik je bil zdravljen z manitolom in furosemidom.
Simptomi:
Slabost, bruhanje, hipotenzija, podaljšanje intervala QT (c), omotica, mioza, težave z dihanjem, koma, nemir, zaspanost.
Zdravljenje.
Navedeni so splošni podporni ukrepi in poskusiti je treba zaužite snovi odstraniti iz prebavil z izpiranjem želodca ali aktivnim ogljem. Prisilna diureza naj bi pospešila izločanje tizanidina. Nadaljnja zdravljenja bi morala biti simptomatska. Bolnik mora biti dobro hidriran.
05.0 FARMAKOLOŠKE LASTNOSTI -
05.1 "Farmakodinamične lastnosti -
Farmakoterapevtski razred: mišično relaksanti s centralnim delovanjem, drugi mišični relaksanti s centralnim delovanjem.
Oznaka ATC: M03BX02.
Tizanidin je agonist adrenergičnih receptorjev alfa2 v centralnem živčnem sistemu na nad-spinalni in spinalni ravni. Ta vpliv določa "zaviranje" refleksne polisinaptične aktivnosti hrbtenice. Tizanidin nima neposrednega učinka na skeletne mišice, živčno -mišične stike ali spinalne monosinaptične reflekse.
Pri ljudeh tizanidin zmanjša patološko povečan mišični tonus, vključno z odpornostjo na pasivno gibanje, in lajša boleče krče in klone.
05.2 "Farmakokinetične lastnosti -
Absorpcija in distribucija
Tizanidin se hitro absorbira in doseže najvišjo plazemsko koncentracijo v približno 1 uri. Tizanidin je le 30% vezan na beljakovine v plazmi in v študijah na živalih je bilo dokazano, da zlahka prečka krvno-možgansko pregrado. Povprečni volumen porazdelitve v stanju dinamičnega ravnovesja (Vss) po i.v. je 2,6 l / kg (CV 21%). Čeprav se tizanidin zlahka absorbira, presnova prvega prehoda omeji biološko uporabnost na 34% intravenskega odmerka. Največja plazemska koncentracija (Cmax) tizanidina je 12,3 ng / ml (koeficient variacije, CV, 56%) oziroma 15,6 ng / ml (CV 60%) po enkratnem in 4 -kratnem dajanju 4 mg.
Sočasno zaužitje hrane nima vpliva na farmakokinetični profil tablet tizanidina (v obliki tablet po 4 mg). Čeprav je vrednost Cmax po dajanju tablete v pogojih hranjenja približno 1/3 višja, se ne šteje za klinični pomen, tako kot učinek na obseg absorpcije (AUC) ni pomemben.
Biotransformacija in izločanje
Tizanidin se hitro in v veliki meri (približno 95%) presnovi v jetrih, vzorec biotransformacije pri živalih in ljudeh je kakovostno podoben.Tizanidin se in vitro presnavlja predvsem s citokromom p450 1A2. (približno 70% danega odmerka in se zdi, da je praktično neaktiven) .Ledvično izločanje (določeno z odstotkom celotne uporabljene radioaktivnosti v urinu) je približno 53% po enkratnem odmerku 5 mg in 66% po dajanje 4 mg trikrat na dan. Razpolovni čas tizanidina iz plazme je 2-4 ure.
Linearnost / nelinearnost
Tizanidin ima linearno farmakokinetiko v razponu odmerkov od 1 do 20 mg.
Značilnosti pri posebnih populacijah bolnikov
Bolniki z okvaro ledvic
Pri bolnikih s hudo okvaro ledvic (očistek kreatinina
Bolniki z okvaro jeter
Posebne študije pri tej populaciji niso bile izvedene. Ker se tizanidin v jetrih obsežno presnavlja z encimom CYP1A2, lahko okvara jeter poveča njegovo sistemsko izpostavljenost. Tizanidin je kontraindiciran pri bolnikih s hudo okvaro jeter (glejte poglavje 4.3).
Starejša populacija
Farmakokinetični podatki pri tej populaciji so omejeni.
Spol in narodnost
Spol nima klinično pomembnega vpliva na farmakokinetiko tizanidina. Vpliv etnične občutljivosti in rase na farmakokinetiko tizanidina ni bil raziskan.
05.3 Predklinični podatki o varnosti -
Akutna strupenost
Tizanidin ima nizko stopnjo akutne toksičnosti. Po enkratnih odmerkih> 40 mg / kg so pri živalih opazili znake prevelikega odmerjanja in so povezani s farmakološkim delovanjem zdravila.
Strupenost pri ponavljajočih se odmerkih
Strupeni učinki tizanidina so predvsem posledica njegovega farmakološkega delovanja. Pri odmerkih 24 in 40 mg / kg / dan v subkroničnih študijah pri glodalcih učinek agonista alfa 2 vodi do stimulacije centralnega živčnega sistema, npr. Motoričnega vzbujanja, agresije, tremorja in krčev.
Znaki, povezani s centralno posredovano sprostitvijo mišic, npr. sedacijo in ataksijo so pogosto opazili pri nižjih odmerkih v študijah subkronične in kronične peroralne toksičnosti pri psih. Ti znaki, povezani z miotonolitično aktivnostjo zdravila, so bili opaženi pri odmerkih 1- 4 mg / kg / dan v 13-tedenski študiji pri psu in 1,5 mg / kg / dan v 52-tedenski študiji pri psu.
V študijah kronične toksičnosti pri psih v odmerkih 1,0 mg / kg / dan in več so opazili podaljšanje intervala QT in bradikardijo.
V več študijah toksičnosti so pri večjih odmerkih opazili rahlo zvišanje serumskih transaminaz. Te niso bile vedno povezane s histopatološkimi spremembami v jetrih.
Mutageneza
Različni testi in vitro in in vivo, niso dokazali mutagenega potenciala tizanidina.
Kancerogeneza
V dveh dolgotrajnih študijah na miših (78 tednov) in podganah (104 tedni) pri odmerkih do 9 mg / kg / dan pri podganah in do 16 mg / kg / dan pri podganah niso dokazali nobenih dokazov o rakotvornosti miška. Pri teh ravneh odmerkov, ki ustrezajo največjemu dopustnemu odmerku, na podlagi zmanjšanja hitrosti razvoja niso opazili neoplastičnih ali pred-neoplastičnih patologij, ki bi jih pripisali zdravljenju.
Strupenost za razmnoževanje
Študije razmnoževanja pri podganah v odmerku 3 mg / kg / dan in pri kuncih v odmerku 30 mg / kg / dan tizanidina niso pokazale nobenih znakov teratogenosti. Odmerki 10 in 30 mg / kg / dan so podaljšali obdobje brejosti in distocijo pri samicah podgan. Opazili so povečanje izgube ploda in mladičev ter zaostanek v razvoju (kar dokazujejo zmanjšana telesna teža ploda in zapoznela okostenelost okostja). Pri teh odmerkih so matere pokazale izrazite znake mišične sprostitve in sedacije.
Pri podganah samcev pri odmerku 10 mg / kg / dan in pri samicah pri odmerku 3 mg / kg / dan niso opazili zmanjšanja plodnosti. Plodnost se je zmanjšala pri samcih podganah, zdravljenih s 30 mg / kg / dan (popolnoma reverzibilno po obdobju okrevanja po 2 tednih), in pri podganah samicah z 10 mg / kg / dan. Pri teh odmerkih so opazili vedenjske učinke matere in klinične znake, vključno z izrazito sedacijo, izgubo teže in ataksijo.
Znano je, da tizanidin in / ali njegovi presnovki prehajajo v mleko glodalcev.
06.0 FARMACEVTSKE INFORMACIJE -
06.1 Pomožne snovi -
Brezvodna laktoza,
mikrokristalna celuloza,
brezvodni koloidni silicijev dioksid, stearinska kislina.
06.2 Nezdružljivost "-
Se ne uporablja.
06.3 Obdobje veljavnosti "-
3 leta.
06.4 Posebna navodila za shranjevanje -
Ne shranjujte pri temperaturah nad 30 ° C.
06.5 Vrsta neposredne embalaže in vsebina pakiranja -
PVC / PVdC - aluminijasti pretisni omoti.
Pretisni omoti po 15, 20, 30, 100 in 120 tablet.
Na trgu ni vseh navedenih pakiranj
06.6 Navodila za uporabo in ravnanje -
Brez posebnih navodil.
07.0 IMETNIK "DOVOLJENJA ZA PROMET" -
I.B.N SAVIO S.R.L, Via del Mare 36
00071 Pomezia
Rim
Prodajalec prodam :
Itapharma Srl - Via Ponte a Piglieri n. 8, 56121 Pisa
08.0 ŠTEVILKA DOVOLJENJA ZA PROMET -
"2 mg tablete" 15 tablet v pretisnem omotu Pvc / Pvdc / Al AIC n. 039422011
"2 mg tablete" 20 tablet v pretisnem omotu Pvc / Pvdc / Al AIC n. 039422023
"2 mg tablete" 30 tablet v pretisnem omotu Pvc / Pvdc / Al AIC n. 039422035
"2 mg tablete" 100 tablet v pretisnem omotu Pvc / Pvdc / Al AIC n. 039422047
"2 mg tablete" 120 tablet v pretisnem omotu Pvc / Pvdc / Al AIC n. 039422050
"4 mg tablete" 15 tablet v pretisnem omotu Pvc / Pvdc / Al AIC n. 039422062
"4 mg tablete" 20 tablet v pretisnem omotu Pvc / Pvdc / Al AIC n. 039422074
"4 mg tablete" 30 tablet v pretisnem omotu Pvc / Pvdc / Al AIC n. 039422086
"4 mg tablete" 100 tablet v pretisnem omotu Pvc / Pvdc / Al AIC n. 039422098
"4 mg tablete" 120 tablet v pretisnem omotu Pvc / Pvdc / Al AIC n. 039422100
09.0 DATUM PRVEGA DOVOLJENJA ALI PODALJŠANJA DOVOLJENJA -
05/03/2010